трисомия по 16 хромосоме что это значит
Предимплантационный скрининг и хромосомные нарушения
Предимплантационный генетический скрининг (ПГС) представляет собой метод диагностики ЭКО-эмбрионов с целью обнаружения у них хромосомной патологии. Возможны сбои как в количестве хромосом эмбриона, так и в их распределении. Необходимо помнить, что ПГС не предназначен для выявления носительства конкретных генетических болезней, в отличие от ПГД.
В последнее время активно применяется новейший метод исследования хромосомных нарушений плода – неинвазивная пренатальная диагностика (НПД / NIPT). Данный метод позволяет выявить анеуплодии у плода лишь с использованием венозной крови матери, т.е. без какого-либо воздействия на плод. Эффективность НПД очень высока, составляя 90-99%, и его применение возможно уже с 10 недели беременности.
Что такое анеуплоидии?
Человеческая яйцеклетка в большинстве случаев является носителем хромосомного набора с патологией, и процент таких ненормальных яйцеклеток увеличивается с возрастом женщины. В общей сложности, порядка 50% человеческих эмбрионов имеют тот или иной тип хромосомной аномалии, говоря медицинским языком – анеуплоидии.
Анеуплоидия переводится с греческого языка как «не полностью кратный вид», т.е. это явление, при котором изменяется число хромосом в клетках организма. В норме каждый человек является носителем диплоидного (двойного) набора хромосом, состоящего из аутосом – 22 пары и половых хромосом – 2 штуки, в соматических клетках. В половых клетках (гаметах) человека содержится гаплоидный (одинарный) набор хромосом, который в момент оплодотворения превращается в диплоидный набор.
Анеуплоидии в сторону уменьшения количества хромосом, т.е. отсутствие 1 хромосомы в любой из хромосомных пар, называются моносомией. В большинстве случаев из-за отсутствия аутосомы у плода развиваются пороки не совместимые с жизнью, приводящие либо к его внутриутробной гибели, либо к спонтанному выкидышу.
Вследствие анеуплоидии хромосомный набор может также увеличиваться, приводя к явлению полисомии (полиплоидии) в виде трисомии – добавляется одна хромосома, тетрасомии – добавляются две хромосомы и пентасомии – добавляются три хромосомы. Данная патология, как правило, так же не совместима с жизнью, но есть некоторые виды этих нарушений, с которыми рождаются детки.
Показания к предимплантационной генетической диагностике
В настоящее время сфера предимплантационной генетической диагностики и скрининга является одной из самых динамично развивающихся областей репродуктивной медицины.
Данное исследование может быть рекомендовано для выявления анеуплоидии в следующих случаях:
В заключение хочу сказать, что даже в ситуации неблагоприятной наследственности Вы можете стать родителями малыша, который будет здоров с высокой долей вероятности. Помогут Вам в этом предимплантационный генетический скрининг ЭКО-эмбрионов и неинвазивная пренатальная диагностика материнской крови.
Статьи
Классификация хромосомных болезней
Хромосомные болезни появляются вследствие повреждений ге¬нома, возникающих при созревании гамет, в процессе оплодотворе¬ния или на ранних стадиях дробления зиготы. Все хромосомные болезни могут быть разделены на 3 большие группы:
1) связанные с нарушением плоидности;
2) обусловленные нарушением числа хро¬мосом;
3) связанные сизменением структуры хромосом.
Аномалии хромосом, связанные с нарушением плоидности, пред¬ставлены триплоидией и тетраплоидией, которыевстречаются пре¬имущественно в материале спонтанных абортусов. Отмечены лишь единичные случаи рождения детей-триплоидов с тяжелыми МВПР, несовместимыми с нормальной жизнедеятельностью. Триплоидия может возникать каквследствие дигении (оплодотворение дипло¬идной яйцеклетки гаплоидным сперматозоидом), так и вследствие диандрии (обратный вариант) и диспермии (оплодотворение гап¬лоидной яйцеклетки двумя сперматозоидами).
Хромосомные болезни, связанные с нарушением структуры хро¬мосом, представляют большую группу синдромов частичных моно- или трисомии. Как правило, они возникают в результате структурных перестроек хромосом, имеющихся вполовых клетках родите¬лей, которые вследствие нарушения процессов рекомбинации в мейозе приводят к утрате или избытку фрагментов хромосом, вовлечен¬ных в перестройку. Частичные моно- или трисомии известны практи¬чески повсем хромосомам, но лишь некоторые из них формируют четко диагностируемые клинические синдромы. Фенотипические про-явления этих синдромов более полиморфны, чем синдромов целых моно- и трисомии. Отчасти этосвязано с тем, что размеры фрагмен¬тов хромосом и, следовательно, их генный состав, могут варьиро¬вать в каждом отдельном случае, а также тем, что при наличии хро¬мосомной транслокации у одного из родителей частичная трисомия поодной хромосоме у ребенка может сочетаться с частичной моно¬сомией по другой.
Клинико-цитогенетическая характеристика синдромов, связанных с числовыми аномалиями хромосом
Синдром трисомии хромосомы 8. Впервые описан в 1962 году. Популяционная частота 1 на 50000. Возникает врезультате нерас¬хождения хромосом на ранних стадиях бластулы, кроме редких слу¬чаев мутаций de novo в гаметогенезе. Цитогенетически выявляются как полные, так и мозаичные формы, которые составляют до 90% всех случаев. Различий поклинической картине таких форм нет. Не обнаружено корреляции между тяжестью заболевания и долей мо¬заичного клона.
Основными диагностическими признаками данного синдрома яв¬ляются: макроцефалия, микрогнатия, вывернутая нижняя губа, мас¬сивный выступающий лоб, широкая спинка носа, высокое акровидное небо, большие оттопыренные уши с выступающим противозавитком. Кроме того, имеются аномалии скелета, выражающиеся в добавочных ребрах и позвонках, закрытые спинномозговые грыжи в шейном и грудном отделах позвоночника, аплазия и гипоплазия надколенника, короткая шея. Имеются множественные контрактуры су¬ставов, клинодактилия, камптодактилия. Распространены пороки мо-чевой системы, особенно гидронефроз. Диагностируют пороки серд¬ца, особенно дефекты перегородок и крупных сосудов. Интеллект у больных снижен, отмечена задержка психомоторного и речевого раз-вития. Прогноз физического, психического развития и жизни небла¬гоприятный, хотя и отмечены пациенты в возрасте 17 лет.
Синдром трисомии хромосомы 9. Описан в 1970 году. В осно¬ве этиологии лежит нерасхождение хромосом на раннихстадиях бла¬стулы, кроме редких случаев мутаций de novo в гаметогенезе. Цито-генетически отмечены полные формытрисомии и мозаики (50%). Му¬тации de novo составляют 1/3 всех описанных случаев. Кроме полных аутосомных трисомийхромосомы 9 выявлены также делеции дистального участка ее длинного плеча. Транслокационные варианты встречаются редко.
Основными диагностическими признаками синдрома трисомий 9 являются: микроцефалия (долихоцефалия), глубокопосаженные гла¬за, высокий лоб, широкая переносица, бульбообразный нос, высо¬кое небо, часто с расщелиной, микроретрогнатия. Ушные раковины деформированы и низко посажены, отмечается короткая шея с низ¬кой линией роста волос. Наблюдаются аномалии развития опорно-двигательного аппарата, включающие дисплазию тазобедренного сустава, вывих локтевого или коленного суставов, аномалии ребер. У мальчиков выражен крипторхизм и микропенис. Из патологии внут¬ренних органов, в основном, отмечена патология сердечно-сосудис¬той системы, почек, комплексные порокижелудочно-кишечного трак¬та. Прогноз жизни неблагоприятный. Большинство больных погиба¬ют в первые 4 месяца жизни, особенно от респираторных инфекций.
Синдром Патау (трисомия по хромосоме 13). Впервые опи¬сан в 1960 году. Популяционная частота 1 на 7800. Цитогенетические варианты могут быть различны: целая трисомия 13 (нерасхождение хромосом в мейозе, в 80% случаев уматери), транслокационный ва¬риант (робертсоновские транслокации D/13 и G/13), мозаичные фор¬мы, дополнительная кольцевая хромосома 13, изохромосомы.
Для синдрома Патау характерны следующие диагностические при¬знаки: микроцефалия, расщелина верхней губы и неба, низко поса¬женные деформированные ушные раковины, микрогения, полидак-тилия, флексорное положение пальцев рук, выпуклые ногти, попе¬речная ладонная складка, стопа-качалка. Из пороков внутренних ор¬ганов отмечены врожденные пороки сердца (дефекты перегородок и крупных сосудов), незавершенный поворот кишечника, дивертикул Меккеля, поликистоз почек, удвоение мочеточника. Наблюдается крипторхизм, гипоплазия наружных половых органов, удвоениемат¬ки и влагалища. Глубокая идиотия. Дети, в основном, умирают в воз¬расте до 1 года, чаще в первые 2-3 месяца жизни.
Синдром трисомий хромосомы 14. Описан в 1975 году. Ос¬новными цитогенетическими формами являются мозаики. Кроме того, часто встречаются транслокационные варианты, включающие робертсоновские транслокации 14/14.
Основными диагностическими признаками синдрома являются: микроцефалия, асимметрия лица, высокий и выступающийлоб, нос короткий и бульбообразный, губы полные, высокое небо, часто с расщелинами, микроретрогнатия. Ушные раковины низко посажены, с маленькими мочками. Короткая шея, узкая и деформированная груд¬ная клетка, крипторхизм, гипогонадизм и маленький пенис. Из поро¬ков внутренних органов выражены пороки сердечно-сосудистой сис¬темы, смещение почки и почечная недостаточность, астма и дерма¬тозы. Прогноз жизни неблагоприятный, однако отмечены больные в возрасте 13,5 лет.
Синдром Эдвардса (трисомия по хромосоме 18). Описан в 1960 году. Популяционная частота составляет 1 на 6500. Цитогенетически в большинстве случаев представлен целой трисомиеи 18 (гаметическая мутация одного из родителей, чаще по материнской линии). Кроме того, встречаются и мозаичные формы, а транслокации наблюдаются очень редко. Критическим сегментом, ответственным за формирование основных признаков синдрома, является сег¬мент 18q11. Клинических различий между цитогенетическими фор¬мами не обнаружено.
Основными диагностическими признаками синдрома являются: типичное плоское лицо, монголоидный разрез глаз, эпикант, откры¬тый рот, макроглоссия и аномалии зубов, короткий нос и плоская пе-реносица, избыток кожи на шее, короткие конечности, поперечная четырех-пальцевая ладонная складка (обезьянья борозда). Из по¬роков внутренних органов часто отмечаются врожденные пороки сер¬дца и желудочно-кишечного тракта, которые и определяют продолжительность жизни больных. Умственная отсталость обычно сред¬ней степени тяжести. Дети с синдромом Дауна часто ласковые и при-вязчивые, послушные и внимательные.
Клинико-цитогенетическая характеристика синдромов, связанных с аномалиями половых хромосом
Синдром Шерешевского-Тернера (моносомия Х-хромосомы).
Это единственная форма моносомии у человека, которая может быть выявлена у живорожденных. Популяционная частота 1 на 3000 ново¬рожденных. Кроме простой моносомии по X хромосоме, составляю¬щей 50%, встречаются мозаичныеформы, делеции длинного и ко¬роткого плеча X хромосомы, изо-Х-хромосомы, а также кольцевые X хромосомы. Интересноотметить, что мозаицизм 45,X/46,XY состав¬ляет 2-5% от всех больных с этим синдромом и характеризуется широким диапазоном признаков: от типичного синдрома Шерешевс¬кого-Тернера до нормального мужского фенотипа Основными клиническими признаками заболевания являются: на¬низм, крыловидные кожные складки на шее, короткая шея с низкой линией роста волос, отеки кистей и стоп новорожденных, бочкооб¬разная грудная клетка, вальгусная девиация коленных и локтевых суставов. У больных выявляются первичная аменорея и половой ин¬фантилизм, бесплодие, гиперпигментациякожи, снижение зрения и слуха. Часто встречаются врожденные пороки сердца и почек. Ин¬теллектуальное развитие в пределах нормы.
Синдром Клайнфельтера. Описан в 1942 году. Популяционная частота 1 на 1000 мальчиков. Цитогенетические вариантысиндрома могут быть различны: 47.XXY; 48.XXYY; 48.XXXY; 49.XXXXY. Отме-чены как полные, так и мозаичные формы. Больные высокого роста с непропорционально длинными конечностями, выраженной гинеко¬мастией и оволосением поженскому типу. В детстве отличаются хруп¬ким телосложением, а после 40 лет страдают ожирением. Важными диагностическими признаками являются гипогонадизм и гипогенитализм. Характерно снижение полового влечения, импотенция и бес-плодие. Коэффициент интеллекта ниже 80.
Синдром полисомии Y-хромосомы. Популяционная частота 1 на 1000 мальчиков. Цитогенетически отмечены полные имозаичные формы. Большинство индивидов по физическому и умственному развитию не отличается от здоровых. Обычноони высокого роста и в 50% случаев могут иметь нормальное потомство. При данном синд¬роме имеются некоторые особенности поведения: склонность к аг¬рессии, асоциальному поведению, гомосексуализму.
Клинико-цитогенетическая характеристика синдромов, связанных со структурными перестройками хромосом
Синдром дупликации короткого плеча хромосомы 9 (синдром 9р+). Описан в 1970 году. Это наиболее частая формачастич¬ных трисомий у человека. Цитогенетика синдрома разнообразна: простые дупликации, изохромосомы 9р, несбалансированные транс¬локации, но во всех случаях имеется тройной набор генов части ко¬роткого плеча хромосомы 9. Диагностическими признаками заболе¬вания являются: микробрахицефалия, антимонголоидный разрез глаз, гипертелоризм, анофтальм, широкий и округлый кончик носа, выступающая верхняя губа и верхняя челюсть. Ушные раковины низко расположены с аномальным противозавитком и противокозелком, узкий слуховой канал. Кроме того имеется короткая шеяс низкой линией роста волос, поперечная ладонная складка, рентгенологи¬чески отмечается задержка костного возраста. Убольных обна¬руживают патологию почек. Олигофрения. Прогноз жизни благопри¬ятный, больные доживают до пожилого возраста 25%
Синдром трисомии длинного плеча 14-й хромосомы (синд¬ром 14q+). Описан в 1970 году. Цитогенетически проявляетсякак дупликация участка хромосомы 14, имеются транслокационные фор-мы и изохромосома 14 по длинному плечу. Типичными признаками заболевания являются: микроцефалия, луковицеобразный нос, тон¬кая верхняя губа, микростомия, опущенные углы рта, низкорасполо¬женные ротированные назад ушные раковины, короткая шея. Харак¬терно неправильное расположение пальцев на руке, клинодактилия, косолапость. Из внутренних пороков описана патология сердечно-¬сосудистой системы. Дети резко отстают в психомоторном и физи¬ческом развитии.
Синдром кольцевой хромосомы 18. Описан в 1962 году. Цито¬генетически представлен кольцевой хромосомой 18, возможны мо¬заичные варианты. Основные клинические признаки заболевания: микроцефалия, гипертелоризм, страбизм, птоз, нистагм, колобома радужной оболочки глаза, уплощенная спинка носа, рот «карпа», тон¬кая верхняя губа, высокое небо (часто с расщелиной). Патология внутренних органов встречается редко. Умственная отсталость как правило тяжелая ипроявляется у 100% больных.
Синдром моносомии короткого плеча 18 хромосомы (синд¬ром 18р-). Описан в 1963 году. Цитогенетически характеризуетсяде¬лециеи короткого плеча 18 хромосомы. Отмечается низкая масса тела при рождении. Основными диагностическими признаками синдрома являются: мышечная гипотония, умеренная микроцефалия, высокий лоб, гипертелоризм, эпикант, птоз, широкая уплощенная переноси¬ца, микрогения, широкий рот с опущенными уголками губ и выпячиванием верхней губы в виде «полицейской фуражки», аномалии зу¬бов, крупные деформированные ушные раковины. Часто встречают¬ся короткая шея, вдавленная грудная клетка, пупочная и паховая грыжы. Скелетные аномалии могут быть представленывывихом бед¬ра, деформацией локтевого сустава. Из пороков внутренних органов встречается ВПС. Выявляется также дефицит IgA. Все больные от¬стают в психомоторном развитии, во многих случаях отсутствует фразовая речь до 7-9 лет.
Синдром делеции длинного плеча 21 хромосомы (синдром 21 q-). Выделен в отдельную нозологическую группу в 1970 году. Ци¬тогенетически характеризуется частичной делециеи длинного плеча хромосомы 21, а также кольцевой хромосомой. Отмечены моза¬ичные формы этих хромосомных нарушений. Диагностическими при¬знаками заболевания являются: низкая масса тела при рождении, микроцефалия, антимонголоидный разрез глаз, эпикант, широкая переносица, большиенизко посаженные деформированные уши с расширенным слуховым каналом, микрогнатия. К основным призна¬камотносятся также сколиоз, клинодактилия, паховая грыжа, косо¬лапость и крипторхизм. Их пороков внутренних органов наблюдают¬ся пороки сердца и патология почек (гидронефроз, удвоение почеч¬ных лоханок). Отмечена задержка психомоторного развития. При грубых пороках развития дети умирают в первые недели жизни, хотя описаны больные в возрасте 50 лет.
Синдром кольцевой хромосомы 22. Выделен в самостоятель¬ный синдром в 1972 году. Цитогенетические варианты могутбыть раз¬личны: кольцевая хромосома 22, делеции длинного плеча этой хро¬мосомы и мозаичные варианты. В 90% случаев данные хромосом¬ные нарушения являются мутациями de novo. Основными диагнос¬тическими признаками заболеванияя вляются: микроцефалия, эпикант, гипертелоризм, крупные выступающие глаза («глаза лани»), расщелина язычка инеба, густые брови и ресницы. Кроме того, от¬мечается дисплазия тазобедренных суставов, клинодактилия и син-дактилия. Пороки внутренних органов не характерны. Умственная от¬сталость проявляется как легкой, так и выраженной олигофренией. Больные легко возбудимы, отмечается частая смена настроения, на-рушение координации, а также грубое недоразвитие речи, вплоть до ее отсутствия.
Клинико-цитогенетическая характеристика синдромов и злокачественных новообразований, вязанных с микроструктурными аномалиями хромосом
В последнее время клинико-цитогенетические исследования ста¬ли опираться на высокоразрешающие методыхромосомного анали¬за, позволившее подтвердить предположение о существовании мик-рохромосомных мутаций, выявление которых находится на грани воз¬можностей светового микроскопа. Используя стандартные цитогенетические методы можно достичь визуального разрешения хромосом с числом сегментов не более 400, а применение методов прометафазного анализа, предложенного Юнисом в 1976 году, удается полу¬чать хромосомы с числом сегментов до 550-850. Незначительные нарушения в структуре хромосом могут быть выявлены с помощью этихметодов хромосомного анализа не только среди больных с МВПР, но и при некоторых неизвестных менделирующих синдромах. Отли-чительная черта этих синдромов состоит в том, что клинически они были описаны задолго до того, как была выявлена их хромосомная этиология. Нет никаких сомнений в том, что еще некоторые синдро¬мы, рассматриваемые пока в группе синдромов с неясной этиологи¬ей, могут оказаться хромосомными. На сегодняшний день выяснена этиология около 20 нозологических форм, при которых выявлены мик-роструктурные хромосомные нарушения. Показано, что микрострук¬турные аномалии хромосом сопровождают не только синдромы МВПР, но и различные гиперпластические процессы, включая и зло-качественные образования. Большинство синдромов, связанных с микроаномалиями хромосом, встречается редко-1 случай на 50000-100000 новорожденных).
Синдром Лангера-Гидиона (трихо-рино-фалангиальный синдром). Особый интерес к этому синдрому проявился в 1980 году, когда была выяснена его хромосомная этиология, выражающаяся в микроделеции хромосомы длинного плеча хромосомы 8. Отмечены мозаичные формы синдрома.
Основными клиническими признаками заболевания являются: тонкие и редкие волосы, бульбообразныйнос, конические эпифизы фаланг пальцев, множественные хрящевые экзостозы. Кроме этих признаков больные имеют ряд микроаномалий: широкие редкие бро¬ви, глубоко посаженые глаза, макростомию, нарушение прорезыва¬ния и расположения зубов, микрогнатию, большие и низко располо¬женные ушные раковины. Множественные хрящевые экзостозы проявляются до 4-х лет и располагаются везде, где есть хрящи, причем их рост усиливается в периоды активного роста организма и прекра¬щается в возрасте 18-20 лет. У новорожденных бывает избыточная кожа. Отмечается умственная отсталость различной степени, задер¬жка речевого развития.
Синдром Видемана-Беквита. Цитогенетически характеризует¬ дупликацией участка короткого плеча 11 хромосомы-11р15. Основными диагностическими признаками заболевания являются: макроглоссия, макросомия с увеличением мышечной массы и подкожного жирового слоя, выступающий затылок и аномалии прикуса, связанные с гипоплазией верхней челюсти и относительной гиперплазией верхней. Характерным признаком является нали¬чие вертикальных бороздок на мочках ушей. Описана патология раз¬вития внутренних органов: дефекты межжелудочковых перегородок, добавочная селезенка, цитомегалия коры надпочечников, незавершенный поворот кишечника. Костный возраст опережает паспортный.
Психическое развитие соответствует возрасту, возможна умеренная умственная отсталость. В сегменте 11 р15 локализован ген «инсулиноподобного фактора роста II типа», при дупликации которого обра-зуются три его копии, что приводит к появлению таких признаков син¬дрома как большой вес, пупочная грыжа, увеличенный язык и т.д.
Синдром Прадера-Вилли. Описан в 1956 году. Популяционная частота 1 на 15 000. Встречается в основномспорадически, хотя описаны и семейные случаи с аутосомно-доминантным типом наследования. Основные диагностические признаки заболевания: слабое шевеление плода во II триместре беременности, мышечная гипотония, умственная отсталость, нанизм, ожирение, гипогонадотропный гипогонадизм, маленькие дистальные отделы конечностей (акромикрия).
Отмечаются также гипопигментация, страбизм, микрогнатия, доли¬хоцефалия, миндалевидный разрез глаз, крипторхизм игипоплазия полового члена у мальчиков.
Синдром Энгельмана (синдром «счастливой куклы»). Опи¬сан в 1965 году. Основными признаками заболевания являются: нео¬бычный и частый смех, специфичное лицо с гримасой улыбки, повторяющиеся кукольные стереотипные движения, отсутствие речи. Имеется выраженная умственная отсталость. Большинство больных имеют микроделецию 15q11-q13, но эта делеция всегда материнско¬го происхождения. Обнаружены также пациенты с типичным синдро¬мом Энгельмана безмикроделеции, у которых выявляется одноро¬дительская дисомия хромосомы 15 отцовскою происхождения.
Моногенные заболевания, проявляющиеся хромосомной нестабильностью
Остановка развития зародыша
В основу статьи положены работы проф. Буэ.
Остановка развития зародыша в дальнейшем приводит к изгнанию плодного яйца, что проявляется в виде самопроизвольного выкидыша. Однако во многих случаях остановка развития происходит на очень ранних сроках и сам факт зачатия остается неизвестным для женщины. В большом проценте случаев такие выкидыши связаны с хромосомными аномалиями у зародыша.
Самопроизвольные выкидыши
Самопроизвольные выкидыши, определением которых служит «самопроизвольное прерывание беременности между сроком зачатия и сроком жизнеспособности плода», во многих случаях с большим трудом поддаются диагностике: большое число выкидышей происходит на очень ранних сроках: задержки месячных не происходит, или эта задержка настолько мала, что сама женщина не подозревает о беременности.
Клинические данные
Изгнание плодного яйца может произойти внезапно, или ему могут предшествовать клинические симптомы. Чаще всего угроза выкидыша проявляется кровянистыми выделениями и болями внизу живота, переходящими в схватки. Далее следуют изгнание плодного яйца и исчезновение признаков беременности.
Клиническое обследование может выявить несоответсвие между предполагаемым сроком беременности и размерами матки. Уровни гормонов в крови и моче могут быть резко снижены, указывая на отсутствие жизнеспособности зародыша. Ультразвуковое исследование позволяет уточнить диагноз, выявляя либо отсутствие зародыша («пустое плодное яйцо»), либо отставание в развитии и отсутствие сердцебиения
Клинические проявления самопроизвольного выкидыша значительно варьируют. В одних случаях выкидыш проходит незамеченным, в других — сопровождается кровотечением и может потребовать выскабливания полости матки. Хронология симптоматики может косвенно указывать на причину самопроизвольного выкидыша: кровянистые выделения с ранних сроков беременности, остановка роста матки, исчезновение признаков беременности, «немой» период в течение 4-5 недель, а затем изгнание плодного яйца чаще всего свидетельствуют о хромосомных нарушениях зародыша, а соответствие срока развития зародыша сроку выкидыша говорит в пользу материнских причин невынашивания беременности.
Анатомические данные
Анализ материала самопроизвольных выкидышей, сбор которого был начат в начале двадцатого века в Институте Карнеги, позволил выявить огромный процент аномалий развития среди абортусов ранних сроков
В 1943 году Хертиг и Шелдон опубликовали результаты патологоанатомического исследования материала 1000 выкидышей на ранних сроках. Материнские причины невынашивания беременности были ими исключены в 617 случаев. Современные данные указывают на то, что мацерированные зародыши во внешне нормальных оболочках тоже могут быть связаны с хромосомными аномалиями, что в сумме составляет около 3/4 всех случаев данного исследования.
| Морфологическое исследование 1000 абортусов (по Hertig и Sheldon, 1943) | ||
| Грубые патологические нарушения плодного яйца: плодное яйцо без зародыша или с недифференцированным зародышем | 489 | |
| Локальные аномалии зародышей | 32 | |
| Аномалии плаценты | 96 | 617 |
| Плодное яйцо без грубых аномалий | ||
| с мацерированными зародышами | 146 | |
| 763 | ||
| с немацерированными зародышами | 74 | |
| Аномалии матки | 64 | |
| Другие нарушения | 99 | |
Дальнейшие исследования Микамо и Миллера и Полланда позволили уточнить связь между сроком выкидыша и частотой нарушений развития зародыша. Оказалось, что чем меньше срок выкидыша, тем частота аномалий выше. В материалах выкидышей, происшедших до 5-й недели после зачатия макроскопические морфологические аномалии плодного яйца встречаются в 90% случаев, при сроке выкидыша от 5 до 7 недель после зачатия — в 60%, при сроке больше 7 недель после зачатия — менее, чем в 15—20%.
Важность значения остановки развития зародыша в ранних самопроизвольных выкидышах была показана прежде всего фундаментальными исследованиями Артура Хертига, который в 1959 г. опубликовал результаты исследования человеческих зародышей до 17 дней после зачатия. Это был плод его 25-летней работы.
У 210 женщин в возрасте до 40 лет, идущих на операцию гистерэктомии (удаления матки) дата операции была сопоставлена с датой овуляции (возможного зачатия). После операции матки подвергались самому тщательному гистологическому исследованию на предмет выявления возможной беременности малого срока. Из 210 женщин только 107 были оставлены в исследовании в связи с обнаружением признаков овуляции, и отсутствием грубых нарушений труб и яичников, препятствующих наступлению беременности. Было обнаружено 34 плодных яйца, из них 21 плодное яйцо было внешне нормальным, а 13 (38%) имело явные признаки аномалий, которые, по мнению Хертига, обязательно привели бы к выкидышу или на этапе имплантации или вскоре после имплантации. Поскольку в то время не было возможности проведения генетического исследования плодных яиц, причины нарушений развития зародышей оставались неизвестными.
При обследовании женщин с подтвержденной фертильностью (все пациентки имели по несколько детей) было обнаружено, что одно из трех плодных яиц имеет аномалии и подвергается выкидышу до появления признаков беременности.
Эпидемиологические и демографические данные
Нечеткая клиническая симптоматика ранних самопроизвольных выкидышей приводит к тому, что достаточно большой процент выкидышей на малых сроках проходит незамеченным женщинами.
В случае клинически подтвержденных беременностей около 15% всех беременностей заканчивается выкидышем. Большая часть самопроизвольных выкидышей (около 80%) происходит в первом триместре беременности. Однако если принять во внимание тот факт, что выкидыши часто случаются спустя 4-6 недель после остановки развития беременности, можно сказать, что с первым триместром связано более 90% всех самопроизвольных выкидышей.
Специальные демографические исследования позволили уточнить частоту внутриутробной смертности. Так, Френч и Бирман в 1953 — 1956 гг. регистрировали все беременности у женщин острова Канаи и показали, что из 1000 беременностей, диагностированных при сроке после 5 недель, 237 не увенчались рождением жизнеспособного ребенка.
Анализ результатов нескольких исследований позволил Леридону составить таблицу внутриутробной смертности, включающей в себя и неудачи оплодотворения (половой акт в оптимальные сроки — в течение суток после овуляции).
| Полная таблица внутри утробной смертности (на 1000 яйцеклеток, подвергшихся риску оплодотворения) (по Leridon, 1973) | ||
|---|---|---|
| Недели после зачатия | Остановка развития с последующим изгнанием | Процент продолжающихся беременностей |
| 16* | 100 | |
| 0 | 15 | 84 |
| 1 | 27 | 69 |
| 2 | 5,0 | 42 |
| 6 | 2,9 | 37 |
| 10 | 1,7 | 34,1 |
| 14 | 0,5 | 32,4 |
| 18 | 0,3 | 31,9 |
| 22 | 0,1 | 31,6 |
| 26 | 0,1 | 31,5 |
| 30 | 0,1 | 31,4 |
| 34 | 0,1 | 31,3 |
| 38 | 0,2 | 31,2 |
| * — неудачи зачатия | ||
Все эти данные указывают на огромную частоту самопроизвольных выкидышей и на важную роль нарушений развития плодного яйца в этой патологии.
Эти данные отражают общую частоту нарушений развития, не выделяя среди них конкретные экзо- и эндогенные факторы (иммунологические, инфекционные, физические, химические и т. д.).
Важно отметить, что независимо от причины повреждающего воздействия, при исследовании материала выкидышей обнаруживается очень большая частота генетический нарушений (хромосомных аберраций (на сегодня изучены лучше всего) и генных мутаций) и аномалий развития, как, например, дефекты развития нервной трубки.
Хромосомные аномалии, ответственные за остановку развития беременности
Цитогенетические исследования материала выкидышей позволили уточнить характер и частоту тех или иных хромосомных аномалий.
Общая частота
При оценке результатов больших серий анализов следует иметь в виду следующее. На результаты исследований подобного рода могут оказать значительное влияние следующие факторы: способ сбора материала, относительная частота более ранних и более поздних выкидышей, доля материала искусственных абортов в исследовании, часто не поддающаяся точной оценке, успех культивирования клеточных культур абортуса и хромосомного анализа материала, тонкие методы обработки мацерированного материала.
Общая оценка частоты хромосомных аберраций при невынашивании беременности составляет около 60%, а в первом триместре беременности — от 80 до 90%. Как будет показано ниже, анализ, основанный на стадийности развития зародыша, позволяет сделать гораздо более точные выводы.
Относительная частота
Практически все большие исследования хромосомных аберраций в материале выкидышей дали поразительно сходные результаты относительно характера нарушений. Количественные аномалии составляют 95% всех аберраций и распределяются следующим образом:
| трисомии | 50—55% |
| моносомии X | 15—20% |
| триплоидии | 15—20% |
| тетраплоидии | 5% |
Количественные хромосомные аномалии
Различные типы количественных хромосомных аберраций могут возникать в результате:
Моносомии
Моносомия X (45,X) представляет одну из часто встречающихся аномалий в материале самопроизвольных выкидышей. При рождении она соответствует синдрому Шерешевского-Тернера, и при рождении она встречается реже, чем другие количественные аномалии половых хромосом. Эта бросающаяся в глаза разница между относительно высокой частотой обнаружения лишних X-хромосом у новорожденных и относительно редким обнаружением моносомии X у новорожденных указывает на высокую частоту летальности моносомии X у зародыша. Кроме того, обращает на себя внимание очень большая частота мозаик у больных с синдромом Шерешевского-Тернера. В материале выкидышей, наоборот, мозаики с моносомией X крайне редки. Данные исследований показали, что только менее 1% всех моносомий X доходит до срока родов. Моносомии аутосом в материале выкидышей встречаются довольно редко. Это очень контрастирует с высокой частотой соответствующих трисомий.
Трисомии
В материале выкидышей трисомии представляют более половины всех количественных хромосомных аберраций. Обращает на себя внимание то, что в случаях моносомий недостающей хромосомой обычно оказывается X-хромосома, а в случаях избыточных хромосом, дополнительная хромосома чаще всего оказывается аутосомой.
Точная идентификация дополнительной хромосомы стала возможна благодаря методу G-бэндинга. Исследования показали, что все аутосомы могут принимать участие в нон-дисджанкшн (см. таблицу). Обращает на себя внимание, что три хромосомы, чаще всего встречающиеся при трисомиях новорожденных (15-я, 18-я и 21-я) чаще всего обнаруживаются и при летальных трисомиях у зародышей. Вариации относительных частот различных трисомий у зародышей отражают во многом сроки, на которых происходит гибель зародышей, поскольку, чем более летальной является комбинация хромосом, тем на более ранних сроках происходит остановка развития, тем реже будет обнаруживаться такая аберрация в материалах выкидышей (чем меньше срок остановки развития, тем труднее обнаружить такой зародыш).
| Лишняя хромосома при летальных трисомиях у зародыша (данные 7 исследований: Буэ (Франция), Карр (Канада), Кризи (Великобритания), Дилл (Канада), Кадзи (Швейцария), Такахара (Япония), Теркелсен (Дания)) | |||
|---|---|---|---|
| Дополнительная аутосома | Количество наблюдений | ||
| A | 1 | ||
| 2 | 15 | ||
| 3 | 5 | ||
| B | 4 | 7 | |
| 5 | |||
| C | 6 | 1 | |
| 7 | 19 | ||
| 8 | 17 | ||
| 9 | 15 | ||
| 10 | 11 | ||
| 11 | 1 | ||
| 12 | 3 | ||
| D | 13 | 15 | |
| 14 | 36 | ||
| 15 | 35 | ||
| E | 16 | 128 | |
| 17 | 1 | ||
| 18 | 24 | ||
| F | 19 | 1 | |
| 20 | 5 | ||
| G | 21 | 38 | |
| 22 | 47 | ||
Триплоидии
Крайне редко наблюдаемые при мертворождениях, триплоидии составляют пятую по частоте хромосомную аномалию в материале выкидыше. В зависимости от соотношения половых хромосом может быть 3 варианта триплоидий: 69XYY (самая редкая), 69, XXX и 69, XXY (самая частая). Анализ полового хроматина показывает, что при конфигурации 69, XXX чаще всего обнаруживается только одна глыбка хроматина, а при конфигурации 69, XXY чаще всего половой хроматин не обнаруживается.
Приведенный ниже рисунок иллюстрирует различные механизмы, приводящие к развитию триплоидии (диандрию, дигинию, диспермию). С помощью специальных методов (хромосомные маркеры, антигены тканевой совместимости) удалось установить относительную роль каждого из этих механизмов в развитии триплоидии у зародыша. Оказалось, что на 50 случаев наблюдений триплоидия была следствием дигинии в 11 случаях (22%), диандрии либо диспермии — в 20 случаях (40%), диспермии — в 18 случаях (36%).
| Механизмы образования триплоидной зиготы |
|---|
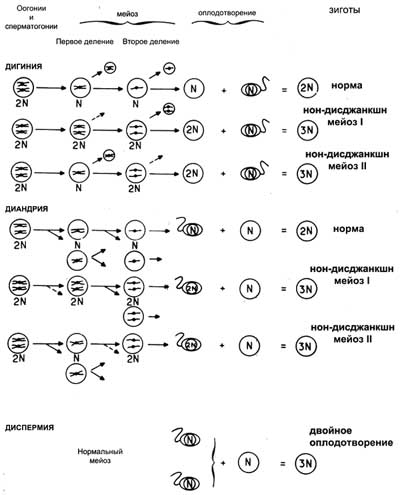 |
Тетраплоидии
Тетраплоидии встречаются примерно в 5% случаев количественных хромосомных аберраций. Чаще всего встречаются тетраплоидии 92, XXXX. Такие клетки всегда содержат 2 глыбки полового хроматина. В клетках с тетраплоидией 92, XXYY никогда не бывает видно полового хроматина, но в них обнаруживают 2 флуоресцирующие Y-хромосомы.
Двойные аберрации
Большая частота хромосомных аномалий в материале выкидышей объясняет высокую частоту комбинированных аномалий в одном и том же зародыше. Напротив, у новорожденных комбинированные аномалии крайне редки. Обычно в таких случаях наблюдаются комбинации аномалии половой хромосомы и аномалии аутосомы.
В связи с более высокой частотой аутосомных трисомий в материале выкидышей, при комбинированных хромосомных аномалиях у абортусов чаще всего встречаются двойные аутосомные трисомии. Трудно сказать, связаны ли такие трисомии с двойным «нон-дисджанкшн» в одной и той же гамете, или со встречей двух аномальных гамет.
Частота сочетаний различных трисомий в одной и той же зиготе носит случайный характер, что позволяет предположить независимость друг от друга появления двойных трисомий.
Комбинация двух механизмов, приводящих к появлению двойных аномалий, позволяет объяснить появление других аномалий кариотипа, встречающихся при выкидышах. «Нон-дисджанкшн» при образовании одной из гамет в сочетании с механизмами образования полиплоидии объясняет появление зигот с 68 или 70 хромосомами. Сбой первого митотического деления у такой зиготы с трисомией может приводить к таким кариотипам, как 94,XXXX,16+,16+.
Структурные хромосомные аномалии
Согласно классическим исследованиям, частота структурных хромосомных аберраций в материале выкидышей составляет 4—5%. Однако многие исследования были сделаны до широкого использования метода G-бэндинга. Современные исследования указывают на более высокую частоту структурных хромосомных аномалий у абортусов. Обнаруживаются самые разные виды структурных аномалий. Примерно в половине случаев эти аномалии являются унаследованными от родителей, примерно в половине случаев они возникают de novo.
Влияние хромосомных аномалий на развитие зиготы
Хромосомные аномалии зиготы проявляются как правило уже в первые недели развития. Выяснение конкретных проявлений каждой аномалии сопряжено с целым рядом трудностей.
Во многих случаях установление срока беременности при анализе материала выкидышей крайне затруднено. Обычно сроком зачатия считается 14-й день цикла, но у женщин с невынашиванием беременности часто бывают задержки цикла. Кроме того, очень трудно бывает установить дату «смерти» плодного яйца, поскольку от момента гибели до выкидыша может пройти много времени. В случыае триплоидии этот период может составить 10—15 недель. Применение гормональных препаратов может еще более удлиннить это время.
С учетом этих оговорок, можно сказать, что чем меньше срок беременности на момент гибели плодного яйца, тем выше частота хромосомных аберраций. Согласно исследованиям Кризи и Лоритсена, при выкидышах до 15 недель беременности частота хромосомных аберраций составляет около 50%, при сроке 18 — 21 неделя — около 15%, при сроке более 21 недели — около 5—8%, что примерно соответствует частоте хромосомных аберраций в исследованиях перинатальной смертности.
Фенотипические проявления некоторых летальных хромосомных аберраций
Моносомии X обычно останавливаются в развитии к 6 неделям после зачатия. В двух третях случаев плодный пузырь размером 5—8 см не содержит зародыша, но существует шнурообразное образование с элементами эмбриональной ткани, остатками желточного мешка, плацента содержит субамниотические тромбы. В одной трети случаев плацента имеет такие же изменения, но обнаруживается морфологически неизмененный зародыш, погибший в возрасте 40—45 дней после зачатия.
При тетраплоидиях развитие останавливается к сроку 2-3 недели после зачатия, морфологически эта аномалия характеризуется «пустым плодным мешком».
При трисомиях наблюдаются различные типы аномалий развития, в зависимости от того, какая хромосома является лишней. Однако в подавляющем большинстве случаев развитие останавливается на очень ранних сроках, элементов зародыша не обнаруживается. Это классический случай «пустого плодного яйца» (анэмбрионии).
Трисомия 16, очень частая аномалия, характеризуется наличием маленького плодного яйца диаметром около 2,5 см, в полости хориона находится небольшой амниотический пузырек около 5 мм в диаметре и эмбриональный зачаток размером 1—2 мм. Чаще всего развитие останавливается на стадии эмбрионального диска.
При некоторых трисомиях, например, при трисомиях 13 и 14, возможно развитие зародыша до срока около 6 недель. Зародыши характеризуются циклоцефалической формой головы с дефектами закрытия верхнечелюстных холмиков. Плаценты гипопластичны.
Зародыши с трисомиями 21 (синдром Дауна у новорожденных) не всегда имеют аномалии развития, а если и имеют, то незначительные, не могущие служить причиной их гибели. Плаценты в таких случаев бывают бедны клетками, и представляются остановившимися в развитии на ранней стадии. Гибель зародыша в таких случаях представляется следствием плацентарной недостаточности.
Заносы. Сравнительный анализ цитогенетических и морфологических данных позволяет выделить два типа заносов: классический пузырный занос и эмбриональный триплоидный занос.
Выкидыши при триплоидиях имеют четкую морфологическую картину. Это выражается в сочетании полной или (чаще) частичной пузырной дегенерации плаценты и амниотического пузырька с зародышем, размеры которого (зародыша) очень малы по сравнению с относительно большим амниотическим пузырьком. Гистологическое исследование показывает не гипертрофию, а гипотрофию пузырно измененного трофобласта, образующего микрокисты в результате многочисленный инвагинаций.
Напротив, классический пузырный занос не затрагивает ни амниотический мешок, ни зародыш. В пузырьках обнаруживается избыточное образование синцитиотрофобласта с выраженной васкуляризацией. Цитогенетически большинство классических пузырных заносов имеет кариотип 46,XX. Проведенные исследования позволили установить хромосомные сбои, участвующие в образовании пузырного заноса. Было показано, что 2 X-хромосомы в классическом пузырном заносе идентичны и имеют отцовское происхождение. Наиболее вероятным механизмом развития пузырного заноса является истинный андрогенез, возникающий вследствие оплодотворения яйцеклетки диплоидным сперматозоидом, возникшим в результате сбоя второго мейотического деления и последующим полным выключением хромосомного материала яйцеклетки. С точки зрения патогенеза, такие хромосомные нарушения близки к нарушениям при триплоидии.
Оценка частоты хромосомных нарушений в момент зачатия
Можно попробовать расчитать количество зигот с хромосомными аномалиями при зачатии, основываясь на частоте хромосомных аномалий, обнаруживаемых в материале выкидышей. Однако прежде всего следует отметить, что поразительное сходство результатов исследований материала выкидышей, проведенное в разных частях света, говорит о том, что хромосомные сбои в момент зачатия являются очень характерным явлением в репродукции у человека. Кроме того, можно констатировать, что реже всего встречающиеся аномалии (например, трисомии A, B и F) связаны с остановкой развития на очень ранних стадиях.
Анализ относительной частоты различных аномалий, возникающих при нерасхождении хромосом в процессе мейоза, позволяет сделать следующие важные выводы:
1. Единственной моносомией, обнаруживаемой в материале выкидышей, является моносомия X (15% всех аберраций). Напротив, аутосомные моносомии практически не обнаруживаются в материале выкидышей, хотя теоретически их должно быть столько же, сколько и аутосомных трисомий.
2. В группе аутосомных трисомий частота трисомий разных хромосом значительно варьирует. Исследования, выполненные с использованием метода G-бэндинга, позволили установить, что все хромосомы могут быть участницами трисомии, однако некоторые трисомии встречаются гораздо чаще, например, трисомия 16 встречается в 15% случаев всех трисомий.
Из этих наблюдений можно сделать вывод, что, скорее всего, частота нерасхождения разных хромосом приблизительно одинакова, а различная частота аномалий в материале выкидышей связана с тем, что отдельные хромосомные аберрации приводят к остановке развития на очень ранних стадиях и поэтому с трудом поддаются обнаружению.
Эти соображения позволяют приблизительно расчитать реальную частоту хромосомных нарушений в момент зачатия. Расчеты, сделанные Буэ, показали, что каждое второе зачатие дает зиготу с хромосомными аберрациями.
Данные цифры отражают среднюю частоту хромосомных аберраций при зачатии в популяции. Однако данные цифры могут значительно колебаться у разных супружеских пар. У некоторых супружеских пар вероятность возникновения хромосомных аберраций в момент зачатия значительно превышает средний риск в популяции. У таких супружеских пар невынашивание беременности на малых сроках происходит гораздо чаще, чем у остальных супружеских пар.
Данные расчеты подтверждаются другими исследованиями, проведенными с использованием других методов:
1. Классическими исследованиями Хертига
2. Определением уровня хорионического гормона (ХГ) в крови женщин после 10 после зачатия. Часто этот тест оказывается положительным, хотя менструация приходит вовремя или с небольшой задержкой, и субъективно наступления беременности женщина не замечает («биохимическая беременность»)
3. Хромосомный анализ материала, полученного при искусственных абортах показал, что при абортах на сроке 6—9 недель (4—7 недель после зачатия) частота хромосомных аберраций составляет примерно 8%, а при искусственных абортах на сроке 5 недель (3 недели после зачатия) эта частота возрастает до 25%.
4. Было показано, что нерасхождение хромосом в процессе сперматогенеза является очень частым явлением. Так Пирсон и сотр. обнаружили, что вероятность нерасхождения в процессе сперматогенеза для 1-й хромосомы составляет 3,5%, для 9-й хромосомы — 5%, для Y-хромосомы — 2%. Если и другие хромосомы имеют вероятность нерасхождения примерно такого же порядка, то тогда только 40% всех сперматозоидов имеют нормальный хромосомный набор.
Экспериментальные модели и сравнительная патология
Частота остановки развития
Хотя различия в типе плацентации и количестве плодов затрудняют сравнение риска неразвивающейся беременности у домашних животных и у человека, определенные аналогии проследить можно. У домашних животных процент летальных зачатий колеблется между 20 и 60%.
Изучение летальных мутаций у приматов дало цифры, сравнимые с таковыми у человека. Из 23 бластоцист, выделенных у макак до зачатия, у 10 были грубые морфологические аномалии.
Частота хромосомных аномалий
Только экспериментальные исследования позволяют провести хромосомный анализ зигот на разных стадиях развития и оценить частоту хромосомных аберраций. Классические исследования Форда выявили хромосомные аберрации у 2% зародышей мышей в возрасте от 8 до 11 дней после зачатия. Дальнейшие исследования показали, что это слишком продвинутая стадия развития зародышей, и что частота хромосомных аберраций гораздо выше (см. ниже).
Влияние хромосомных аберраций на развитие
Большой вклад в дело выяснения масштаба проблемы внесли исследования Альфреда Гроппа из Любека и Чарльза Форда из Оксфорда, проводившиеся на так называемых «табачных мышах» (Mus poschiavinus). Скрещивание подобных мышей с нормальными мышами дает большой спектр триплоидий и моносомий, позволяющих оценить влияние обоих типов аберраций на развитие.
Данные профессора Гроппа (1973 г.) приведены в таблице.
| Распределение эуплоидных и анэуплоидных зародышей у гибридных мышей | |||||
|---|---|---|---|---|---|
| Стадия развития | День | Кариотип | Всего | ||
| Моносомии | Эуплоидии | Трисомии | |||
| До имплантации | 4 | 55 | 74 | 45 | 174 |
| После имплантации | 7 | 3 | 81 | 44 | 128 |
| 9—15 | 3 | 239 | 94 | 336 | |
| 19 | 56 | 2 | 58 | ||
| Живые мыши | 58 | 58 | |||
Эти исследования позволили подтвердить гипотезу о равной вероятности возникновения моносомий и трисомий при зачатии: аутосомные моносомии возникают с такой же частотой, как и трисомии, но зиготы с аутосомными моносомиями погибают еще до имплантации и не обнаруживаются в материале выкидышей.
При трисомиях гибель зародышей происходит на более поздних сдадиях, но ни один зародыш при аутосомных трисомиях у мышей не доживает до родов.
Исследования группы Гроппа позволили показать, что в зависимости от типа трисомии, зародыши погибают на разных сроках: с трисомиями 8, 11, 15, 17 — до 12 дня после зачатия, с трисомиями 19 — ближе к сроку родов.
Патогенез остановки развития при хромосомных аномалиях
Исследование материала выкидышей показывает, что во многих случаях хромосомных аберраций эмбриогенез резко нарушается, так что элементов эмбриона не обнаруживается вообще («пустые плодные яйца», анэмбриония) (остановка развития до срока 2-3 недель после зачатия). В других случаях удается обнаружить элементы зародыша, часто неоформленные (остановка развития на сроке до 3-4 недель после зачатия). При наличии хромосомных аберраций эмбриогенез часто или вообще невозможен, или резко нарушается с самых ранних стадий развития. Проявления таких нарушений выражены в гораздо большей степени в случае аутосомных моносомий, когда развитие зиготы останавливается в первые дни после зачатия, но и в случае трисомий хромосом, имеющих ключевое значение для эмбриогенеза, развитие также прекращается в первые дни после зачатия. Так, например, трисомия 17 обнаруживается только у зигот, остановившихся в развитии на самых ранних стадиях. Кроме того, многие хромосомные аномалии связаны вообще с пониженной способностью к делению клеток, как показывает изучение культур таких клеток in vitro.
В других случаях развитие может продолжаться до 5—6—7 недель после зачатия, в редких случаях — дольше. Как показали исследования Филиппа, в таких случаях гибель плода объясняется не нарушением эмбрионального развития (обнаруживаемые дефекты сами по себе не могут быть причиной смерти зародыша), а нарушением формирования и функционирования плаценты (стадия развития плода опережает стадию формирования плаценты.
Исследования культур клеток плаценты при различных хромосомных аномалиях показали, что в большинстве случаев деление плацентарных клеток происходит гораздо медленнее, чем при нормальном кариотипе. Это во многом объясняет, почему новорожденные с хромосомными аномалиями обычно имеют низкую массу тела и сниженную массу плаценты.
Можно предположить, что многие нарушения развития при хромосомных аберрациях связаны именно с пониженной способностью клеток к делению. При этом возникает резкая диссинхронизация процессов развития зародыша, развития плаценты и индукции дифференциации и миграции клеток.
Недостаточное и запоздалое формирование плаценты может приводить к нарушению питания и к гипоксии зародыша, а также — к снижению гормональной продукции плаценты, что может быть дополнительной причиной развития выкидышей.
Исследования клеточных линий при трисомиях 13, 18 и 21 у новорожденных показало, что клетки делятся медленнее, чем при нормальном кариотипе, что проявляется в снижении плотности клеток в большинстве органов.
Загадкой является то, почему при единственной аутосомной трисомии, совместимой с жизнью (трисомия 21, синдром Дауна), в одних случаях происходит задержка развития зародыша на ранних стадиях и самопроизвольный выкидыш, а в других — ненарушенное развитие беременности и рождение жизнеспособного ребенка. Сравнение клеточных культур материала выкидышей и доношенных новорожденных при трисомии 21 показало, что различия в способности клеток к делению в первом и втором случаях резко различается, что возможно объясняет разную судьбу таких зигот.
Причины количественных хромосомных аберраций
Изучение причин хромосомных аберраций крайне затруднено, прежде всего из-за высокой частоты, можно сказать, всеобщности этого явления. Очень трудно корректно собрать контрольную группу беременных женщин, с большим трудом поддаются изучению нарушения сперматогенеза и оогенеза. Несмотря на это, некоторые этиологические факторы повышения риска хромосомных аберраций выяснить удалось.
Факторы, напрямую связанные с родителями
Влияние возраста матери на вероятность рождения ребенка с трисомией 21 наводит на мысль о возможном влиянии возраста матери на вероятность возникновения летальных хромосомных аберраций у зародыша. Приводимая ниже таблица показывает связь возраста матери с кариотипом материала выкидышей.
| Средний возраст матери при хромосомных аберрациях абортусов | ||
|---|---|---|
| Кариотип | Число наблюдений | Средний возраст |
| Нормальный | 509 | 27,5 |
| Моносомия X | 134 | 27,6 |
| Триплоидии | 167 | 27,4 |
| Тетраплоидия | 53 | 26,8 |
| Аутосомные трисомии | 448 | 31,3 |
| Трисомии D | 92 | 32,5 |
| Трисомии E | 157 | 29,6 |
| Трисомии G | 78 | 33,2 |
Как видно из таблицы, не было обнаружено связи между возрастом матери и самопроизвольными выкидышами, связанными с моносомией X, триплоидией или тетраплоидией. Повышение среднего возраста матери отмечено для аутосомных трисомий в целом, но по разным группам хромосом цифры были получены разные. Однако общее число наблюдений в группах недостаточно, чтобы уверенно судить о каких-либо закономерностях.
Возраст матери в большей степени связан с повышенным риском выкидышей с трисомиями акроцентрических хромосом группы D (13, 14, 15) и G (21, 22), что совпадает и со статистикой хромосомных аберраций при мертворождениях.
Для некоторых случаев трисомий (16, 21) было определено происхождение лишней хромосомы. Оказалось, что возраст матери связан с повышением риска трисомий только в случае материнского происхождения лишней хромосомы. Не было обнаружено связи возраста отца с повышением риска трисомий.
В свете исследований на животных высказываются предположения о возможной связи старения гамет и задержки оплодотворения на риск возникновения хромосомных аберраций. Под старением гамет понимают старение сперматозоидов в половых путях женщины, старение яйцеклетки либо в результате перезрелости внутри фолликула или в результате задержки выхода яйцеклетки из фолликула, либо в результате трубной перезрелости (запоздалого оплодотворения в трубе). Скорее всего, подобные законы действуют и у человека, но достоверных подтверждений этого пока не получено.
Факторы окружающей среды
Было показано, что вероятность хромосомных аберраций при зачатии повышается у женщин, подвергшихся действию ионизирующей радиации. Предполагается связь между риском хромосомных аберраций и действием других факторов, в частности — химических.
Заключение
1. Не каждую беременность удается сохранить на малых сроках. В большом проценте случаев выкидыши обусловлены хромосомными нарушениями у плода, и родить живого ребенка невозможно. Гормональное лечение может отсрочить момент выкидыша, но не может помочь зародышу выжить.
2. Повышенная нестабильность генома супругов является одним из причинных факторов бесплодия и невынашивания беременности. Выявить такие супружеские пары помогает цитогенетическое обследование с анализом на хромосомные аберрации. В некоторых случаях повышенной нестабильности генома специальная антимутагенная терапия может помочь повысить вероятность зачатия здорового ребенка. В других случаях рекомендуется донорская инсеминация или использование донорской яйцеклетки.
3. При невынашивании беременности, обусловленном хромосомными факторами, организм женщины может «запомнить» неблагоприятный иммунологический ответ на плодное яйцо (иммунологический импринтинг). В таких случаях возможно развитие реакции отторжения и на зародыши, зачатые после донорской инсеминации или с использованием донорской яйцеклетки. В таких случаях рекомендуется проведение специального иммунологического обследования.