Тюбаж с магнезией как правильно сделать
Тюбаж с магнезией как правильно сделать
Нарушения моторики желчевыводящих путей
С.В. Бельмер, профессор кафедры детских болезней № 2 ГОУ ВПО «Российский государственный медицинский университет» Росздрава, д-р мед. наук
Среди многочисленных вариантов заболеваний желчевыводящих путей (холепатий) нарушения их моторики, или дискинезии, следует считать самыми распространенными, хотя бы по той причине, что они сопровождают практически любой патологический процесс в билиарном тракте.
Нарушения моторики желчевыводящих путей (ЖВП) можно подразделить на функциональные и связанные с органическими причинами. Также нарушения моторики билиарного тракта подразделяют на:
Причины дискинезий
Основными причинами дискинезий ЖВП являются:
Как следует из вышеуказанных причин, нарушения моторики ЖВП всегда носят вторичный характер. О «первичных дискинезиях» можно говорить лишь с определенной долей условности. В случае органических причин дискинезии и дистонии обусловлены поражением самих ЖВП, а при функциональных холепатиях – нарушением регуляции со стороны нервной системы.
Клинические проявления
Основными симптомами нарушений моторики ЖВП являются:
Характер болей в определенной степени определяется характером дискинезии: тупые боли после еды характерны для гипокинетических и гипотонических нарушений, тогда как сильные боли после нагрузки (физической или эмоциональной) указывают на гиперкинетические и гипертонические нарушения. Тошнота наблюдается относительно часто, но развитие рвоты указывает на тяжесть процесса. Горечь во рту является отражением нарушения моторики верхних отделов пищеварительного тракта в целом. Наконец, признаки холестаза могут отсутствовать или быть выражены в различной степени, что определяется характером основного патологического процесса.
При осмотре больного врач обращает внимание на «пузырные» симптомы, выявляемые при пальпации. Основными из них являются болезненность в точке проекции желчного пузыря, симптом Кера, симптом Мерфи, симптом Ортнера (Грекова), симптом Мюсси (Георгиевского; френикус-симптом). Всего же описано несколько десятков пузырных симптомов.
Дополнительные методы исследования
Исследования, позволяющие оценить моторику ЖВП и определить характер дискинезии:
Дуоденальное зондирование позволяет оценить моторику ЖВП, цитологический и биохимический состав желчи, провести ее микробиологическое исследование. В то же время дуоденальное зондирование – длительное и плохо переносимое ребенком исследование. При этом эффект раскрытия сфинктера Одди при использовании сульфата магния удается добиться примерно в 70% случаев. Противопоказаниями к дуоденальному зондированию являются острый холецистит, холангит, обострение хронического холецистита, холангита, варикозное расширение вен пищевода, стенозы пищевода, склонность к бронхоспазмам, сердечная недостаточность. Приведенные выше обстоятельства ограничивает сферу применения данного метода, несмотря на уникальную информацию (недоступную для других методов исследования), которую можно получить при грамотном его проведении.
Наиболее широко в настоящее время для диагностики холепатий применяют ультразвуковое исследование (УЗИ). Чаще всего для оценки моторики желчного пузыря проводят функциональные тесты, назначая желчегонный стимулятор и оценивая изменения размеров желчного пузыря, которые измеряют до и после стимуляции (по данным ультразвукового исследования или, реже, пероральной холецистографии). В качестве стимулятора используются яичные желтки, ксилит, сорбит, лекарственные препараты. В норме поперечник желчного пузыря и его объем через 45 минут должны сократиться примерно на 50%. Более интенсивное сокращение говорит о его гипермоторике (гиперкинезии), а слабое – гипомоторике (гипокинезии). Метод не дает прямого ответа на вопрос о тонусе сфинктеров. Можно предположить, что появление боли на фоне стимуляции сокращения желчного пузыря является косвенным признаком гипертонии сфинктерного аппарата. Аналогичные результаты можно получить, используя рентгенологические методы исследования (холецистография), однако необходимость лучевой нагрузки на ребенка, так же как введения контрастного вещества, несколько ограничивают область их применения.
Гепатобилиарная сцинтиграфия (радиоизотопное исследование печени) проводится, в первую очередь, с целью оценки функции гепатоцита, но одновременно позволяет изучить моторную функцию ЖВП. Метод не является повседневным в силу сложности, необходимости специального оборудования, дороговизны. Кроме того, он не позволяет оценить другие характеристика желчевыводящей системы (форму и размеры протоков и желчного пузыря и др.).
Лечение
Коррекцию нарушений моторики ЖВП начинают с поиска причины и ее устранения – лечения основного заболевания ЖВП, коррекции вегетативного статуса и т.д. (табл. 1)
Таблица 1
Алгоритм коррекции дискинезий и дистоний ЖВП
Диета. При любых формах дискинезий показано многократное питание в течение дня (5-6 раз), а также исключение жареных блюд, шоколада, какао, кофе, крепких бульонов, копченостей, газированных напитков.
При гипотонической гипокинетической формах дискинезий в диету должны быть включены фрукты, овощи, растительное и сливочное масло, сливки, сметана, яйца.
Желчегонные средства подразделяются на холеретики и холекинетики. Холеретики увеличивают концентрацию желчных кислот в желчи. К этой группе относятся препараты, содержащие компоненты бычьей желчи (Фестал, Аллохол, Холензим, Лиобил и др.) и/или растительные стеролы, входящие в состав желчегонных трав, увеличивающие концентрацию органических анионов. Противопоказаниями к назначению холеретиков, в первую очередь, содержащих компоненты желчи, являются гепатиты, циррозы печени, язвенная болезнь, эрозии слизистой оболочки желудочно-кишечного тракта, панкреатит, диарейный синдром. Эти же препараты, в связи с их раздражающим действием на слизистую оболочку желудочно-кишечного тракта, у детей с гастроэнтерологической патологией следует применять ограниченно.
Холекинетики стимулируют сократительную функцию желчного пузыря и снижают давление в билиарной системе (сернокислая магнезия, многоатомные спирты, растительные препараты – Фламин, Берберин и др.)
Высокоэффективным холекинетическим средством остаются тюбажи с минеральной водой. Утром натощак больной выпивает 100-150 мл теплой минеральной воды без газов, после чего ложится на правый бок, под который подкладывают теплую грелку, и лежит в течение 45-120 минут. В минеральную воду могут добавляться сорбит, сульфат магния, соль Барбара и др. Вместо минеральной воды могут использоваться соли, обладающие желчегонным эффектом, или мед. Конкретный стимулирующий состав подбирает врач, исходя из особенностей больного. Курс обычно состоит из 10 процедур, которые проводятся один раз в три дня.
Важным компонентом лечения являются холеспазмолитики (мебеверин, дротаверин, гимекромон и др.). Особое место среди миотропных спазмолитиков занимает мебеверин (Дюспаталин), обладающий двойным механизмом действия, препятствующим развитию гипотонии как побочного эффекта спазмолитической терапии. Особенностью Дюспаталина является его форма выпуска, обеспечивающая пролонгированный эффект. Дюспаталин назначается внутрь за 20 минут до еды по 1 капсуле 2 раза в день (утром и вечером). Многолетний опыт применения мебеверина показал не только эффективность препарата, но и его безопасность. Важной особенностью препарата является отсутствие антихолинергических эффектов, что значительно расширяет область его применения. В нашей стране Дюспаталин разрешен к применению у детей с 12 лет. Мебеверин является препаратом выбора для детей старше 12 лет при гипертонии сфинктеров, гиперкинезии и особенно при сочетании обоих нарушений.
Нейротропные средства назначаются с учетом характера дискинезии и вегетативной дисфункции. В соответствии с этим рекомендуют тонизирующие (женьшень, кофеин и т.п.) или седативные (бромиды, настой валерианы, настой пустырника и др.) препараты. Выбор препарата желательно обсудить с невропатологом.
Физиотерапия при гиперкинетических и гипертонических формах дискинезий может включать электрофорез с новокаином, парафиновые аппликации, общие радоновые или хвойные ванны, а при гипокинетических и гипотонических – электрофорез с или сульфатом магнезии, фарадизацию, гальванизацию, диадинамические токи Бернара.
Минеральные воды с высокой минерализацией, значительным содержанием газа, сульфатов, хлоридов (Ессентуки № 17, Арзни и др.) комнатной температуры или слегка подогретые за 30-60 минут до еды стимулируют моторику ЖВП, в то время как слабо минерализированные воды (Славяновская, Смирновская, Ессентуки №4, №20, Нарзан и др.) в подогретом виде обладают спазмолитическим и тормозящим моторику эффектом.
В качестве дополнительных средств при внепеченочном холестазе могут быть назначены гепатопротекторы, обеспечивающие защиту клеток печени и протоков от повреждающего действия желчи в условиях гипертензии в ЖВП.
Гепатопротекторы подразделяются на препараты:
Как проявляется лямблиоз у взрослых
Среди всех протозойных заболеваний, лямблиоз у взрослых занимает лидирующие позиции. Заболеваемости лямблиозом в одинаковой степени подвержены все люди, независимо от пола и возраста. Эта патология вызывает тяжелые расстройства пищеварения, влияет на функциональное состояние органов желудочно-кишечного тракта и может провоцировать тяжёлые осложнения.
Характеристики лямблиоза
Лямблиоз относится к группе кишечных инфекций, и развивается при попадании лямблий в просвет тонкой кишки. Это заболевание распространено повсеместно, а в развитых странах заболеваемость лямблиозом составляет от 3 до 5%.В развивающихся странах, распространенность лямблиоза составляет от 10 до 15%. Повышенному риску заболеваемости этой протозойной инфекцией подвержены дети, посещающие дошкольные и школьные учреждения.
Причины развития
По своей природе, лямблии являются простейшими одноклеточными паразитами. Питаются эти микроорганизмы с помощью осмоса. Источником распространения инфекции является больной человек, который выделяет лямблий с испражнениями в окружающую среду. Распространителями лямблиоза, также могут быть животные (морские свинки, кошки, кролики, собаки). Благоприятные условия для распространения инфекции и инфицирования людей создаются районах с низким качеством питьевой воды, при недостаточном уровне навыков личной гигиены среди населения, а также при большой скученности людей.
К предрасполагающим факторам развития лямблиоза, можно отнести:
Клинические симптомы
С момента проникновения возбудителей лямблиоза во внутреннюю среду организма и до момента появления клинических симптомов проходит от 1 до 3-х недель. К основным симптомам лямблиоза у взрослых можно отнести:
Острая фаза клинических симптомов поражения тонкой кишки может продолжаться от 5 до 7 дней. После завершения острой фазы, лямблиоз самопроизвольно проходит или переходит в хроническое подострое течение.
От масштабов инвазивного поражения кишечника лямблиями напрямую зависит выраженность интоксикации. Кроме перечисленных симптомов, лямблиоз может сопровождаться увеличением температуры тела до субфебрильных показателей, увеличением регионарных лимфатических узлов, быстрой утомляемостью, бруксизмом и эмоциональной лабильностью. Если данное заболевание развивается в детском возрасте, то оно нередко сопровождается гиперкинезами, снижением артериального давления и обморочными состояниями.
Методы диагностики
Клинические симптомы лямблиоза неспецифичны, поэтому диагностировать данную патологию на основании жалоб невозможно. Для диагностики лямблиоза назначаются такие методы обследования:
Лечение
Комплексное лечение лямблиоза включает ряд таких последовательных этапов:
На завершающем этапе комплексного лечения важно позаботиться о восстановлении кишечной микрофлоры. С этой целью используются метапребиотики, которые стимулируют рост и размножение естественной кишечной микрофлоры. Метапребиотик Стимбифид плюс восстанавливает популяцию собственных бифидумбактерий человека, количество которых значительно уменьшается при лямблиозе. Данное средство используется для лечения кишечных инфекций и их профилактики.
Кроме того, Стимбифид Плюс стимулирует иммунитет и ускоряет процесс регенерации кишечного эпителия. Метапребиотик может быть использован для профилактики лямблиоза у детей с 3-х лет. Средство благоприятно воспринимается организмом взрослых и детей, а также помогает ускорить процесс выздоровления при лямблиозе.
Магния сульфат (Magnesium sulfate)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Магния сульфат
| Порошок для приготовления раствора для приема внутрь | 1 пак. |
| магния сульфат | 100 % |
Фармакологическое действие
Механизм противосудорожного действия связан с уменьшением высвобождения ацетилхолина из нервно-мышечных синапсов, при этом магний подавляет нервно-мышечную передачу, оказывает прямое угнетающее действие на ЦНС.
Антиаритмическое действие магния обусловлено снижением возбудимости кардиомиоцитов, восстановлением ионного равновесия, стабилизацией клеточных мембран, нарушением натриевого тока, медленного входящего кальциевого тока и одностороннего калиевого тока. Кардиопротекторный эффект обусловлен расширением коронарных артерий, снижением ОПСС и агрегации тромбоцитов.
Токолитическое действие развивается в результате угнетения сократительной способности миометрия (снижение поглощения, связывания и распределения кальция в клетках гладкой мускулатуры) под влиянием ионом магния, усиления кровотока в матке в результате расширения ее сосудов. Магний является антидотом при отравлениях солями тяжелых металлов.
Фармакокинетика
После приема внутрь абсорбируется не более 20% принятой дозы.
Проникает через ГЭБ и плацентарный барьер, выделяется с грудным молоком в концентрации, в 2 раза превышающей концентрации в плазме. Выводится почками, скорость почечной экскреции пропорциональна концентрации в плазме и уровню клубочковой фильтрации.
Показания активных веществ препарата Магния сульфат
Для приема внутрь: запоры, холангит, холецистит, дискинезия желчного пузыря по гипотоническому типу (для проведения тюбажей), дуоденальное зондирование (для получения пузырной порции желчи), очищение кишечника перед диагностическими манипуляциями.
Отравление солями тяжелых металлов (ртуть, мышьяк, тетраэтилсвинец, барий).
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| E61.2 | Недостаточность магния |
| G40 | Эпилепсия |
| G93.4 | Энцефалопатия неуточненная |
| I10 | Эссенциальная [первичная] гипертензия |
| I47.2 | Желудочковая тахикардия |
| I51.9 | Болезнь сердца неуточненная |
| K59.0 | Запор |
| K81.0 | Острый холецистит |
| K81.1 | Хронический холецистит |
| K82.8 | Другие уточненные болезни желчного пузыря и пузырного протока (в т.ч. дискинезия) |
| K83.0 | Холангит |
| O15 | Эклампсия |
| O60 | Преждевременные роды и родоразрешение |
| R25.2 | Судорога и спазм |
| R29.0 | Тетания |
| R33 | Задержка мочи |
| T50.9 | Другими и неуточненными лекарственными средствами, медикаментами и биологическими веществами |
| T56.0 | Свинца и его соединений |
| T56.1 | Ртути и ее соединений |
| T57.0 | Мышьяка и его соединений |
| Z51.4 | Подготовительные процедуры для последующего лечения или обследования, не классифицированные в других рубриках |
Режим дозирования
Применяют внутрь, в/м и в/в (струйно медленно или капельно). Дозу, способ и схему применения, длительность терапии определяют индивидуально, в зависимости от показаний, клинической ситуации и возраста пациента.
Побочное действие
Ранние признаки и симптомы гипермагниемии: брадикардия, диплопия, внезапный прилив крови к лицу, головная боль, головокружение, снижение АД, тошнота, одышка, смазанная речь, рвота, астения.
Признаки гипермагниемии (в порядке повышения концентрации магния в сыворотке крови): снижение глубоких сухожильных рефлексов (2-3.5 ммоль/л), удлинение интервала PQ и расширение комплекса QRS на ЭКГ (2.5-5 ммоль/л), утрата глубоких сухожильных рефлексов (4-5 ммоль/л), угнетение дыхательного центра (5-6.5 ммоль/л), нарушение проводимости сердца (7.5 ммоль/л), остановка сердца (12.5 ммоль/л).
При приеме внутрь: тошнота, рвота, диарея, обострение воспалительных заболеваний ЖКТ, нарушение электролитного баланса (повышенная утомляемость, астения, спутанное сознание, аритмия, судороги), метеоризм, абдоминальная боль спастического характера, жажда, признаки гипермагниемии при наличии почечной недостаточности.
При в/в введении: замедление частоты дыхания, одышка; острая недостаточность кровообращения; ослабление рефлексов; гиперемия; выраженное снижение АД; гипотермия; ослабление мышечного тонуса; атония матки; гипергидроз; тревога; выраженная седация; полиурия; урежение ЧСС; изменения на ЭКГ. Магния сульфат понижает возбудимость дыхательного центра, высокие дозы при парентеральном введении могут вызвать паралич дыхательного центра.
Противопоказания к применению
Повышенная чувствительность к магния сульфату; хроническая почечная недостаточность тяжелой степени.
Для приема внутрь: аппендицит, ректальное кровотечение (в т.ч. недиагностированное), кишечная непроходимость, дегидратация, гипермагнемия; беременность, период грудного вскармливания; детский возраст до 18 лет.
С осторожностью: нарушение проводимости сердца, сердечная недостаточность, хроническая почечная недостаточность.
Для парентерального введения: тяжелая артериальная гипотензия, угнетение дыхательного центра, тяжелая брадикардия, AV-блокада I-III степени; предродовый период (за 2 ч до родов); состояния, связанные с дефицитом кальция.
С осторожностью: миастения; хроническая почечная недостаточность (клиренс креатинина 20-60 мл/мин); заболевания органов дыхания; острые воспалительные заболевания ЖКТ; пожилой возраст, беременность, период грудного вскармливания, возраст до 18 лет.
Применение при беременности и кормлении грудью
Противопоказано применение магния сульфата внутрь при беременности. Парентеральное применение при беременности возможно только по назначению врача, если предполагаемая польза для матери превышает потенциальный риск для плода; противопоказано применение в предродовой период (за 2 часа до родов).
При необходимости применения в период лактации грудное вскармливание следует прекратить.
Применение при нарушениях функции почек
Противопоказан при хронической почечной недостаточности тяжелой степени. C осторожностью принимать внутрь или вводить парентерально при хронической почечной недостаточности.
Применение у детей
Возможно применение у детей по показаниям, в рекомендуемых соответственно возрасту дозах и лекарственных формах. Необходимо строго следовать указаниям в инструкциях препаратов магния сульфата по противопоказаниям к применению у детей разного возраста конкретных лекарственных форм магния сульфата.
Применение у пожилых пациентов
С осторожностью применять парентерально у пациентов пожилого возраста, у этой категории больных обычно следует применять уменьшенную дозу, т.к. у них снижена функция почек.
Особые указания
C осторожностью принимать внутрь или вводить парентерально при блокаде сердца, поражении миокарда, хронической почечной недостаточности, заболеваниях органов дыхания, острых воспалительных заболеваниях ЖКТ, беременности.
Магния сульфат следует применять осторожно у пациентов пожилого возраста У этой категории больных обычно следует применять уменьшенную дозу, т.к. у них снижена функция почек.
Магния сульфат можно применять для купирования эпилептического статуса (в составе комплексного лечения).
При применении магния сульфата могут быть искажены результаты радиологических исследований, для которых применяется технеций.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения пациентам следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (риск развития диплопии, головокружения, головной боли).
Лекарственное взаимодействие
Магния сульфат усиливает эффект других лекарственных средств, угнетающих ЦНС.
При парентеральном применении магния сульфата и одновременном применении миорелаксантов периферического действия происходит усиление эффектов миорелаксантов периферического действия.
Описан случай остановки дыхания при применении гентамицина у грудного ребенка с повышенной концентрацией магния в плазме крови на фоне терапии магния сульфатом.
При одновременном применении с нифедипином возможна выраженная мышечная слабость.
Уменьшает эффективность пероральных антикоагулянтов (в т.ч. кумариновых производных или дериватов индандиона), сердечных гликозидов, фенотиазинов (особенно хлорпромазина). Снижает абсорбцию ципрофлоксацина, этидроновой кислоты, ослабляет действие стрептомицина и тобрамицина.
При совместном применении магния сульфата для парентерального введения с другими вазодилататорами возможно усиление гипотензивного эффекта.
Нарушает всасывание антибиотиков группы тетрациклина, ослабляет действие стрептомицина и тобрамицина. Соли кальция уменьшают действие магния сульфата.
При содержании ионов магния выше 10 ммоль/мл в смесях для полного парентерального питания возможно разделение жировых эмульсий.
Фармацевтически несовместим (образуется осадок) с препаратами кальция, этанолом (в высоких концентрациях), карбонатами, гидрокарбонатами и фосфатами щелочных металлов, солями мышьяковой кислоты, бария, стронция, клиндамицина фосфатом, гидрокортизона натрия сукцинатом, полимиксина В сульфатом, прокаина гидрохлоридом, салицилатами и тартратами.
Функциональные расстройства желчевыводящей системы у детей
Дискинезия желчевыводящих путей является классическим представителем функциональных нарушений (заболеваний) желудочно-кишечного тракта. Современное определение, согласно D. A. Drossman, гласит, что «функциональные нарушения — это разнообразная

Структура желчевыводящей системы складывается из правого и левого печеночного протоков, общего печеночного протока, желчного пузыря (ЖП), пузырного протока, общего желчного протока. Общий желчный проток открывается в двенадцатиперстную кишку вместе с главным панкреатическим протоком через выступающий в ее просвет большой дуоденальный (Фатеров) сосок, в толще которого расположен истинный анатомический сфинктер — сфинктер Одди, который регулирует поступление желчи и панкреатического секрета в кишечник. Сфинктер Одди состоит из собственного сфинктера большого дуоденального сосочка, сфинктера общего желчного протока и сфинктера панкреатического протока. В редких случаях эти сфинктеры открываются в просвет двенадцатиперстной кишки отдельно. Кроме анатомического, в желчевыводящей системе выделяют два функциональных сфинктера — сфинктер Мирици (при слиянии правого и левого печеночных протоков) и Люткенса (в месте перехода шейки ЖП в пузырный проток). Основная задача сфинктерного аппарата — регуляция поступления желчи в кишку и предотвращение рефлюксов. Желчевыводящая система имеет общее для всего желудочно-кишечного тракта слоистое строение, включая слизистую и подслизистую оболочки, мышечный слой из продольных и циркулярных волокон и рыхлую наружную соединительнотканную оболочку, в которой расположены сосуды и нервы. Кроме обеспечения пассажа желчи, билиарные пути принимают участие в формировании окончательного состава желчи, поскольку слизистая оболочка отвечает за процессы всасывания и секреции воды, хлоридов, бикарбонатов и др.
Регуляция работы желчевыводящей системы координируется и контролируется вегетативной нервной системой (plexus hepaticus, симпатическим и парасимпатическим отделом) и нейрогуморальными факторами (холецистокинином, гастрином, секретином), среди которых наиболее значимым влиянием обладает холецистокинин. Умеренное раздражение блуждающего нерва вызывает координированную активность ЖП и сфинктеров, сильное раздражение — спастическое его сокращение. Повышение тонуса симпатического звена — расслабление сфинктеров и снижение тонуса ЖП. Забегая вперед, необходимо отметить, что большинство детей старшего возраста, особенно с заболеваниями верхних отделов желудочно-кишечного тракта, — парасимпатотоники, что априорно обуславливает гипертонический тип дисфункции желчевыводящей системы. В норме сфинктер Одди периодически открывается и в межпищеварительный период желчь равномерно истекает в просвет 12-перстной кишки со скоростью 4–5 капель в минуту. Самым сильным стимулятором сокращения ЖП является прием пищи. Поступление желчи в 12-перстную кишку совпадает со временем прохождения перистальтической волны через привратник. При поступлении пищи в 12-перстной кишке вырабатывается регуляторный пептид — холецистокинин, регулирующий дальнейшее сокращение ЖП. Время тонического сокращения ЖП зависит от объема и качественного состава принятой пищи — при обильной еде, особенно жирной, сокращение ЖП длится до полного опорожнения желудка. При приеме небольшого количества пищи, особенно с небольшим содержанием жиров, сокращение ЖП кратковременное. Подобную закономерность сокращения ЖП необходимо учитывать при построении функциональных проб и использовать только адекватные желчегонные завтраки. Из пищевых веществ максимальное сокращение ЖП вызывают яичные желтки — до 80%. После сокращения тонус ЖП снижается и наступает период наполнения его желчью.
Причины развития функциональных нарушений билиарного тракта. Причины функциональных нарушений, как правило, связаны с расстройством регуляции органа, функция которого нарушена. Эти изменения нервной регуляции провоцируются обычно психоэмоциональными и стрессорными факторами и обусловлены вегетативными нарушениями или органическим поражением ЦНС с последующим развитием вегетативной дисфункции. У детей первого года жизни функциональные нарушения желудочно-кишечного тракта чаще всего являются проявлением перинатальных поражений ЦНС в структуре вегето-висцерального синдрома или натальной травмы спинальных отделов нервной системы. В более старшем возрасте возрастает роль рефлекторных и нейрогуморальных нарушений при развитии хронических заболеваний желудочного кишечного тракта. К развитию моторно-тонических нарушений билиарного тракта приводят вегетативные расстройства, неврозы, психоэмоциональные нарушения, пищевая аллергия, паразитозы и хронические заболевания пищеварительной системы, нарушения режима питания, гиподинамия, курение, алкоголь и многое другое.
Терминология и классификация. В российской медицинской литературе широко употребляется и привычен термин «дискинезия желчевыводящих путей» (ДЖВП). В зарубежной медицинской практике ему соответствует понятие «дисфункциональные расстройства билиарного тракта». Существует много определений ДЖВП. Самым полным определением дискинетических расстройств билиарного тракта можно считать определение, предложенное отечественными гастроэнтерологами академиком А. Л. Гребеневым и профессором А. А. Шептулиным в 1997 г.: «ДЖВП — расстройство моторно-тонической функции желчевыводящей системы, в основе которого лежит несогласованное (чрезмерное или недостаточное) сокращение ЖП, сфинктеров Одди, Люткенса, Мирици, вследствие нарушения взаимодействия иннервационной и паракринной систем, координирующих последовательность их сокращения и расслабления». МКБ 10 выделяет две формы — дискинезия ЖП и пузырного протока (К 82,8) и спазм сфинктера Одди (К 83,4). Согласно Римскому консенсусу III (Лос-Анжелес, 2006) выделяют следующие формы дискинетических расстройств: Е1 — функциональные нарушения ЖП, Е2 — функциональное билиарное нарушение сфинктера Одди, Е3 — функциональное панкреатическое нарушение сфинктера Одди. Нарушение синхронности в работе ЖП и сфинктерного аппарата является причиной формирования клинической симптоматики.
Клинические проявления. Для больных с ДЖВП типичны жалобы на колющие боли в правом боку или подреберье после жирной, жареной пищи или при физической или эмоциональной нагрузке. Подобная симптоматика обусловлена спастическим состоянием сфинктера Одди или чрезмерными сокращениями мышечного слоя ЖП. При перерастяжении ЖП (при гипотонии или нарушенном желчеоттоке вследствие выраженного спазма сфинктеров) появляются жалобы на чувство тяжести и/или распирания в правом боку или подреберье. При употреблении жирной или жареной пищи возможно появление тошноты или рвоты.
При объективном осмотре можно отметить болезненность при пальпации в правом подреберье, положительные пузырные симптомы, в том числе и положительный frenicus-симптом справа.
Диагностика. Из исследований клинического минимума только в копрограмме можно отметить признаки нарушения желчеотделения — нейтральный жир, жирные кислоты, мыла. В биохимическом спектре крови можно отметить повышение уровня щелочной фосфатазы. По критериям Римского консенсуса при панкреатической дисфункции сфинктера Одди отмечается повышение уровня липазы и амилазы в крови. Дуоденальное зондирование сегодня редко применяется в клинической практике. Самым частым и доступным методом исследования состояния желчевыводящих путей является ультразвуковая диагностика. УЗ-исследование ЖП проводится натощак. В норме ЖП имеет округлую, овальную или грушевидную форму. Толщина стенки ЖП может колебаться в норме от 0 до 4 мм, при описании стенки важна однородность ее структуры. Просвет пузыря эхонегативен. Размеры ЖП вариабельны и мало зависят от возраста. В наших наблюдениях встречался длинник желчного пузыря, равный 7 см у новорожденного и 4 см у подростка. Средняя длина ЖП при УЗ-исследовании составляет 5–7 см, ширина 1,2–2,5 см. Необходимо помнить, что УЗ-размеры пузыря не соответствуют его истинным анатомическим размерам и категорически неправильно на основании только увеличения УЗ-размеров без проведения функционального исследования устанавливать диагноз гипомоторной дисфункции ЖП!
Частой находкой при ДЖВП на УЗИ является локация густой неоднородной желчи в просвете ЖП, что свидетельствует о ее застойных изменениях.
С момента внедрения УЗ-исследования в клиническую практику резко возросло выявление аномалий формы ЖП (перегибов).
Необходимо помнить, что большая часть выявленных перегибов являются функциональными (при исследовании в положении стоя они расправляются) и связаны с интенсивным ростом ЖП и малой емкостью его ложа. В процессе роста ребенка такие перегибы неоднократно могут появляться и исчезать и принимать порой самые причудливые формы. Ошибкой является постановка диагноза ДЖВП только на основе выявления функциональных перегибов, поскольку они редко затрудняют желчеотток, хотя их можно отнести к предрасполагающим факторам.
Функциональное исследование сократительной способности ЖП (эхохолецистографию) лучше всего проводить по методике, предложенной в НИИ педиатрии в 1987 году. Согласно этой методике размеры ЖП снимаются натощак и через каждые 15 минут после приема желчегонного завтрака в течение 90 минут. Оптимальным завтраком являются сырые желтки или ксилит (5 г/20 кг веса). Использование других завтраков (хлеб с маслом, йогурт, сметана, сыр, шоколад) вызывает или слабое, или отсроченное сокращение ЖП, что приводит к ошибочному диагнозу гипомоторной дискинезии. При нормальном сокращении ЖП его объем сокращается примерно на 50% через 30–60 минут после приема желчегонного завтрака, затем отмечается его восстановление. Контрольное определение размеров ЖП только через час после начала исследования (без промежуточных измерений) приводит опять-таки к ошибочному диагнозу гипомоторной дисфункции в силу того, что через 1 час у многих детей происходит восстановление объема (рис.), а исследователи делают вывод о снижении моторной функции ЖП.
У детей с явлениями ДЖВП на фоне хронического заболевания желудочно-кишечного тракта чаще отмечается нормокинетический или гиперкинетический вариант сокращения ЖП (рис.).
Нами было проведено изучение сократительнеой функции ЖП у детей с неврологическими отклонениями (последствиями перинатальных поражений ЦНС). Итоги исследования сократительной функции ЖП у детей с последствиями перинатальных поражений ЦНС выявили настолько индивидуальный и хаотичный кинетический профиль сокращения, что у этих пациентов невозможно было говорить о нормо- или гиперкинезе ЖП, в связи с чем не представлялось возможным сделать заключение о варианте дисфункции. Вот почему более правильно в данных случаях говорить о некоординированном сокращении ЖП, которое в свою очередь обусловлено дисфункцией вегетативной нервной системы на фоне последствий перинатальных поражений ЦНС. Сразу необходимо отметить, что суммарное сокращение объема ЖП составляло 50–95%, что исключает гипотонический вариант дисфункции.
Другие методы исследования, такие как ретроградная холангиопанкреатография, сцинтиграфия билиарного тракта, редко применяются в отечественной медицинской практике.
Лечение функциональных нарушений желчевыводящей системы. В первую очередь при лечении любого заболевания необходимо обратить внимание на оптимизацию образа жизни и нивелировать воздействие предрасполагающих и повреждающих факторов. Так, рекомендуется нормализовать длительность ночного сна, поскольку именно во сне происходит восстановление регуляторных процессов со стороны ЦНС. Физиологическая длительность ночного сна в подростковом возрасте составляет 8 часов в сутки, у младших школьников 9–10 часов. При выраженном астеническом синдроме рекомендуется дополнительный дневной сон. Достаточная ежедневная физическая активность и прогулки являются профилактическим и лечебным компонентом при ведении больных с ДЖВП. Существенное повреждающее действие на центральную нервную и вегетативную систему оказывает электромагнитное излучение, в связи с чем необходимо ограничивать время просмотра телепередач и работы за компьютером до 2–3 часов в день. Что касается фактора питания, то при патологии желчевыводящей системы рекомендуется диета № 5. Поскольку сам факт приема пищи является хорошим стимулятором поступления желчи в 12-перстную кишку, питание должно быть регулярным, необильным, 4–5 раз в день. Рекомендуется механическое и химическое щажение, пища готовится на пару либо в отварном виде. Рекомендуются: овощные и фруктовые салаты, винегреты, яйца всмятку, сыр, творог, мясо и рыба в отварном или запеченном виде, вегетарианские супы, молочные и кисломолочные продукты, соки. Разрешается добавлять растительные масла в салаты в каждый прием пищи в небольшом количестве. Исключаются блюда с высоким содержанием экстрактивных веществ (крепкие мясные, рыбные, грибные бульоны, пряности, маринады, копчености), ограничиваются тугоплавкие жиры — сало, свинина. Исключаются газированные напитки и холодные напитки и блюда (способствуют спазму желчных путей).
Медикаментозная терапия. Медикаментозное лечение при дисфункциональных заболеваниях билиарного тракта зависит от формы дисфункции и характера основного заболевания и должно быть комплексным. Учитывая большую роль нарушений вегетативной и центральной нервной систем в реализации билиарных расстройств, необходимо использовать средства, направленные на восстановление нарушенной регуляции, проводится лечение заболеваний, на фоне которых развился дискинетический процесс.
При гипертонической форме дисфункции для купирования болевого синдрома назначаются спазмолитики: Но-шпа, Папаверин гидрохлорида, Дибазол и др. Назначаются препараты в возрастных дозах, коротким курсом 3–5 дней, поскольку все они обладают системным спазмолитическим действием. В клинической практике сегодня широко используется периферический спазмолитик мебеверин (Дюспаталин). Дюспаталин назначается за 20 минут до приема пищи по 1 капсуле 2 раза в день, может применяться длительно (разрешен к применению у детей старше 12 лет). После купирования болевого синдрома проводится подбор дальнейшей терапии. Как правило, современные препараты, применяемые для коррекции дисфункции билиарного тракта, обладают сочетанным действием: мягким спазмолитическим, холеретическим и холекинетическим, гепатопротекторным, что позволяет индивидуализировать проводимую терапию. Ниже приводится характеристика некоторых рекомендуемых препаратов.
Олиметин. Растительный препарат (масло аира, мяты, оливковое, терпентинное, сера), форма выпуска — капсулы. Обладает спазмолитическим, холеретическим, противовоспалительным, мочегонным действием. Принимается по 1–2 капсулы в день до еды.
Холасас. Сгущенный водный экстракт плодов шиповника. Форма выпуска — сироп. Обладает желчегонным действием. Назначается по 1/2–1 чайной ложке до еды.
Холагол. Комбинированный препарат (куркума, крушина, оливковое масло, магния салицилат), обладает противовоспалительным и желчегонным действием. Форма выпуска — капли. Применяется по 1–5 капель на кусочек сахара или хлеба за 30 минут до еды.
Гепабене. Комбинированный препарат (дымянка аптечная, расторопша), обладает холеретическим, холекинетическим и гепатопротекторным действием. Форма выпуска — капсулы (разрешен к применению у детей старше 6 лет). Назначается по 1–2 капсулы во время еды.
Одестон. Действующее вещество — гимекромон. Обладает периферическим селективным спазмолитическим и желчегонным действием. Форма выпуска — таблетки. Принимается за 30 минут до еды.
ЛИВ-52. Комплексный препарат растительного происхождения (каперсы колючие, цикорий, паслен черный, сенна, терминалия, тысячелистник, тамарикс гальский), обладает широким спектром активности, оказывая противовоспалительное, желчегонное, гепатопротекторное и спазмолитическое действие. Форма выпуска — капли и таблетки. Разрешен к применению у детей с 2-х лет. Назначается за 10–15 минут до еды.
Хофитол. Препарат на основе артишока полевого. Обладает системным комплексным действием; гепатопротектор растительного происхождения, увеличивает отток желчи, уменьшает внутрипеченочный холестаз, обладает мягким диуретическим эффектом, снижает содержание азотистых веществ в крови, проявляет антиоксидантную активность, улучшает антитоксическую функцию печени, кроме того, уменьшает синтез холестерина гепатоцитами, нормализует внутриклеточный обмен фосфолипидов, снижает атерогенные фракции холестерина, нормализует показатели липидограммы. Разрешен к применению у детей с первых дней жизни. Имеет следующие формы выпуска: раствор (с низким объемным содержанием спирта), таблетки и раствор для инъекций в ампулах. Принимается до еды.
Галстена. Комплексный гомеопатический препарат (расторопша, одуванчик, чистотел, сульфат Na, фосфор). Обладает противовоспалительным желчегонным и гепатопротекторным действием. Форма выпуска — капли. Разрешен к применению у детей младшего возраста. Назначается за 30 минут до еды.
Хепель. Комплексный гомеопатический препарат. Обладает противовоспалительным, желчегонным и гепатопротекторным действием, нормализует процессы вегетативной регуляции желчевыводящей системы. Форма выпуска — таблетки. Назначается сублингвально за 30 минут до еды.
Нужно отметить, что рынок лекарственных препаратов, в том числе и желчегонных, пополняется ежегодно. Как уже говорилось ранее, для оптимизации лечения необходимо учитывать спектр действия препарата и особенности течения заболевания у больного. При выявлении синдрома сгущения желчи, обменных нарушений или обнаружении кристаллических изменений структуры желчи (по данным УЗИ) необходимо выбирать препарат, обладающий гепатопротекторным действием, или назначать отдельные курсы гепатопротекторной терапии. Средний курс медикаментозного лечения при билиарной дисфункции составляет 2–3 недели. Затем для закрепления эффекта можно рекомендовать фитотерапию. Выбор трав, обладающих желчегонным действием, достаточно широк: аир болотный, артишок посевной, барбарис обыкновенный, бессмертник песчаный, одуванчик лекарственный, мята перечная, сушеница топяная, кукурузные рыльца, шалфей лекарственный и др. Курс фитотерапии в среднем составляет 1 месяц, можно использовать лечебный фиточай. Хорошим дренажным действием обладают тюбажи, необходимо отметить, что тюбажи назначаются только после купирования спастического состояния сфинктеров, соответственно на втором или третьем этапе лечения. Техника проведения тюбажей (по Демьянову): утром натощак пациенту дают выпить «желчегонный завтрак», которым может быть 15–20 мл 33% теплого раствора сернокислой магнезии, или 2 яичных желтка, или теплое оливковое (кукурузное масло), или 100–200 мл 10% раствора сорбита, ксилита, теплая минеральная вода (3 мл/кг веса); затем надо уложить его на правый бок на теплую грелку на 1,5–2 часа, во время процедуры для открытия сфинктера Одди делать по 2–3 глубоких вдоха каждые 5 минут. Рекомендуется проведение 1–2 процедур в неделю, курс 8–10 процедур.
Физиотерапия. Применяются методики, направленные на нормализацию деятельности ЦНС и ВНС; фотохромотерапия или электрофорез с Са и Br по Щербаку на воротниковую зону, трансаир, КВЧ-пунктура на область проекции 7-го шейного позвонка. Местно — электрофорез с 5% раствором сернокислой магнезии, парафиновые или озокеритовые аппликации, индуктотермия на область правого подреберья, курс 8–10 процедур.
Диспансеризация. Характер и объем проводимых диспансерных мероприятий определяются структурой имеющейся патологии.
В. А. Александрова, доктор медицинских наук, профессор
С. В. Рычкова, кандидат медицинских наук, доцент
СПб МАПО, Санкт-Петербург
Дискинезия желчевыводящих путей у детей
Статья обновлена: 2020-01-05
Дискинезии желчного пузыря чаще всего являются проявлением вегетативных дисфункций, однако могут возникать на фоне поражения желчного пузыря (при воспалении, изменении состава желчи, холелитиазе), а также при заболеваниях других органов пищеварения. У детей первого года жизни функциональные нарушения чаще всего являются проявлением перинатальных поражений центральной нервной системы в структуре вегето-висцерального синдрома или натальной травмы спинальных отделов нервной системы.
В более старшем возрасте к развитию нарушений желчевыводящих путей приводят вегетативные расстройства, неврозы, психоэмоциональные нарушения, нарушения режима питания, гипотония, пищевая аллергия, паразиты и хронические заболевания пищеварительной системы, нарушения режима питания, курение, алкоголь и др.
Симптомы дискинезии желчного пузыря
Симптомы гиперкинетической и гипокинетической формы дискинезии желчного пузыря имеют некоторые отличия.
Гиперкинетическая форма дискинезии желчного пузыря.
Гипокинетическая формы дискинезии желчного пузыря.
Дифференциальную диагностику дискинезии проводят с органическими поражениями желчного пузыря: холециститом, панкреатитом, язвенной болезнью, паразитарной инвазией.
Симптомы дисфункции сфинктера Одди
Симптомы дисфункции сфинктера Одди включают: боль в животе (самый распространенный симптом), тошнота, рвота, лихорадка, озноб, диарея. Читайте больше в статье «Дисфункции сфинктера Одди и их лечение».
Лечение дискинезии желчного пузыря
Лечение начинается после медицинского обследования ребенка и зависит от формы дисфункции и характера основного заболевания. Лечение должно быть комплексным.
Существенное повреждающее действие на центральную нервную и вегетативную систему оказывает электромагнитное излучение, в связи с чем необходимо ограничивать время просмотра телепередач и работы за компьютером до 2–3 часов в день.
Травы, обладающие желчегонным действием: сушеница топяная, артишок посевной, аир болотный, бессмертник песчаный, одуванчик лекарственный, барбарис обыкновенный, мята перечная, кукурузные рыльца, шалфей лекарственный и др. Курс фитотерапии в среднем составляет 1 месяц.
Рекомендуют электрофорез папаверина, новокаина, тепловые процедуры (парафиновые и озокеритовые аппликации) на область печени.
В питании, кроме общих рекомендаций, описаных выше, необходимо ограничить прием продуктов, стимулирующих отделение желчи: яйца, пряности, растительное масло.
При гипокинетической форме рекомендуют нейротропные средства стимулирующего действия: настойку женьшеня, экстракт алоэ, пантокрин, элеутерококк по 1-2 капли на год жизни 3 раза в сутки.
Показаны холекинетики (домперидон, магния сульфат и др.), ферменты.
В питании рекомендован прием продуктов, стимулирующих отделение желчи: яйца, пряности, растительное масло, овощи, фрукты.
Как сделать тюбаж?
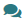
Искусство диетотерапии при заболеваниях желчевыводящих путей
Питание является важнейшей составляющей частью терапии заболеваний желчевыводящих путей. С помощью диеты можно воздействовать на различные механизмы патогенеза при данной патологии: холестатический синдром, нарушение физико-химических свойств желчи, воспаление, дисмоторику желчевыводящих путей и кишечника.
Для нормального функционирования билиарной системы необходимы следующие условия: адекватная выработка желчи гепатоцитами, беспрепятственный ее пассаж по желчевыводящим путям, хорошая сократительная функция желчного пузыря и нормальное давление в просвете двенадцатиперстной кишки.
Питание является важнейшей составляющей частью терапии заболеваний желчевыводящих путей
Белок в рационе
Холерез (выделение желчи печеночными клетками) зависит от характера питания, прежде всего от количества и качества белков в рационе. Большинство клиницистов считают, что количество белков в рационе должно соответствовать физиологической норме: 1 г на 1 кг идеальной массы тела, из них 50 % должны составлять белки животного происхождения (мясо, рыба, птица, яйца, молочные продукты).
Белки являются важнейшим фактором, обеспечивающим стабильность растворов холестерина за счет увеличения содержания желчных кислот и относительного снижения уровня холестерина. Животные белки богаты незаменимыми аминокислотами и липотропными факторами (метионином, холином), которые предупреждают развитие жировой дистрофии печени. Из продуктов растительного происхождения большое количество метионина и холина содержат соевая мука, овсяная и гречневая крупы. Особый интерес представляют серосодержащие аминокислоты (метионин, цистин, цистеин), так как сера усиливает холерез, входит в состав цитохромов и таурина, необходимого для связывания желчных кислот. Аминокислоты триптофан и тирозин также стимулируют синтез в печени желчных кислот. Повышенное количество белков (до 1,5 г/кг) требуется больным при наличии белково-энергетической недостаточности.
Адекватно обеспечить потребности организма в белке только за счет обычной пищи — слишком сложная задача диетологии во многих клинических случаях, особенно когда идет речь о лечении больных в острой фазе заболеваний, в случаях энтеральной несостоятельности пищеварительного конвейера и, конечно, при белково-энергетической недостаточности. Именно для этого согласно Приказу Минздрава РФ № 330 от 5.08.2003 «О мерах по совершенствованию лечебного питания в лечебно-профилактических учреждениях Российской Федерации» (с изменениями, внесенными приказом Минздравсоцразвития России от 26.04.2006 № 316) для оптимального решения данной проблемы рекомендованы специализированные продукты питания.
В первую очередь здесь стоит обратить внимание на смеси белковые композитные сухие (СБКС) (такие, например, как «Дисо®» «Нутринор», «Дисо®» «Нутрифиб») — группу продуктов наиболее глубоко и по широкому диапазону нозологических форм с хорошими результатами, изученных в клинической медицине. За счет введения данных продуктов в стандартные, специализированные и индивидуальные диеты осуществляется замена до 20 % белков ежедневного рациона диетического питания пациента белками, обладающими высокой пластичностью, способностью быстро и без перегрузок ферментных систем утилизироваться на всех физиологических этапах пищеварения, выигрышно по отношению к белкам традиционного питания россиянина не сопровождающимися неблагоприятными реакциями организма в виде различных форм пищевой непереносимости.
Для решения рассматриваемого вопроса у больных с билиарной патологией смеси белковые композитные сухие вводятся в карточки- раскладки в качестве компонента для приготовления готовых блюд для диетического (лечебного) питания. Следует обратить внимание, что СБКС, относящиеся к категории средств усиленного диетического питания, безопасны и соответствуют установленным санитарно-гигиеническим нормам.
Наиболее часто в своей клинической деятельности мы (авторы данной статьи) используем смесь белковую композитную сухую «Дисо®» «Нутринор». Этот продукт имеет хорошие вкусовые данные, при использовании не нарушает привычных органолептических и вкусовых качеств готовых блюд, его применение значительно сокращает время приготовления специализированных блюд (исключается процесс протирания). В 20,0 г (1 ст. л.) смеси «Дисо®» «Нутринор» содержится 8,0 г белков высокой биологической активности, поэтому двукратный прием этого продукта обеспечивает 20–25 % суточной потребности белка.
Приводим несколько вариантов приготовления готовых блюд с использованием смесей белковых композитных сухих для больных с обострениями хронических заболеваний системы желчевыделения и при острых билиарных процессах:
Большой опыт авторов настоящей статьи в использовании белковых специализированных продуктов в диетическом питании при самых различных заболеваниях, в том числе послеоперационных состояниях, позволяет им планировать серию статей по данному вопросу в будущих номерах журнала.
Режим питания при заболеваниях желчевыводящих путей
Большое значение для профилактики и лечения холестатического синдрома имеет режим питания. Сокращение желчного пузыря происходит в ответ на прием пищи. «Лучшим средством, противодействующим застою желчи, является частый прием пищи… каждые 3–4 часа», — писал основоположник отечественной диетологии М. И. Певзнер (1949). Это положение часто нарушается пациентами, рацион у некоторых состоит из завтрака и ужина. Редкие приемы пищи способствуют развитию холестаза (недостаточности выделения желчи, обусловленной нарушением ее выработки печеночными клетками или прекращением тока желчи по желчным протокам), а при наличии повышенной литогенности желчи — образованию камней. Дробное питание помогает избежать переедания. Обильные приемы даже диетической пищи могут вызвать боль и диспепсические явления, спровоцировать приступ печеночной колики у больных желчнокаменной болезнью.
Жиры в рационе
Наиболее выраженным холекинетическим действием обладают жиры. Жиры улучшают вкусовые качества пищи, вызывают чувство насыщения, способствуют усвоению жирорастворимых витаминов (A, D, E, К), являются самым богатым источником энергии.
Хотите больше информации по вопросам диетологии?
Приобретите информационно-практический журнал «Практическая диетология» в электронном или печатном формате! особенно разбавленные в 10 раз. При этом морковный, капустный и брюквенный соки не вызывают раздражения слизистой оболочки желудка в отличие от свекольного и редечного.
Сочетание овощных соков с белками, жирами и углеводами пищи приводит к увеличению желчеобразования в среднем на 49 %. По мнению Н. И. Лепорского, сочетание овощей с жирами — это холеретика (желчегонное средство), не уступающая многим лекарствам. В последующие годы другими исследователями было также показано стимулирующее влияние овощей и соков на функции желудка, поджелудочной железы и желчеотделение. Так, в своей клинической деятельности мы с успехом применяли диету с включением на второй завтрак сырой тертой моркови (150 г) с растительным маслом (10 г) и добавлением 6 г микрокристаллической целлюлозы в кислородный коктейль, котлеты, запеканки или соусы. На фоне данной диеты достоверно чаще по сравнению со стандартной диетой № 5 уменьшались явления холестаза и запоры.
Уменьшить воспаление
С целью уменьшения воспаления в желчном пузыре в диете ограничивают поваренную соль до 3 г в сутки и простые углеводы (10 % от общего количества углеводов), избыточное потребление которых не только поддерживает воспаление, но и увеличивает насыщение желчи холестерином, способствует застою желчи и сдвигу ее рН в кислую сторону, таким образом, создает условия для образования холестериновых камней. Общее количество углеводов соответствует физиологической норме.
Ценность пищевых волокон
Для снижения интрадуоденального давления и, таким образом, для улучшения оттока желчи необходимо обеспечить регулярный стул за счет достаточного потребления воды (которая необходима также и для гидрохолереза), растительных масел и пищевых волокон. Пищевые волокна понижают давление в двенадцатиперстной кишке и тем самым улучшают отток желчи в кишку. Основными представителями пищевых волокон являются неперевариваемые углеводы — целлюлоза (клетчатка), гемицеллюлоза, пектиновые вещества. Источники пищевых волокон — это фрукты, ягоды, овощи, отруби. Данные продукты обладают и другими лечебными свойствами: они ощелачивают желчь, содержат витамины С и Р, каротиноиды. Дефицит пищевых волокон, обусловленный употреблением в пищу рафинированных продуктов питания, способствует росту в цивилизованных странах заболеваемости желчнокаменной болезнью. Пищевые волокна способствуют размягчению кала, усиливают перистальтику кишечника, экскрецию холестерина с калом. При употреблении в пищу отрубей увеличивается количество первичных и уменьшается количество вторичных желчных кислот. Это объясняется влиянием пищевых волокон на бактериальную флору кишечника, которая участвует в дегидроксилировании первичных желчных кислот. Связывающая способность различных пищевых волокон по отношению к желчным кислотам неодинакова. Она особенно высока у фруктов (яблок, груш), ягод (малины), овощей (цветной капусты, моркови, картофеля, пастернака, зеленого горошка), пшеничных отрубей и хлеба из непросеянной муки.
Фрукты, ягоды и овощи являются источником природных антиоксидантов (витаминов С, Р, каротиноидов), роли которых в настоящее время придается большое значение.
Улучшить свойства желчи
Одним из направлений лечебного и профилактического питания при заболеваниях желчевыводящих путей, особенно при желчнокаменной болезни, является улучшение физико-химических свойств желчи за счет снижения содержания в ней холестерина, увеличения содержания желчных кислот и щелочности, уменьшения вязкости. В диете ограничивают продукты, богатые холестерином (субпродукты, желтки яиц, масло сливочное, сыры, икру). При этом общее содержание холестерина в рационе не должно превышать 300 мг/сут.
Ощелачивают желчь продукты, содержащие калий, магний, кальций (фрукты, овощи, молочные продукты), в то время как избыток мясных, крупяных и хлебобулочных изделий сдвигает рН желчи в кислую сторону. С целью уменьшения концентрации желчи показано обильное питье (количество жидкости в рационе — не менее 35 мл/кг идеальной массы тела), курсы питьевого лечения минеральными водами. Для профилактики слущивания эпителия желчных путей, который может стать центром кристаллизации желчи, необходимо адекватное поступление с пищей витамина А и его предшественников — каротиноидов. Следует отметить, что усвоение жирорастворимых витаминов при патологии гепатобилиарной системы у некоторых больных может быть нарушено из-за дефицита желчных кислот.
Не навреди!
С помощью диеты можно воздействовать на моторику желчного пузыря и функцию сфинктера Одди (гладкая мышца, располагающаяся в большом дуоденальном сосочке, находящемся на внутренней поверхности нисходящей части двенадцатиперстной кишки). Так, при наличии гипермоторной дискинезии желчного пузыря, спазме сфинктера Одди, нефункционирующем желчном пузыре показано ограничение жиров, яичных желтков, орехов и др. Полезно включать в рацион продукты, содержащие большое количество магния, который уменьшает спазм гладкой мускулатуры. Пищевые источники магния — это отруби пшеничные, гречка, пшено, арбуз, соя, крабы, морская капуста. Следует особо подчеркнуть плохую переносимость больными холодной пищи (мороженого, кефира из холодильника и др.), которая может вызывать спазм сфинктера Одди и боль, вплоть до развития приступа печеночной колики.
При гипотонии желчного пузыря рацион должен содержать продукты, обладающие холекинетическим действием. Традиционный совет врачей «Не ешьте жирного и жареного» часто приводит к развитию гипомоторной дискинезии желчного пузыря («ленивому» желчному пузырю).
При анализе фактических рационов питания пациентов с патологией билиарной системы нами наиболее часто выявлялись следующие ошибки:
Хотите больше информации по вопросам диетологии?
Приобретите информационно-практический журнал «Практическая диетология» в электронном или печатном формате!
© 2011-2022 «Практическая диетология». Все права защищены
Электронное периодическое издание «Практическая диетология» зарегистрировано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций 25 января 2013 г.
Свидетельство о регистрации ЭЛ № ФС 77 – 52586.
Как заставить печень «похудеть»?
Знаете ли вы, что 27% жителей России страдают ожирением печени? Не все из них принимают алкоголь, страдают от лишнего веса и ходят к врачам, как на работу.
В этой статье мы развенчаем мифы о жире в печени и расскажем, как не получить инфаркт или цирроз от незнания.
Когда жир накапливается в печени,а вы не знаете? Неочевидные факторы риска
Мало кто идет к врачу, чувствуя себя здоровым. Многие не идут, даже если есть симптомы. Поэтому ожирение печени выявляется чаще всего случайно, во время обследования по поводу других заболеваний.
Кому стоит поберечься? В группе риска по ожирению печени те,кто:
И все же, «чемпионы» по риску для печени — те, кто страдают ожирением. При этом состоянии в печень поступает больше свободных жирных кислот, и они откладываются в клетках печени в виде жира. Клетки теряют чувствительность к инсулину, которого становится все больше, происходит срыв, и развивается диабет.
Любите расслабиться с бокалом спиртного? Ожирение печени на горизонте
Алкоголь в процессе обмена превращается в жир, который накапливают клетки печени. Потом клетки переполняются жиром, не получают должного питания и гибнут. Это есть и причина цирроза у тех, кто «употребляет».
Что убивает пациента с нелеченым ожирением печени: инфаркт или цирроз?
Жировой гепатоз, как еще называют ожирение печени, сочетается с отложением жира на стенках артерий, и, как следствие, ускоряет развитие сердечно-сосудистых катастроф. Если ожирение печени не лечить, оно переходит в фиброз, когда вместо «рабочих лошадок» — клеток печени, образуется соединительная ткань, иначе говоря — рубец. Так постепенно развивается цирроз. И это последствия любви к сладкому, жирному, жестким диетам, «отдыху» с бокалом пива в руке или чего покрепче.
Но печень — удивительный орган, и процесс обратим, если вовремя начать уделять себе внимание.
Как избавиться от жира в печени? 5 правил поведения
К сожалению, «волшебной таблетки» от жирового гепатоза не существует. Только диета и физическая активность. Поэтому:
Как мы можем вам помочь?
Печень не болит, жир накапливается незаметно. Задумайтесь, пока не стало слишком поздно. Пройдите обследование и убедитесь, что все в порядке. А если проблема существует, не закрывайте на нее глаза и обратитесь за помощью. Мы готовы помочь.
Дюбаж печени с минеральной водой детям
Следить за своим здоровьем – это очень важно. Особенно если дело касается такого органа, как печень, которая отвечает за фильтрацию крови и выведение из организма токсинов, вредных веществ, шлаков. Касается это не только взрослых людей, но и детей, для которых очищение печени, то есть тюбаж или метод слепого зондирования тоже бывает очень полезен.
Вполне понятно, что проведение чистки печени детям требует выполнения особых правил, поскольку даже для взрослых данная процедура имеет ряд предостережений и противопоказаний. Так детям с самого раннего возраста можно проводить тюбаж (дюбаж) печени с минеральной водой, а как правильно использовать данную методику, мы рассмотрим прямо сейчас.
Как делать дюбаж печени с минеральной водой?
Главное правило, о котором нельзя забывать ни в коем случае, касается того, что любые процедуры, в том числе и очищение печени, нужно проводить только после тщательного обследования и консультации врача. И даже если дюбаж печени с минеральной водой детям делается по назначению педиатра и гастроэнтеролога, нужно четко придерживаться всех правил, рекомендаций и порядка проведения процедур.
Поскольку для организма ребенка сильнодействующие желчегонные препараты имеют определенные противопоказания, тюбаж печени должен проводиться только самыми безопасными и щадящими средствами. Лечебная минеральная вода в этом случае подходит как нельзя лучше, и использовать её можно для чистки печени детям самого раннего возраста.
Как проводится дюбаж печени?
Дюбаж печени с минеральной водой должен проводиться с утра, натощак. При этом бутылка лечебной минеральной воды («Боржоми», «Ессентуки №4 или №17», «Нарзан») должна быть открыта с вечера, чтобы за ночь полностью избавиться от газов. Воду следует хорошо нагреть и дать ребенку выпить 50-200 мл, в зависимости от возраста. Учитывая советы медиков проводить процедуру необходимо 1-2 раза в неделю.
Чтобы выведению желчи ничего не препятствовало, нужно знать, как правильно вести себя во время процедуры. Во-первых, воду проследить, чтобы ребенок пил воду не спеша, маленькими глотками.
Затем нужно уложить малыша на правый бок и положить ему под подреберье горячую грелку. Ноги необходимо согнуть в коленях и постараться максимально расслабиться. В таком положении ребенок должен находиться не менее 40-60 минут.
Если почитать отзывы родителей, которые уже применяли способ дюбажа печени с минеральной водой для своих малышей, то все сомнения по поводу пользы такой процедуры отпадают. Но в тоже время дети неохотно соглашаются лежать тихонько целый час, испытывая при этом не совсем приятные ощущения. Поэтому родители должны постараться в течение всей процедуры развлекать свое чадо, чтобы не давать ему вертеться и менять нужное положение.
В прошествии положенного срока нужно чтобы ребенок медленно встал, сделал несколько глубоких вдохов и выполнил несложную утреннюю зарядку – приседания и наклоны. После этого можно приступать к легкому завтраку, который должен состоять из каши и яблочного или морковного сока.
Описторхоз в клинической практике врача-инфекциониста
Рассмотрены распространение, патогенез, клиническая картина описторхоза, формы заболевания, методы лабораторной диагностики и подходы к лечению пациентов, а также применяемые препараты и меры по контролю эффективности терапии.
Propagation, pathogenesis, clinical picture of opistorchosis, are examined, as well as forms of disease, methods of laboratory diagnostics and approaches to the treatment of patients, and also applied preparations and the measures to control the therapy efficiency.
Описторхоз — внекишечный природно-очаговый биогельминтоз, вызываемый трематодами из семейства Opisthorchidae, характеризующийся полиморфизмом клинических проявлений, обусловленных паразитированием этих гельминтов в желчных протоках печени и протоках поджелудочной железы и длительным течением.
История изучения и распространение описторхоза
Возбудитель описторхоза был открыт и описан S. Rivolta в 1884 г. у кошек и назван Opisthorchis (Distomum) felineus. В 1891 г. профессор Томского университета К. Н. Виноградов при вскрытии трупа человека обнаружил подобного же гельминта, подробно описал его и назвал Distomum sibiricum (сибирская двуустка) [4]. В 1894 г. M. Braun доказал идентичность Distomum felineum Rivolta (1884 г.) и Distomum sibiricum Winogradov (1891 г.) [1, 2].
Описторхоз занимает доминирующее место в краевой инфекционной патологии Западной Сибири, где существует самый напряженный в мире очаг этой инвазии. В низовьях Иртыша и среднего течения Оби пораженность местного населения достигает 70–80% и даже 90% [1].
Очаги описторхоза расположены также в бассейнах рек Днестра, Немана, Волги, Днепра. Имеются данные о наличии очагов с низким уровнем экстенсивности в притоках Енисея, в бассейне Урала, Северной Двины и Бирюсы. За рубежом очаги описторхоза зарегистрированы в Италии, Германии, Франции, Болгарии и других странах [1].
Жизненный цикл паразита
Описторхисы относятся к классу трематод, семейству Opisthorchidae. O. felineus — плоский гельминт ланцетовидной формы, длиной 4–20 мм и шириной 1–4 мм. Яйца описторхисов с уже сформированными личинками выделяются с фекалиями во внешнюю среду, и дальнейшее развитие происходит в пресноводных водоемах, где обитает промежуточный хозяин описторхисов — пресноводные моллюски Codiella inflata и Codiella troscheli. Моллюск с пищей заглатывает яйцо, из которого выходят мирацидии, превращающиеся в спороцисту, редию и хвостатую личинку — церкария. Церкарий покидает тело моллюска, выходит в водоем и в силу хемо- и фототаксиса прикрепляется к телу своего дополнительного хозяина — рыбы семейства карповых. К семейству карповых относится 23 вида рыб (язь, лещ, карп, чебак, елец, линь, красноперка, сазан, пескарь и др.). Проникшие в мышечную и соединительную ткань рыбы церкарии инцистируются и превращаются в метацеркарий. Метацеркарии достигают инвазионной стадии через 6 недель. В организм окончательного хозяина — человека и животных — метацеркарии попадают при употреблении в пищу инвазированной необезвреженной рыбы. Круг дефинитивных хозяев паразита насчитывает 34 вида рыбоядных млекопитающих (кошка, собака, свинья, лисица, волк, корсак, песец, бурый медведь, росомаха, хорь, бобр и др.). В желудке окончательного хозяина происходит переваривание наружной капсулы, а под действием дуоденального сока метацеркарии освобождаются от своей внутренней оболочки и через ампулу дуоденального сосочка мигрируют в общий желчный проток и внутрипеченочные желчные протоки. У 20–40% зараженных лиц описторхисы также обнаруживаются и в протоках поджелудочной железы, куда они проникают по вирсунгову протоку [3]. Проникшие в гепатобилиарную систему и поджелудочную железу метацеркарии через 3–4 нед достигают половой зрелости и начинают продуцировать яйца. Число паразитов у одного человека может быть от единиц до десятков тысяч. Весь цикл развития описторхиса от яйца до половозрелой стадии длится 4–4,5 мес.
Патогенез
В патогенезе описторхоза, как и многих других гельминтозов, прослеживается 2 фазы: ранняя и поздняя. Ранняя фаза, или острый описторхоз, длится от нескольких дней до 4–8 и более недель и связана с проникновением эксцистированных метацеркариев паразита в гепатобилиарную систему и поджелудочную железу. Поздняя фаза или хронический описторхоз продолжается многие годы.
Молодые описторхисы повреждают стенки желчных протоков своими шипиками, а половозрелые — присосками, отрывая эпителий желчных протоков, которым они питаются, чем определяется развитие множественных кровоточащих эрозий и бурной регенеративно-гиперпластической реакции эпителия. Это эволюционно сформировавшееся качество описторхисов, направленное на создание оптимальных условий для их жизнедеятельности и поддержание вида. В условиях этого процесса чрезвычайно велика возможность мутации, что в сочетании с иммуносупрессорным влиянием описторхисов значительно повышает риск канцерогенеза [4]. Скопление в желчных и панкреатических протоках гельминтов, их яиц, слизи, слущенного эпителия создает препятствие для оттока желчи и секрета, что способствует развитию пролиферативного холангита и каналикулита поджелудочной железы, сопровождающихся различной степенью фиброза этих органов.
Механическое раздражение стенок желчных протоков печени и панкреатических протоков приводит к развитию патологических висцеро-висцеральных рефлексов, ведущих к нарушению моторной и секреторной функции органов желудочно-кишечного тракта.
Альтеративные изменения в органах локализации и других органах обусловлены и влиянием продуктов метаболизма описторхисов, которые преодолевают эпителиальный барьер и поступают в кровеносное русло, оказывая токсическое воздействие на организм человека.
Пролиферативные процессы в желчных протоках, а также сами гельминты, слизь, слущенный эпителий, создают условия для развития желчной гипертензии, способствуют формированию дискинезии желчевыводящих путей, стазу желчи, созданию благоприятных условий для развития вторичной инфекции (кишечная палочка, стафилококки, дрожжеподобные грибки и различные микробные ассоциации).
Клиническая картина заболевания
Клиническая картина описторхоза полиморфна и варьирует от бессимптомных форм до тяжелых проявлений, обусловленных развитием гнойного холангита, абсцесса печени и др.
Общепризнанной классификации описторхоза не существует. Выделяют раннюю фазу (острый описторхоз) и позднюю (хронический описторхоз). Острый описторхоз длится от нескольких дней до 4–8 и более недель и связан с проникновением личинок паразита в гепатобилиарную систему и поджелудочную железу. В ранней фазе описторхоза ведущим звеном в патогенезе является развитие аллергических реакций и органных поражений в ответ на воздействие продуктов метаболизма паразита. В патогенезе хронической стадии описторхоза большую роль играют повторные заражения с обострением воспалительного процесса, фиброзом билиарных путей, поджелудочной железы, дистрофией паренхимы печени, дискинезией желчевыводящих путей, холестазом. Хронический описторхоз продолжается многие годы.
Инкубационный период равняется в среднем 2–3 нед.
Клинические варианты острого описторхоза разнообразны — от латентных до генерализованных аллергических реакций с множественными поражениями.
В эндемичных по описторхозу очагах у коренных жителей и у длительно проживающих в течение нескольких поколений местных жителей чаще не выявляется клинически выраженная острая фаза болезни, в то время как у вновь прибывших из благополучных по описторхозу местностей острая фаза описторхоза наблюдается почти всегда. Причина этого явления заключается в том, что у аборигенов (иммунное население) формируется иммунологическая толерантность супрессорного типа. Иммунологическая толерантность к описторхозному антигену формируется в связи с поступлением описторхозного антигена в организм на ранних стадиях эмбриогенеза. После рождения уже зрелый организм воспринимает этот антиген как «свое» [5, 6].
Инаппарантная (субклиническая) форма описторхоза выявляется случайно, когда при исследовании периферической крови отмечается большая эозинофилия.
При клинически выраженном остром описторхозе у больных наблюдается лихорадка — от субфебрильной до фебрильной длительностью от 3–4 дней до нескольких недель, интоксикационный синдром, умеренные артралгии и миалгии, экзантема различного характера, гепатобилиарный синдром: боли в правом подреберье (тупые, ноющие, давящие, жгучие), желтуха — от субиктеричности до интенсивной, кожный зуд, гепатомегалия, у части больных выявляются положительные пузырные симптомы. Характерны симптомы диспепсического характера (тошнота, рвота, изжога). Более чем у 80% больных выявляется цитолитический синдром с повышением активности аминотрансфераз (аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ)) в 2–7 раз по сравнению с нормой, часто холестаз (повышение уровня гамма-глутамилтранспептидазы (ГГТП) и щелочной фосфатазы (ЩФ)), развивается мезенхимально-воспалительный печеночный синдром [7]. Одним из проявлений острого описторхоза может быть бронхолегочный синдром: катаральные проявления со стороны верхних дыхательных путей (гиперемия зева, зернистость задней стенки глотки, насморк), астматоидный бронхит, эозинофильные инфильтраты в легких и экссудативные плевриты [8]. Реже наблюдается гастроэнтероколитический синдром, характеризующийся субфебрильной лихорадкой, умеренно выраженный интоксикацией и преобладанием симптомов поражения желудочно-кишечного тракта (боли в эпигастрии, изжога, тошнота, рвота, частый жидкий стул, иногда с примесью слизи).
Описанные синдромы острой фазы описторхоза не исчерпывают всего разнообразия клиники этого гельминтоза, и при любом варианте общие и локальные симптомы тесно переплетаются, что обусловливает полиморфизм клинических проявлений и индивидуальную неповторимость этих сочетаний у каждого больного.
У больных в острую фазу описторхоза могут развиваться и очень тяжелые токсико-аллергическиие проявления, такие как острый эпидермальный некролиз (синдром Лайелла), синдром Стивена–Джонсона, острый миокардит, отек Квинке, крапивница.
Большое значение для диагностики острого описторхоза имеет исследование периферической крови. У всех больных наблюдается лейкоцитоз до 20–60 × 10 9 л, умеренно повышенная скорость оседания эритроцитов (СОЭ) и эозинофилия — 20–40%, иногда до 90%.
С переходом заболевания в хроническую фазу симптоматика существенно изменяется и характеризуется, прежде всего, устранением лихорадки и нормализацией гематологических показателей.
Латентное течение описторхоза чаще наблюдается у коренного и местного населения в очагах этой инвазии, а также нередко у лиц молодого возраста, инвазированных описторхисами.
Проявления клинически выраженного хронического описторхоза неспецифичны, полиморфны и не укладываются в какой-либо один синдром. Холангит при описторхозе является абсолютно обязательным звеном патогенеза. Некоторые исследователи [7, 9] не относят желчный пузырь к числу органов постоянного пребывания описторхисов и считают, что паразиты в желчный пузырь попадают случайно с током желчи. Учитывая функционально-морфологические связи внутрипеченочных желчных протоков и желчного пузыря, сочетанное поражение этих органов у больных описторхозом наблюдается очень часто, и синдромы холангита и холецистита относится к наиболее распространенным (80–87% случаев) [7, 9]. Проявления этих синдромов зависят от длительности и интенсивности инвазии. Так, в первые 3 года после заражения у 86% больных наблюдается гиперкинетический тип дискинезии желчевыводящих путей, у 11% — нормокинетический и у 3% — гипокинетический. Спустя 5–7 лет в 87% случаев выявляется гипокинетический тип дискинезии, в 6% — нормокинетический, в 7% — гиперкинетический [9]. У 50–85% больных отмечается гепатомегалия, у 30–40% — положительные пузырные симптомы [7].
У 13–17% больных хроническим описторхозом наблюдается гепатит, основными проявлениями которого являются боли в правом подреберье, тошнота, рвота, отрыжка, артралгии, нередко — кожный зуд, гепатомегалия, при обострении развивается желтуха различной интенсивности [7–9].
У части больных развивается панкреатит, отличающийся волнообразным течением с частой сменой периодов обострений и ремиссий, и редко наблюдается прогрессирующее течение [10]. Чаще всего панкреатит протекает в виде болевой формы. Редкими формами панкреатита являются хронический псевдоопухолевый панкреатит и описторхозные кисты поджелудочной железы.
У больных описторхозом отмечаются и поражения органов, не являющихся местом постоянной локализации возбудителя. Так, у 45–50% больных описторхозом отмечаются различные формы гастродуоденальной патологии (гастриты, дуодениты, язвенная болезнь желудка и двенадцатиперстной кишки) [10–11]. Поражение кишечника у больных хроническим описторхозом отмечается довольно часто, и основным его проявлением является кишечная диспепсия. При изучении состава микрофлоры фекалий у них выявляется дисбактериоз, который характеризуется отсутствием или резким снижением количества бифидобактерий, уменьшением количества эшерихий, нередко в сочетании с угнетением их ферментативных свойств, и повышенным содержанием факультативной условно-патогенной микрофлоры (S. epidermidis, S. aureus и др.) [7].
Изменения со стороны сердечно-сосудистой системы проявляются сердцебиениями, болями в области сердца, наклонностью к гипотонии, диффузными дистрофическими изменениями миокарда по данным электрокардиографии (ЭКГ).
Описторхозная инвазия может приводить к нарушению деятельности центральной и вегетативной нервной системы, о чем свидетельствуют частые жалобы больных на повышенную утомляемость, раздражительность, бессонницу, головную боль, головокружение [3, 9]. Наблюдаются признаки лабильности вегетативной нервной системы: потливость (часто локальная — потные руки), слюнотечение, выраженный дермографизм, тремор век, языка, пальцев рук, проявления вазомоторных сосудистых реакций, субфебрильная температура. В ряде случаев неврологическая симптоматика выступает на первый план, и больным ставят диагноз нейроциркуляторной дистонии, вегетативного невроза и т. д.
Аллергический синдром при хроническом описторхозе может проявляться кожным зудом, крапивницей, рецидивирующим отеком Квинке, артралгией, пищевой аллергией, умеренной эозинофилией.
Лабораторная диагностика
Лечение
При назначении лечения больным описторхозом необходимо учитывать фазу болезни, вариант ее течения с учетом всех клинических синдромов, степень тяжести и особенности организма (возраст, сопутствующие заболевания и т. д.), возможность супер- и реинвазии.
Лечение описторхоза включает 3 этапа.
1-й этап — подготовительная патогенетическая терапия, направленная на обеспечение должного оттока из желчевыводящих путей и протоков поджелудочной железы; восстановление моторно-кинетической функции желчевыделительной системы; купирование аллергического, интоксикационного синдромов, воспалительных процессов в желчевыводящих путях и желудочно-кишечном тракте.
В качестве противоаллергических средств рекомендуется применение блокаторов Н1-гистаминовых рецепторов, которые назначаются во время курса подготовительной патогенетической терапии, при проведении этиотропной терапии и по показаниям — в период реабилитации.
При наличии воспалительных процессов в желчевыводящих путях показаны коротким курсом (чаще всего 5-дневным) антибиотики широкого спектра действия.
Желчегонная и спазмолитическая терапия должна осуществляться дифференцированно, с учетом типа дискинезии желчевыводящих путей в течение 1–3 месяцев.
Классификация желчегонных препаратов
I. Препараты, стимулирующие желчеобразовательную функцию печени — истинные желчегонные (холеретики):
II. Препараты, стимулирующие желчевыведение:
Из спазмолитических средств можно использовать традиционные препараты (Но-шпа, дротаверин, Бускопан), но предпочтительнее применение селективных препаратов (мебеверина гидрохлорид (Дюспаталин)), ввиду их преимуществ селективности в отношении желудочно-кишечного тракта, отсутствия побочных эффектов; двойного механизма действия (снижение тонуса и уменьшение сократительной активности гладкой мускулатуры), высокой тропности к сфинктеру Одди.
При явлениях холестаза назначаются препараты урсодезоксихолевой кислоты (Урсофальк, Урсосан), Гептрал.
По показаниям применяются прокинетики (метоклопрамид, домперидон — Мотилиум, Мотилак), ферментные препараты (Мезим форте, Креон, Панкреофлат, Пензитал и др.), пре- и пробиотики, средства эрадикационной терапии
Показано физиотерапевтическое лечение (микроволновая терапия, магнитотерапия, электрофорез с 10% раствором сернокислой магнезии), оказывающее спазмолитическое, десенсибилизирующее, микроциркуляторное действия.
2-й этап лечения описторхоза предусматривает проведение специфической химиотерапии. В настоящее время эффективным средством специфической терапии описторхоза является празиквантел. Фармакокинетика празиквантела и его аналогов связана с повышением проницаемости клеточных мембран паразитов для ионов кальция, сокращением мускулатуры паразитов, переходящим в спастический паралич. Препараты празиквантела назначаются из расчета 50–60 мг на 1 кг массы тела больного в 3 приема с интервалом между приемами 4–6 часов. А. И. Пальцев [6] предлагает щадящую методику применения празиквантела, когда указанная суточная доза делится на двое суток. При щадящей методике применения празиквантеля курсовую дозу делят на 6 приемов в течение 2 сут: 3 приема в первые сутки с интервалом 4 ч и 3 — на вторые сутки. По данным автора, антигельминтная эффективность при этом остается такой же.
Противопоказаниями к приему препаратов празиквантела являются повышенная чувствительность к препарату, цистицеркоз глаз и печени, первый триместр беременности, лактация, детский возраст до 4 лет, печеночная недостаточность.
Необходимо отметить, что наличие описторхоза не является абсолютным показанием к дегельминтизации. Например, ее нужно назначать с осторожностью лицам пожилого и старческого возраста. Назначение антигельминтиков больным с тяжелой сопутствующей патологией (декомпенсированные пороки сердца, тяжелые поражения почек и печени и др.) также должно проводиться с известной осторожностью. Лечение препаратами празиквантела рекомендуется начинать не ранее 3-й недели от начала болезни и при уровне эозинофилии не более 20%.
После приема препарата могут возникать побочные явления: головная боль, головокружение, слабость, нарушение координации, тошнота, усиление или возобновление болей в правом подреберье. В большинстве случаев побочные реакции кратковременны и исчезают в течение суток. В части случаев в первые 2–3 недели после лечения больные отмечают общую слабость, усиление болей в животе и диспептических проявлений, возможно появление эозинофилии, ухудшение показателей функциональных проб печени, высыпания на коже типа крапивницы. Эти симптомы обусловлены в основном дополнительным антигенным воздействием в результате гибели гельминтов.
На 2-й день после приема празиквантела назначают дуоденальное зондирование или слепое зондирование с минеральной водой, сорбитом, ксилитом для эвакуации продуктов жизнедеятельности и распада описторхисов. Для увеличения пассажа желчи можно рекомендовать электростимуляцию правого диафрагмального нерва, импульсное магнитное поле.
3-й этап лечения — реабилитационная патогенетическая терапия, направленная на максимальное выведение продуктов жизнедеятельности и распада паразитов: желчегонная терапия, адекватная типу дискинезии желчевыводящих путей, беззондовое дуоденальное зондирование (тюбажи с ксилитом, сорбитом, сернокислым магнием, минеральной водой) 2–3 раза в течение 1-й недели, далее 1–2 раза в неделю (до 3 мес), сорбенты (Лактофильтрум, Энтеросгель, Полифепан и др.), пре- и пробиотики — для восстановления биоценоза кишечника.
При усилении аллергических реакций, интоксикационного синдрома, связанных с дополнительным антигенным воздействием при гибели гельминтов, требуется назначение десенсибилизирующей (антигистаминные препараты, при необходимости — глюкокортикоиды) и дезинтоксикационной (инфузии растворов, сорбенты) терапии.
Комплекс реабилитационных мероприятий включает также прием гепатопротекторов, отваров желчегонных трав в течение 3–4 месяцев (табл.), по показаниям применяют спазмолитики, антихолестатические препараты и другие патогенетические средства.
Контроль эффективности дегельминтизации проводится через 1, 3 и 6 месяцев после лечения: выполняются гельминтоовоскопические исследования фекалий не менее 3 раз в каждый из указанных сроков и исследование дуоденального содержимого. Необходимо подчеркнуть, что паразитологическое выздоровление далеко не всегда сопровождается клиническим выздоровлением: у лиц, страдавших описторхозом более 5 лет, жалобы и объективные изменения, имевшие место в период хронической фазы, сохраняются [4, 6]. Объясняется это наличием глубоких морфологических изменений в органах, сформировавшихся в хроническую фазу болезни. Вопрос же о тактике лечения резидуальных форм описторхоза остается до сих пор нерешенным.
Литература
ГБОУ ВПО НГМУ МЗ РФ, Новосибирск
Желтухи у новорожденных
Желтуха, или визуальное проявление гипербилирубинемии, включает синдромы различного происхождения, общей чертой которых является желтушное прокрашивание кожи и слизистых оболочек. Всего насчитывается около 50 заболеваний, которые сопровождаются появление
Желтуха, или визуальное проявление гипербилирубинемии, включает синдромы различного происхождения, общей чертой которых является желтушное прокрашивание кожи и слизистых оболочек. Всего насчитывается около 50 заболеваний, которые сопровождаются появлением желтушности кожных покровов. У взрослых прокрашивание кожи происходит при повышении уровня билирубина более 34 мкмоль/л, у новорожденных — при уровне билирубина от 70 до 120 мкмоль/л.
Желтухи периода новорожденности, обусловленные накоплением в крови избыточного количества билирубина, встречаются часто и иногда требуют проведения неотложных лечебных мероприятий. Непрямой билирубин является нейротоксическим ядом и при определенных условиях (недоношенность, гипоксия, гипогликемия, длительная экспозиция и т. д.) вызывает специфическое поражение подкорковых ядер и коры головного мозга — так называемую билирубиновую энцефалопатию. По различным данным, на первой неделе жизни желтуха встречается у 25–50% доношенных и у 70–90% недоношенных новорожденных.
Билирубин является конечным продуктом катаболизма гема и образуется преимущественно вследствие распада гемоглобина (около 75%) с участием гемоксигеназы, биливердинредуктазы, а также неферментных восстанавливающих веществ в клетках ретикулоэндотелиальной системы (РЭС). Другими источниками билирубина являются миоглобин и гемсодержащие ферменты печени (около 25%).
Естественный изомер билирубина — непрямой свободный билирубин — хорошо растворим в липидах, но плохо растворим в воде. В крови он легко вступает в химическую связь с альбумином, образуя билирубин-альбуминовый комплекс, благодаря чему в ткани поступает только менее 1% образующегося билирубина. Теоретически одна молекула альбумина может связать две молекулы билирубина. В комплексе с альбумином билирубин попадает в печень, где он путем активного транспорта проникает в цитоплазму, связывается с Y- и Z-протеинами и транспортируется в эндоплазматический ретикулум. Там под влиянием уридиндифосфатглюкуронилтрансферазы (УДФГТ) происходит соединение молекул билирубина с глюкуроновой кислотой и образуется моноглюкуронидбилирубин (МГБ). При транспортировке МГБ через цитоплазматическую мембрану в желчные капилляры происходит присоединение второй молекулы билирубина и образуется диглюкуронидбилирубин (ДГБ). Конъюгированный билирубин является водорастворимым, нетоксичным и выводится из организма с желчью и мочой. Далее билирубин в виде ДГБ экскретируется в желчные капилляры и выводится вместе с желчью в просвет кишечника. В кишечнике под влиянием кишечной микрофлоры происходит дальнейшая трансформация молекул билирубина, в результате которой образуется стеркобилин, выводящийся с калом.
Практически все этапы билирубинового обмена у новорожденных характеризуются рядом особенностей: относительно большее количество гемоглобина на единицу массы тела, умеренный гемолиз эритроцитов даже в нормальных условиях, даже у здорового доношенного новорожденного ребенка содержание Y- и Z-протеинов, а также активность УДФГТ резко снижены в первые сутки жизни и составляют 5% от активности таковых систем у взрослых. Повышение концентрации билирубина приводит к повышению активности ферментных систем печени в течение 3–4 дней жизни. Полное становление ферментных систем печени происходит к 1,5–3,5 мес жизни. Морфофункциональная незрелость, эндокринные расстройства (гипотиреоз, повышение в женском молоке прогестерона), нарушения углеводного обмена (гипогликемия), наличие сопутствующей инфекционной патологии существенно удлиняют сроки становления ферментных систем печени. Процессы выведения билирубина из организма также несовершенны, с чем связана повышенная кишечная реабсорбция билирубина. Заселение кишечника новорожденного нормальной кишечной микрофлорой резко сокращает количество билирубина, всасываемого из кишечника, и способствует нормализации процессов его выведения из организма.
Все желтухи принято делить по уровню блока билирубинового обмена:
В практике неонатолога используется патогенетическая классификация желтух новорожденных (по Н. П. Шабалову, 1996), согласно которой выделяют:
На патологический характер желтухи всегда указывают следующие признаки: появление желтухи в первые сутки жизни, уровень билирубина более 220 мкмоль/л, почасовой прирост билирубина более 5 мкмоль/л в час (более 85 мкмоль/л в сутки), длительность ее более 14 дней, волнообразное течение заболевания, появление желтухи после 14-го дня жизни.
Наиболее частой причиной конъюгационных гипербилирубинемий у новорожденных является несоответствие между нормальной продукцией билирубина и несовершенной системой его выведения из организма вследствие незрелости ферментных систем печени. Для конъюгационной желтухи характерно появление ее на 3-и сутки жизни, отсутствие увеличения печени и селезенки, изменений в окраске стула и мочи, анемического симптомокомплекса.
Для транзиторной гипербилирубинемии новорожденных характерно появление желтухи в возрасте более 36 ч жизни. Почасовой прирост билирубина не должен превышать 3,4 мкмоль/л ч (85,5 мкмоль в сутки). Наибольшая интенсивность желтушного прокрашивания кожи приходится на 3–4-е сутки, при этом максимальный уровень билирубина не поднимается выше 204 мкмоль/л. Для транзиторной гипербилирубинемии характерно прогрессирующее снижение уровня билирубина и интенсивности желтухи после 4 сут и угасание ее к 8–10-м суткам. Общее состояние ребенка при этом не нарушается. Лечение не требуется.
Для желтухи недоношенных новорожденных характерно более раннее начало (1–2-е сутки жизни), что создает трудности при дифференциации ее с гемолитической болезнью новорожденных. Однако данные анамнеза (группа крови матери и ребенка, отсутствие сенсибилизации) и лабораторных исследований (нормальный уровень гемоглобина, эритроцитов, отсутствие ретикулоцитоза) помогают поставить правильный диагноз. Длительность конъюгационной желтухи у недоношенных — до 3 нед.
В 1963 г. И. М. Ариасом была описана «желтуха от материнского молока» (прегнановая желтуха) у детей, находящихся на грудном вскармливании. Патогенез этого вида желтухи до конца не выяснен. Однако считается, что ее причиной является низкая конъюгация билирубина, являющаяся следствием тормозящего влияния прегнандиола, который содержится в избыточном количестве в крови некоторых женщин в послеродовом периоде, а также пониженная экскреция билирубина. Длительность желтухи составляет от 3 до 6 нед. Диагностическим тестом является отмена грудного вскармливания на 2–3-и сутки, на фоне чего желтуха начинает быстро разрешаться. При возобновлении вскармливания грудью уровень билирубина снова начинает расти.
Синдром Жильбера (конституциональная печеночная дисфункция) — наследственное заболевание, наследуемое по аутосомно-доминантному типу. Частота в популяции составляет 2–6%. Причиной является наследственное нарушение конъюгации непрямого билирубина вследствие нарушения захвата последнего печеночной клеткой. У новорожденных заболевание имеет сходство с транзиторной желтухой. Случаев ядерной желтухи не описано. Прогноз благоприятный. Диагноз ставится на основании семейного анамнеза, длительно сохраняющейся гипербилирубинемии при отсутствии других патологических изменений. Назначение фенобарбитала приводит к резкому уменьшению желтушности, что также свидетельствует о наличии данного заболевания.
Наследуемое нарушение пигментного обмена при синдроме Криглера–Найяра обусловлено отсутствием (I тип) или очень низкой активностью (II тип) глюкуронилтрансферазы в клетках печени.
При синдроме Криглера–Найяра I типа заболевание наследуется по аутосомно-рецессивному типу. Характерна интенсивная желтуха с первых дней жизни с повышением уровня непрямого билирубина сыворотки крови в 15–50 раз выше нормы, полным отсутствием прямой фракции билирубина. При естественном течении заболевания в большинстве случаев происходит прокрашивание ядер мозга, может отмечаться летальный исход. Назначение фенобарбитала неэффективно. Единственным способом лечения являются проведение фототерапии и трансплантация печени.
При II типе заболевания, которое наследуется по аутосомно-доминантному типу, наряду с менее интенсивной желтухой и уровнем непрямого билирубина в 15–20 раз больше нормы, в крови определяется прямая фракция билирубина. Отличительной чертой является положительный ответ на назначение фенобарбитала. Прогностически синдром Криглера–Найяра II типа более благоприятный. Развитие билирубиновой энцефалопатии наблюдается крайне редко.
Первым симптомом наследственно обусловленных нарушений обмена веществ, таких, как галактоземия, фруктоземия, тирозинемия и др., также может быть желтуха, имеющая конъюгационный характер. В первую очередь врача должно насторожить сочетание затяжной желтухи с такими симптомами, как рвота, диарея, гепатомегалия, прогрессирующая гипотрофия, тяжелая неврологическая симптоматика в виде судорог, мышечной гипотонии, парезов, параличей, атаксии, развитие катаракты, задержки нервно-психического развития. Диагноз подтверждается наличием галактозы в моче, позитивными пробами на сахар и другими специальными методами выявления нарушения обмена веществ в каждом отдельном случае.
Желтуха при гипотиреозе отмечается у новорожденных в зависимости от степени недостаточности функции щитовидной железы и сочетается с другими симптомами заболевания, такими, как крупный вес при рождении, выраженный отечный синдром, низкий тембр голоса новорожденного, ранние и упорные запоры и др. В биохимическом анализе крови наряду с непрямой гипербилирубинемией отмечается повышение холестерина. Скрининг-тест на гипотиреоз положительный, в крови повышен уровень тиреотропного гормона при снижении Т4. Длительная (от 3 до 12 нед) желтуха при гипотиреозе обусловлена замедлением всех метаболических процессов, в том числе и созревания глюкуронилтрансферазных систем печени. Своевременная постановка диагноза (в течение первого месяца жизни) и назначение заместительной терапии тиреоидином или L-тироксином приводят к нормализации билирубинового обмена.
Желтуха при полицитемии (диабетической фетопатии) обусловлена задержкой созревания ферментных систем печени на фоне гипогликемии при повышенном гемолизе. Контроль и коррекция гипогликемии, назначение индукторов микросомальных ферментов печени способствуют нормализации обмена билирубина.
Желтуха при пилоростенозе и высокой кишечной непроходимости обусловлена как нарушением конъюгирующих систем печени вследствие обезвоживания и гипогликемии, так и повышенным обратным всасыванием билирубина из кишечника. В данной ситуации лишь устранение пилоростеноза и обструкции кишечника приводят к нормализации пигментного обмена.
Применение лекарственных средств (глюкокортикоиды, некоторые виды антибиотиков и др.) может приводить к резкому нарушению процессов конъюгации в печени вследствие конкурентного вида метаболизма вышеуказанных препаратов. В каждом конкретном случае необходим анализ терапевтических мероприятий, а также знание метаболических особенностей препаратов, назначаемых новорожденному.
Для всех гемолитических желтух характерно наличие симптомокомплекса, включающего желтуху на бледном фоне (лимонная желтуха), увеличение печени и селезенки, повышение в сыворотке крови уровня непрямого билирубина, разной степени тяжести нормохромную анемию с ретикулоцитозом. Тяжесть состояния ребенка всегда обусловлена не только билирубиновой интоксикацией, но и выраженностью анемии.
Гемолитическая болезнь новорожденных возникает в результате несовместимости крови матери и ребенка по резус-фактору, его подтипам или группам крови. Заболевание протекает в виде отечной, желтушной и анемической форм. Отечная форма наиболее тяжелая и проявляется врожденной анасаркой, выраженной анемией, гепатоспленомегалией. Как правило, такие дети нежизнеспособны. Желтушная и анемическая формы заболевания более благоприятны, но также могут представлять угрозу здоровью ребенка. При легком течении уровень гемоглобина в пуповинной крови составляет более 140 г/л, уровень непрямого билирубина в сыворотке крови менее 60 мкмоль/л. В этом случае достаточно проведения консервативной терапии. При гемолитической болезни новорожденных средней степени тяжести и тяжелом течении может потребоваться проведение операции заменного переливания крови. В клинической картине желтуха либо врожденная, либо появляется в течение первых суток жизни, имеет бледно-желтый (лимонный) оттенок, неуклонно прогрессирует, на фоне чего может появляться неврологическая симптоматика билирубиновой интоксикации. Всегда отмечается гепатоспленомегалия. Изменения цвета кала и мочи нехарактерно.
Поражение структур центральной нервной системы (ЦНС) происходит при повышении уровня непрямого билирубина в сыворотке крови у доношенных новорожденных выше 342 мкмоль/л.
Для недоношенных детей этот уровень колеблется от 220 до 270 мкмоль/л, для глубоконедоношенных — от 170 до 205 мкмоль/л. Однако необходимо помнить, что глубина поражения ЦНС зависит не только от уровня непрямого билирубина, но и от времени его экспозиции в тканях головного мозга и сопутствующей патологии, усугубляющей тяжелое состояние ребенка.
Профилактические мероприятия для предупреждения развития гемолитической болезни новорожденных, которые должны проводиться уже в женской консультации, заключаются в постановке на учет всех женщин с резус-отрицательной и с 0(I) группой крови, выяснении данных анамнеза в плане наличия фактора сенсибилизации, определении уровня резус-антител и при необходимости проведении досрочного родоразрешения. Всем женщинам с резус-отрицательной кровью в первый день после родов показано введение анти-D-глобулина.
При развитии гемолитической болезни новорожденному проводится заменное переливание крови, в дооперационном периоде применяют фото- и инфузионную терапию.
Наследственные гемолитические анемии отличаются большим разнообразием. Самая распространенная из них — микросфероцитарная гемолитическая анемия Минковского–Шоффара. Дефектный ген локализован в 8-й паре хромосом. Результатом мутации является продукция аномальных эритроцитов, имеющих сферическую форму и меньшие (менее 7 нм) размеры, подвергающихся избыточному разрушению в криптах селезенки. Для анамнеза характерно наличие в семье родственников с аналогичным заболеванием. Диагноз подтверждается обнаружением микросфероцитарных эритроцитов, сдвигом кривой Прайс–Джонса влево, снижением осмотической стойкости эритроцитов, изменением индекса сферичности и средней концентрации гемоглобина в эритроцитах. Заболевание протекает волнообразно, гемолитические кризы сопровождаются повышением температуры тела, снижением аппетита и рвотами. Кризы провоцируются, как правило, острыми вирусными заболеваниями, переохлаждением, назначением сульфаниламидов и т. д. Основным методом лечения считается спленэктомия.
В период новорожденности может выявляться еще один вид наследственной гемолитической анемии, характеризующийся изменением формы эритроцитов — так называемый инфантильный пикноцитоз. Первые признаки заболевания появляются на первой неделе жизни и чаще у недоношенных детей. Эритроциты в окрашенном мазке крови имеют шиповидные отростки. Помимо анемии выявляются также отеки и тромбоцитоз. Назначение витамина Е в дозе 10 мг/кг в сутки приводит в большинстве случаев к клинико-лабораторной ремиссии.
При исследовании мазка крови у новорожденных могут быть выявлены и мишеневидные эритроциты, что характерно для гемоглобинопатий (талассемия, серповидно-клеточная анемия). Серповидно-клеточная анемия встречается чаще у жителей Средней Азии, Азербайджана и Армении и проявляется в неонатальном периоде только у гомозиготных носителей s-гемоглобина.
Диагноз наследственных энзимопенических анемий (дефицит глюкозо-6-фосфатдегидрогеназы, пируваткиназы, гексогеназы, 2,3-дифосфоглицеромутазы, фосфогексоизомеразы) новорожденным ставится крайне редко, так как требует проведения высокодифференцированных исследований. В клинической картине у новорожденных с этой патологией выявляются гемолитическая анемия с ретикулоцитозом, увеличение печени и селезенки. Характерен семейный анамнез.
Большие гематомы в периоде новорожденности также могут стать причиной выраженной непрямой гипербилирубинемии и анемии. Наличие у ребенка больших размеров кефалогематом, внутрижелудочковых кровоизлияний, субкапсулярных гематом паренхиматозных органов, массивных кровоизлияний в мягкие ткани сопровождается характерной клинической картиной.
Механические желтухи характеризуются накоплением в крови прямого (связанного) билирубина, что сопровождается желтухой, имеющей зеленоватый оттенок, увеличением размеров печени, изменением окраски стула (обесцвечивание) и мочи (нарастание интенсивности окраски).
Синдром сгущения желчи у новорожденных развивается как осложнение гемолитической болезни новорожденных, имеющих обширные кефалогематомы, а также перенесших асфиксию в родах. При этом нарастание интенсивности желтухи отмечается с конца первой недели жизни, сопровождается увеличением размеров печени, иногда значительным, и частичным обесцвечиванием стула. Лечение заключается в применении холеретиков и холекинетиков.
Кроме того, синдром сгущения желчи может являться одним из наиболее ранних клинических проявлений муковисцидоза, особенно если он сочетается с мекониальным илеусом или поражением бронхолегочной системы. Постановке правильного диагноза в данном случае способствуют определение содержания альбумина в меконии, ультразвуковое исследование (УЗИ) поджелудочной железы, проведение потовой пробы.
Причиной механической желтухи в периоде новорожденности могут быть пороки развития желчевыводящих путей: внутри- и внепеченочная атрезия желчных ходов, поликистоз, перекруты и перегибы желчного пузыря, артериопеченочная дисплазия, синдром Аладжилля, синдромальное уменьшение количества междольковых желчных протоков.
При атрезии желчевыводящих путей первым признаком порока развития служит желтуха, которая носит упорно нарастающий характер, сопровождается зудом кожных покровов, из-за чего дети бывают очень беспокойны и раздражительны. Постепенно нарастают размеры и плотность печени, изменяется характер стула: он становится частично или полностью обесцвеченным. Явления холестаза приводят к мальабсорбции жиров и жирорастворимых витаминов, нарастают гипотрофия и гиповитаминоз. В возрасте 4–6 мес появляются признаки портальной гипертензии, геморрагического синдрома. Без оперативного вмешательства такие пациенты погибают в возрасте до 1–2 лет жизни. Биохимический анализ крови выявляет наличие гипопротеинемии, гипоальбуминемии, повышение прямого билирубина, щелочной фосфатазы.
При синдроме канальцевой гипоплазии желчных путей (синдром Аладжилля), наследуемом по аутосомно-рецессивному типу, определяются и другие пороки развития: гипоплазия или стеноз легочной артерии, аномалии позвоночных дуг, почек. Характерны стигмы дизэмбриогенеза: гипертелоризм, выступающий лоб, глубоко посаженные глаза, микрогнатия.
Механические желтухи могут быть обусловлены сдавлением желчных протоков извне опухолью, инфильтратами и другими образованиями брюшной полости. Нередко отмечается обтурация общего желчного протока при врожденной желчнокаменной болезни.
Выделяют группу наследственно обусловленных дефектов экскреции связанного билирубина. К ним относятся синдром Дубина–Джонсона, обусловленный «поломкой» каналикулярной транспортной системы. Синдром наследуется по аутосомно-рецессивному типу, сопровождается умеренным повышением уровня прямого билирубина, небольшим увеличением размеров печени, массивным выделением с мочой копропорфиринов. В биоптатах в клетках печени наблюдается отложение коричнево-черного пигмента, напоминающего меланин. Синдром Ротора также наследуется по аутосомно-рецессивному типу, но в основе этого синдрома лежит дефект захвата и накопления клетками печени органических анионов. Клиническая картина аналогична таковой при синдроме Дубина–Джонсона. Отложения пигмента в клетках печени нет.
Постановке правильного диагноза при синдроме холестаза в период новорожденности помогают УЗИ печени, радиоизотопное сканирование, чрескожная биопсия печени, холангиография и т. д.
Паренхиматозные желтухи обусловлены поражением паренхимы печени воспалительного характера. Причиной поражения могут являться вирусы, бактерии и простейшие: вирус гепатита В и С, цитомегаловирус, Коксаки, краснухи, Эпстайна–Барр, вирус простого герпеса, бледная трепонема, токсоплазма и др. Септический процесс у новорожденного может сопровождаться прямым бактериальным поражением печени.
Клиническая картина паренхиматозной желтухи включает в себя ряд общих и строго специфических признаков: дети часто рождаются недоношенными или незрелыми, с задержкой внутриутробного развития, маловесными к сроку гестации, имеют признаки поражения нескольких органов и систем, вследствие чего состояние их при рождении расценивается как крайне тяжелое. Желтуха имеется уже при рождении и носит сероватый, «грязный» оттенок, на фоне выраженных нарушений микроциркуляции, часто с проявлениями кожного геморрагического синдрома. Характерна гепатоспленомегалия. При исследовании биохимического анализа сыворотки крови выявляются как прямая, так и непрямая фракции билирубина, повышенная активность (в 10-100 раз) трансаминаз печени, увеличение щелочной фосфатазы, глутаматдегидрогеназы. Метод Эберлейна свидетельствует о серьезных нарушениях в конъюгационных механизмах печеночной клетки — подавляющее количество прямого билирубина представлено фракцией моноглюкуронидбилирубина. Общий анализ крови нередко выявляет анемию, ретикулоцитоз, тромбоцитопению, лейкоцитоз или лейкопению. В коагулограмме — дефицит плазменного звена гемостаза, фибриногена. Для установления возбудителя инфекционного процесса проводятся его идентификация путем полимеразной цепной реакции (ПЦР), определение титров специфических иммуноглобулина М и иммуноглобулина G. Лечение заключается в назначении специфической антибактериальной, противовирусной и иммунокорригирующей терапии.
Обобщая вышесказанное, отметим, что диагностические мероприятия при неонатальных желтухах должны учитывать ряд положений.
Кроме того, проведение прямой и непрямой пробы Кумбса позволит предположить, имеет ли место несовместимость крови матери и ребенка по редким факторам.
Биохимический анализ крови (определение общего билирубина и его фракций, уровня трансаминаз печени, щелочной фосфатазы, концентрации общего белка, альбумина, глюкозы, мочевины и креатинина, холестерина и триглицеридов, С-реактивного белка, тимоловой пробы и т. д.) позволяет не только диагностировать вид желтухи, но и собрать данные о состоянии других органов и систем, имеющие большое значение при назначении радикальных способов лечения (например, об изначальной функции почек очень важно иметь представление до проведения заменного переливания крови, так как одним из осложнений этой операции является острая почечная недостаточность).
Метод Эберлейна (определение фракций прямого билирубина — моно- и диглюкуронидбилирубина) имеет значение при дифференциальной диагностике механических и паренхиматозных желтух.
Необходимо также проведение тестов на выявление инфекционного агента в крови, стадии заболевания (ПЦР, иммуноферментный анализ, определение количества и вида иммуноглобулинов, определение авидности и аффинности антител, реакция Вассермана и др.).
Определение профиля гормонов щитовидной железы проводится при подозрении на гипотиреоз.
Осмотическая резистентность эритроцитов, электрофорез гемоглобина, скрининг-тесты на определение глюкозо-6-фосфатдегидрогеназы проводятся с целью уточнения причины наследственных гемолитических анемий.
Потовая проба при подозрении на муковисцидоз проводится у детей старше 1 мес жизни; в раннем неонатальном периоде можно практиковать определение содержания альбумина в меконии.
Анализы включают также определение содержания a-1-антитрипсина в сыворотке крови, УЗИ головного мозга, внутренних органов брюшной полости.
Рентгенологический метод, компьютерная томография проводятся при подозрении на кишечную непроходимость, внутричерепные кровоизлияния, фиброэзофагогастродуоденоскопия — при подозрении на пилоростеноз. Чрескожная биопсия печени проводится в спорных случаях с целью верификации диагноза.
До начала проведения лечебных мероприятий необходимо определить способ кормления новорожденного: грудное вскармливание не допускается при гемолитической болезни новорожденных, галактоземии, тирозинемии.
Лечение гипербилирубинемий
Рассмотрим сновные методы лечения гипербилирубинемий.
Литература
Л. А. Анастасевич, кандидат медицинских наук
Л. В. Симонова, кандидат медицинских наук
РГМУ, Москва
Источники информации:
- http://stimbifid.ru/stati/kak-proyavlyaetsya-lyamblioz-u-vzroslyh.html
- http://www.vidal.ru/drugs/magnesium_sulfate__34103
- http://www.lvrach.ru/2008/07/5546305
- http://med39.ru/article/pediatria/dgp.html
- http://praktik-dietolog.ru/article/103.html
- http://expert-clinica.ru/blog/kak-zastavit-pechen-pohudet
- http://premium-clinic.ru/dyubazh-pecheni-s-mineralnoy-vodoy-detyam/
- http://www.lvrach.ru/2013/06/15435735
- http://www.lvrach.ru/2006/10/4534522

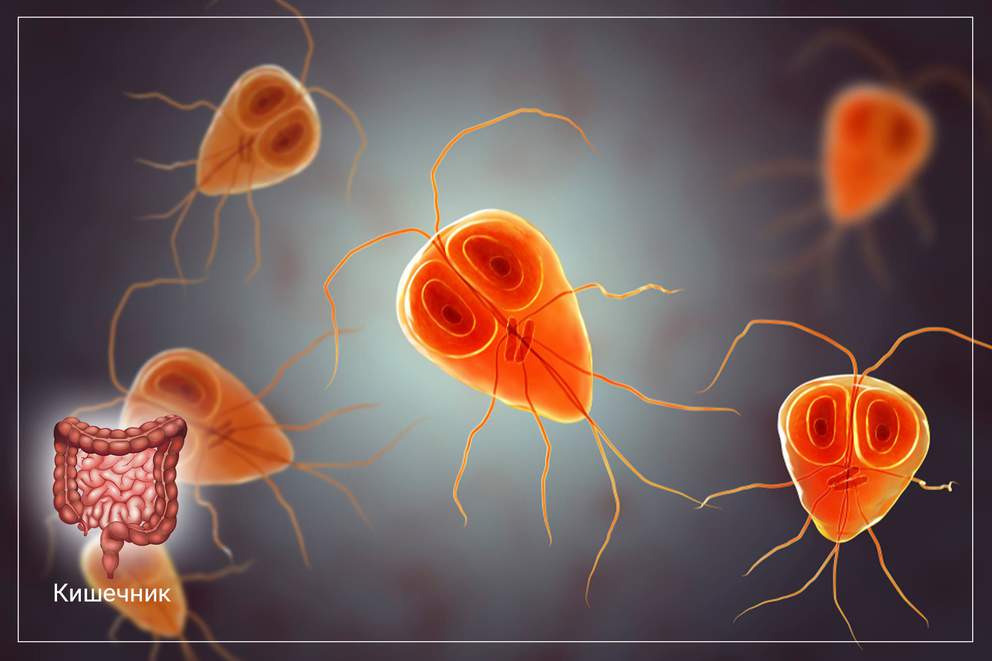




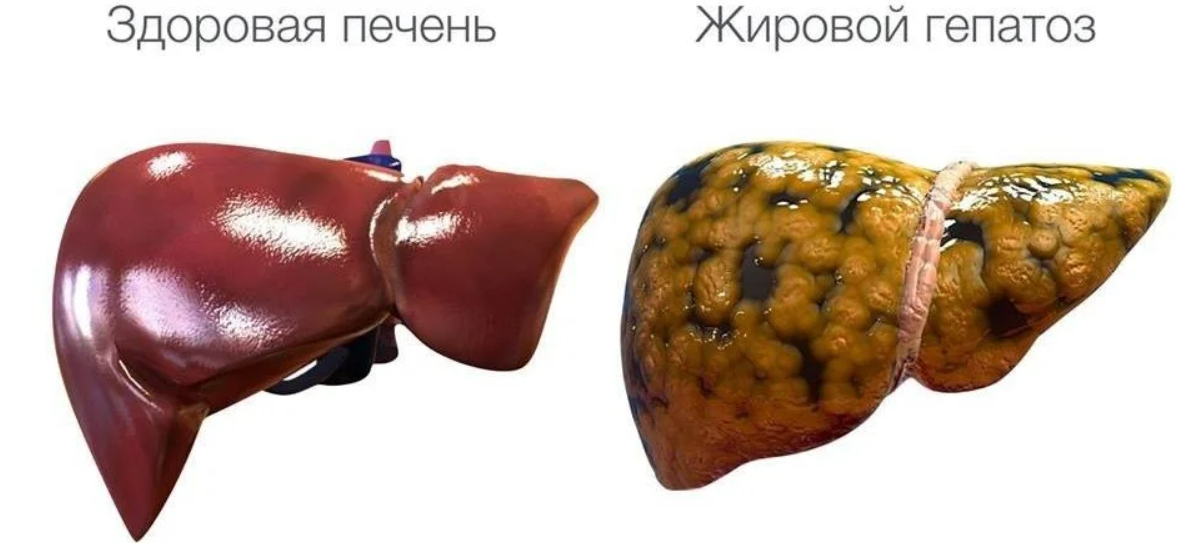
_575.gif)