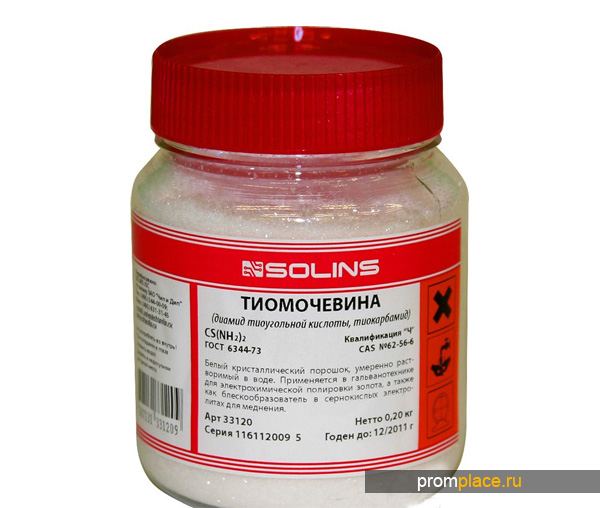
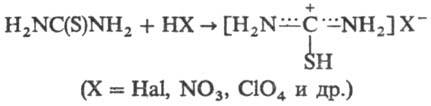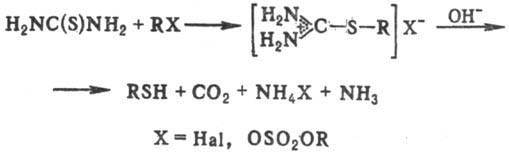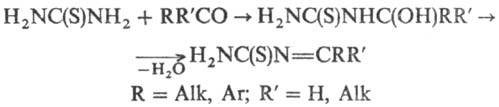тиомочевина что это такое
Тиомочевина
Мы предлагаем тиомочевину со склада по выгодным ценам с доставкой по всей России.
Спецификация
| Чистота | 99% мин. |
| Потери при нагревании | 0,4% макс. |
| Содержание нерастворимых в воде веществ | 0,02% макс. |
| Зольность | 0,005% макс. |
| Содержание роданидов | 0,5% макс. |
Описание
| Мол. масса | 76,12 |
| Внешний вид | Бесцветные кристаллы горького вкуса |
| Растворимость | Растворима в воде, метаноле, этаноле и пиридине. |
| t пл. | 184,5°С |
| Плотность | 1,405 г/см 3 |
| Теплота плавления | 277 кДж/кг |
| Теплота образования | -88,2 кДж/моль |
| Теплоёмкость | При 300K 1235 Дж/(кг·К) |
| Теплопроводность | 0,647 Вт/(м·К) |
Растворимость в воде при соответствующей температуре
Тиомочевина представляет собой сероорганическое соединение. Она структурно подобна мочевине, за исключением того, что атом кислорода заменен атомом серы, но свойства мочевины и тиомочевины существенно различаются. Тиомочевина относится к широкому классу соединений с общей структурой (R1R2N)(R3R4N)C=S.
В смесях с окислителями имеет низкую термостойкость и начинает разлагаться при 80-100°С.
Малотоксична, однако при систематическом воздействии угнетает функцию щитовидной железы и кроветворных органов.
Смеси с хлоратом калия очень чувствительны к механическим воздействиям, поэтому наметилась тенденция по замене тиомочевины менее активным тиурамом или использовании комбинации тиомочевина/мочевина.
Применение
В горнодобывающей сфере тиомочевина используется в качестве флотоагента. С ее помощью обогащают различные металлы.
Она является качественным реагентом во время поиска висмута, рения, рутения.
В сельском хозяйстве тиомочевина выступает в качестве неорганического удобрения. Также ее добавляют в составы фунгицидов. Она имеет высокие дезинфицирующие свойства, поэтому с помощью растворов тиомочевины производят обеззараживание овощей.
Тиомочевину используют для лужения меди, а также в процессе производства полупроводниковой пленки из свинца. Тиомочевина также широко используется в синтезе гетероциклических соединений, а также в качестве ингибитора кислотной коррозии сталей.
Применение тиомочевины в пиротехнике
Используется как низкокалорийное горючее-активатор в цветопламенных и сигнальных дымовых составах.
Способна облегчать воспламенение и интенсифицировать сгорание пиротехнических смесей.
Тиомочевина
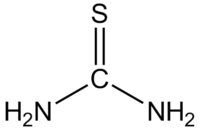
| Тиомочевина | |
 | |
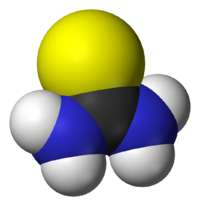 | |
| Общие | |
|---|---|
| Химическая формула | CH4N2S |
| Физические свойства | |
| Молярная масса | 76,12 г/моль |
| Термические свойства | |
| Температура плавления | 182 °C |
| Классификация | |
| Рег. номер CAS | 62-56-6 |
| SMILES | C(=S)(N)N |
Тиомочевина — CS(NH2)2 — диамид тиоугольной кислоты, тиокарбамид, белые кристаллы горького вкуса, tпл 180—182 °C (при быстром нагревании; при медленном — разлагается); умеренно растворима в воде, метаноле, пиридине, хорошо — в 50 %-ном водном пиридине.
Тиомочевину применяют в органическом синтезе, для получения лекарственных препаратов (напр., сульфидина).
Содержание
Синтез
Тиомочевина может быть получена изомеризацией роданида аммония, этот синтез аналогичен классическому синтезу мочевины из цианата аммония (кислородного аналога роданида) по Вёлеру:
Подобно синтезу мочевины из аммиака и диоксида углерода, тиомочевина также быть синтезирована при взаимодействии аммиака и сероуглерода:
Тиомочевину также получают взаимодействием H2S или сульфидов аммония либо щелочных металлов с цианамидом кальция CaCN2 в водных растворах:
Реакционная способность
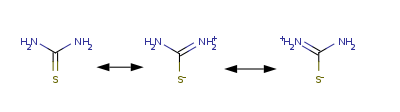
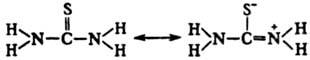
Структура молекулы тиомочевины может быть представлена мезомерными канонической тиоамидной формой и тиоимидными формами, несущими отрицательный заряд на атоме серы и положительный на атомах азота амидинового фрагмента:
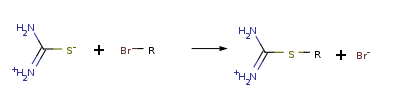
В результате атом серы является сильным нуклеофильным центром и тиомочевина протонируется по атому серы с образованием солей с сильными кислотами. Атаки мягких электрофилов также направляются на атом серы: тиомочевина алкилируется алкилгалогенидами и алкилсульфатами с образованием изотиурониевых солей:
Аналогично протекает реакция тиомочевины с арилдиазониевыми солями.
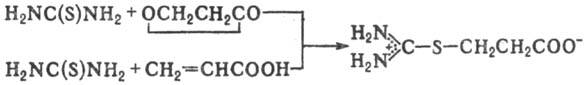
S-алкилирование тиомочевины также является первой стадией её взаимодействия с эпоксидами, ведущего к образованию тииранов (эписульфидов) [2] :
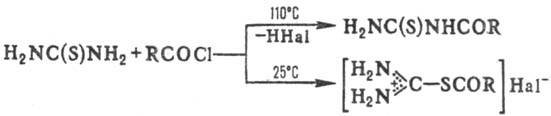
Ацилирование тиомочевины галогенангидридами и ангидридами карбоновых кислот, в зависимости от условий реакции, может протекать как сере (в мягких условиях), так и по азоту (в жестких условиях).
Альдегиды и кетоны с присоединяются к тиомочевине, образуя гидроксиалкилтиомочевины, которые при отщеплении воды превращаются в N-тиокарбамоилимины:
H2NC(S)NH2 + R2CO 

Тиомочевина реагирует с бифункциональными электрофилами, образуя гетероциклические соединения. Так, например, с α-галогенкетонами тиомочевина (и её N-замещенные производные)образует 2-аминотиазолы:
Применение
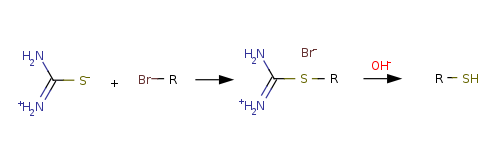
Алкилирование тиомочевины используется алкилирование с образованием алкилтиурониевых солей и их последующим щелочным гидролизом: используется как препаративный метод синтеза алифатических тиолов:
Преимуществом этого метода являются легкая очистка перекристаллизацией тиурониевых солей и достаточно высокие общие выходы тиолов.
Тиомочевина также широко используется в синтезе гетероциклических соединений, а также в качестве ингибитора кислотной коррозии сталей.
Примечания
Литература
Полезное
Смотреть что такое «Тиомочевина» в других словарях:
тиомочевина — сущ., кол во синонимов: 1 • тиокарбамид (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
тиомочевина — (тиокарбамид), (NH2)2CS, бесцветные кристаллы, tпл 182°C. Применяют в органическом синтезе, для разделения углеводородов, как ростовое вещество. * * * ТИОМОЧЕВИНА ТИОМОЧЕВИНА (тиокарбамид), (NH2)2CS, бесцветные кристаллы, tпл 182 °С. Применяют в… … Энциклопедический словарь
тиомочевина — tiokarbamidas statusas T sritis chemija formulė S=C(NH₂)₂ atitikmenys: angl. thiocarbamide; thiourea rus. тиокарбамид; тиомочевина … Chemijos terminų aiškinamasis žodynas
Тиомочевина — диамид тиоугольной кислоты, тиокарбамид, H2NC (S) NH2, белые кристаллы горького вкуса, tпл 180 182 °С (при быстром нагревании; при медленном разлагается); умеренно растворима в воде, метаноле, пиридине, хорошо в 50% ном водном пиридине. Т … Большая советская энциклопедия
ТИОМОЧЕВИНА — (диамид тиоугольной к ты, тиокарба мид) (NH2)2CS, мол. м. 76,12; бесцв. кристаллы горького вкуса; т. пл. 182°С (при быстром нагревании; при медленном нагревании не имеет четкой т ры плавления); плотн. 1,399 1,405 г/см 3; длины связей (нм)… … Химическая энциклопедия
ТИОМОЧЕВИНА — тиокарбамид (от греч. theion сера), (NH2)2C = S белые кристаллы горького вкуса; tnл 180 182 °С. Сырьё для получения меркаптанов, красителей, лекарств. средств, фунгицид, реагент в аналитич. химии … Большой энциклопедический политехнический словарь
ТИОМОЧЕВИНА — (тиокарбамид), (NH2)2CS бесцв. кристаллы, tпл 182 °С. Применяют в органич. синтезе, для разделения углеводородов, как ростовое в во … Естествознание. Энциклопедический словарь
тиомочевина — тиомочев ина, ы … Русский орфографический словарь
ТИОМОЧЕВИНА — тиомочевина, физиологически активное вещество, применяемое для предпосевной обработки картофеля. Производные Т., используемые в качестве гербицидов, инсектицидов и зооцидов, могут быть причиной отравления сельскохозяйственных животных.… … Ветеринарный энциклопедический словарь
ТИОМОЧЕВИНА
С углеводородами тиомочевина образует, подобно мочевине, клат-раты, способные удерживать неск. больших молекул; при этом линейные углеводороды удерживаются слабо, наиб. устойчивы комплексы с объемными молекулами, напр. с n-ди(трет-бутил)бензолом, 2,2,4-триметилпентаном, сква леном, адамантаном и др. (мочевина с указанными соед. клатратов не образует).
Структура молекулы тиомочевины может быть представлена резонансными тиоамидо- и тиоимидоформами с преобладающим вкладом последней, что обусловливает хим. св-ва тиомочевины:
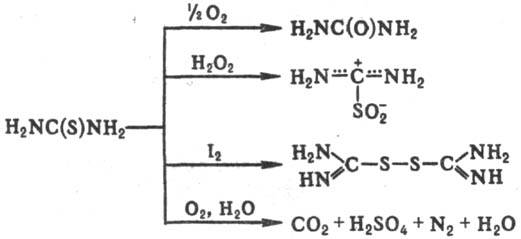
В хим. р-циях тиомочевины в качестве нуклеоф. центра выступает атом S, а не атом N (как в мочевине). Тиомочевина образует соли с галогенами, минер. и орг. к-тами, а также нек-рыми основаниями, напр.:
С солями ряда металлов (Сr, Zn, Cd, Hg, Pb, Ni, Со) дает комплексные соединения. Легко реагирует с алкилгалогени-дами, диалкилсульфатами и др. алкилирующими агентами с образованием S-алкилпроизводных изотиомочевины (S-алкилизотиурониевых солей). Последние малоустойчивы и при попытке выделения распадаются до тиолов:
Взаимодействие тиомочевины с ацилгалогенидами или ангидридами карбоновых к-т в зависимости от т-ры р-ции приводит к N- или S-ацилпроизводным:
S-Арилирование тиомочевины осуществляют с помощью активир. арилгалогенидов или арендиазониевых солей.
При взаимодействии тиомочевины с альдегидами или кетона-ми образуются гидроксиалкилтиомочевины, к-рые при отщеплении воды м. б. превращены в N-тиокарбамоилимины:
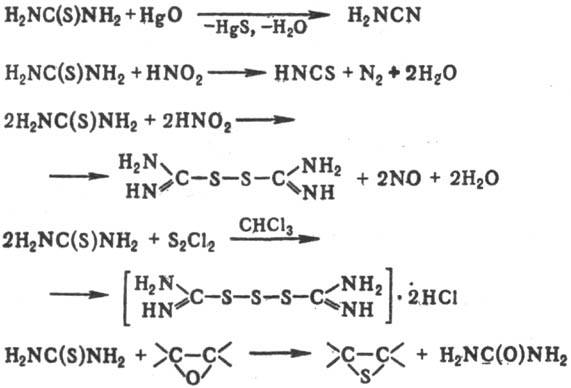
Т иомочевина подвергается окислит. десульфуризации под действием Рb 3 О 4 или HgO с образованием цианамида; с нитритами
металлов в присут. к-т в зависимости от рН среды образует тиоциановую к-ту или формамидиндисульфид, при обработке S 2 Cl 2 в СНСl 3 дает дигидрохлорид формамидинтри-сульфида; с эпоксидами образует тиираны:
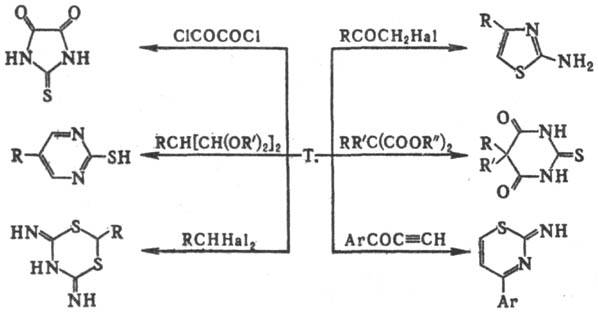
Р-ции тиомочевины с бифункцион. соединениями используют для синтеза разл. гетероциклич. систем, напр.:
Ca(CN) 2 + (NH 4 ) 2 S + 2Н 2 O : H 2 NC(S)NH 2 + Са(ОН) 2 + 2NH 3 CS 2 + 2NH 3 : H 2 NC(S)NH 2 + H 2 S
Для определения тиомочевины используют титрование р-рами окислителей (хлорамины и др.) в присут. KI.
В своб. виде тиомочевина содержится в нек-рых растениях.
Т иомочевину применяют в синтезе тиолов, красителей, синтетич. смол, в произ-ве лек. препаратов, для разделения парафинов, в качестве реагента для фотометрич. определения Bi, Os, Re, Ru; обладает фунгицидным действием.
Тиомочевина
Тиомочевина является канцерогенным веществом, которое в основном применяется для обработки золота. На внешний вид это химическое соединение напоминает кристаллы ромбовидной формы белого цвета. Полное название этого вещества – диамид тиоугольной кислоты. Молекулярная формула тиомочевины CH4N2S. Сейчас ее не используют в пищевой промышленности, так как это вещество выделяет токсичные элементы, но лет 10-15 назад ее применяли в качестве консерванта для свежих цитрусовых плодов.
Качество тиомочевины регламентируется государственным документом ГОСТ 6344-73 «Реактивы. Тиомочевина. Технические условия».
Физико-химические особенности
Молекулярная масса тиомочевины составляет 76,12. Плотность кристаллов предельно невысокая – 1,405 г/см3. Это вещество способно плавиться, но только при температуре 176°C. При повышении температуры до 200 °C тиомочевина начинает разлагаться, выделяя канцерогенные вещества. Класс опасности тиомочевины: 6. Но стоит отметить, что процесс разложения возможен только тогда, когда температура нагрева будет постоянной и быстрой.
Тиомочевина вступает в различные реакции. Она способна создавать соли с минеральными кислотами, а с некоторыми металлами она образует целые комплексные соединения. Это химическое вещество быстро растворяется в водной среде, а также во время нагрева в спиртах.
Получение вещества
Синтез тиомочевины происходит тремя способами:
Сферы применения
Спектр применения тимочевины достаточно широкий. Ее химические свойства ценятся на горнодобывающих комбинатах, в сельском хозяйстве, в текстильной промышленности, металлургии, фармацевтике.
В горнодобывающей сфере тиомочевина используется в качестве флотоагента. С ее помощью обогащают различные металлы. Она является качественным реагентом во время поиска висмута, рения, рутения.
Но особенную ценность это вещество имеет на золотодобывающих комбинатах, так как там из тиомочевины восстанавливают золото и серебро. Чтобы получить золото из тиомочевинных растворов, смолы, в состав которых входит золото и серебро, подвергают десорбции. Для того чтобы тиомочевина осадила золото, необходимо провести ряд реакций:
Последний метод считается одним из самых современных. Во время пропускания многокомпонентной смеси через регенерат постоянного тока, золото и серебро восстанавливаются на катоде.
В сельском хозяйстве тиомочевина выступает в качестве неорганического удобрения. Также ее добавляют в составы фунгицидов. Она имеет высокие дезинфицирующие свойства, поэтому с помощью растворов тиомочевины производят обеззараживание овощей. Посадочный материал замачивают в тиомочевины, из расчета 5 г на 1 л воды. Картофелю достаточно пробыть в таком растворе 18 часов, и споры грибков и бактерий будут полностью удалены.
Применение тиомочевины в сельском хозяйстве обусловлено ее быстрым воздействием на патогенную микрофлору, кроме того, это вещество способно полностью излечивать лук и картофель. Также тиомочевину используют в саду в качестве фунгицида.
Раньше это вещество применяли и в пищевой промышленности, так как тиомочевина – это мощный консервант. Она предотвращает развитие микробиальной порчи фруктов, препятствует ферментации. Но сейчас это химическое соединение запрещается использовать в пищевой сфере, так как оно выделяет канцерогены, блокирует работу щитовидки.
Производные тиомочевины используют в составах электролитического золочения. Изделия, которые покрытые золотом, долго не тускнеют, имеют длительную отражательную способность. Такие характеристики этого вещества ценятся в электронной промышленности. Тиомочевину используют для лужения меди, а также в процессе производства полупроводниковой пленки из свинца.
Особенности, требований безопасности, фасовки, транспортировки и хранения тиомочевины
Так как это вещество имеет 6 класс опасности, допустимой нормой концентрации в воздухе считается 0,3 мг/м. В лабораториях, складских помещениях или цехах, где происходит непосредственный контакт с данным веществом, должна быть установлена соответствующая непрерывная вентиляция. Рабочий персонал должен иметь всевозможные средства защиты:
Любые операции с данным веществом нужно проводить под вентиляционным шкафом.
На производственных предприятиях фасовка тиомочевины может производиться от 10 г и до 25 кг в различные виды тары (полиэтиленовые пакеты, тубы, стеклянные банки, плотные мешки).
Транспортировать тиомочевину согласно ГОСТу 6344 73 разрешается всеми видами транспорта. Допустимый срок хранения составляет 12 месяцев со дня производства.
Цена тиомочевины за 1 кг на российском рынке варьируется от 160 до 220 рублей. Основными производственными компаниями, которые изготавливают тиомочевину, являются:
Мировым лидером по производству тиомочевины считается Китай. Эта страна предлагает поставки по всему миру, в том числе и в Российскую Федерацию.
Тиомочевина: свойства, формула, области применения
Тиомочевина (тиокарбамид) – это твердое белое вещество, сформированное кристаллическими компонентами ромбической сингонии. По сути, является диамидом тиоугольной кислоты. Вкус имеет горький. При стремительном нагреве, достигая температуры 180-182 °C, плавится, а нагреваясь постепенно и неспешно, разлагается. В таких средах, как вода, метиловый спирт и пиридин, растворению поддается в средней степени, в 50 % H2O р-воре пиридина растворяется хорошо, в этоксиэтане – плохо. В бензоле и четыреххлористом углероде не растворимо.
Молярная масса – 76,12 г/моль, плотность – 1,405 г/см 3 (при 20 °C). Термосвойства: t плавления – 176 °C, t разложения – 200 °C. Формула: CH4N2S.
Реагирование

— дихлордисульфаном в метилтрихлориде (в результате появляется дигидрохлорид формамидинтрисульфида);
— оксидом ртути в H2O или эфире (формируется цианамид);
— пероксидом водорода при условии нейтральности среды (на выходе образуется формамидинсульфоновая кислота);
— альдегидами или кетонами (появляются гидроксиалкилмочевины, которые в случае отсоединения от них воды становятся N-тиокарбамоилиминами).
Заслуживают внимания и реакции, происходящие при нагреве данного вещества. Если длительно поддерживать температуру 130 °C, то происходит трансформация в тиоцианит аммония. Достижение 200 °C приводит к формированию ряда продуктов, среди которых: цианамид, дисульфид углерода, нитрид водорода и др. Совместный нагрев со щелочами – основа для гидролиза до аммиака, дигидросульфида и углекислоты, а умеренный вместе с ангидридом уксусной кислоты – для появления N-ацетилтиомочевины.
Также для рассматриваемого вещества характерна реакция S-арилирования (происходит, если задействовать активированные арилгалогениды/соли арилдиазония).
Получение
Для образования тиомочевины, как правило, берут тиоциановокислый аммоний и превращают его в изомер при t 170 °С. Но это не единственно возможный способ синтеза данного соединения. Также получить его можно, по классике жанра, синтезируя цианат аммония по методу Велера. И еще один вариант: в ходе синтеза нитрида водорода и углерода (IV) сульфида. 98 % тиокарбамид при t 130 °С, которая воздействует на него продолжительное время, становится опять роданидом аммония.
Применение
Данный продукт востребован в различных отраслях. Давайте рассмотрим основные из них.
В горнодобывающем направлении, пожалуй, в наибольшей степени, ценны хим. свойства тиокарбамида. Здесь он выполняет роль флотационного средства для различных металлов. Это также отличный реагент, который приходит на помощь в поисках Bi, Re, Os и Ru. С его помощью производят синтетические смолы и рассоединяют парафины.
Особая значимость отмечается в функционировании добывающих золото комбинатов, где с помощью рассматриваемого продукта производят восстановление Au и Ag. Как именно? Содержащие золото и серебро смолы десорбируют. Тиомечевина способна осадить золото при реализации некоторых реакций: цементации (благородный металл вытесняют при помощи Pb, Al или Zn), осаждении щелочью и электролизе с анодами, не поддающимися растворению. Самым инновационным является последний процесс. Когда совокупность многих компонентов проходит сквозь регенерат постоянного тока, происходит восстановление на катоде золота и серебра.
Тиокарбамид задействуют в электролитическом блестящем золочении (является составляющей одного из самых популярных электролитов для гальванозолочения). Кроме того, он задействуем в хим. лужении медных изделий и деталей из сплавов на основе данного металла. С его участием, а также с задействованием нитрата свинца и каустического поташа, на PbS наносят полупроводниковую пленку при t 45-60 °C. Рабочий раствор в данном процессе характеризуется разовостью применения. Работу могут затруднить такие факторы, как высокая t и точные размерные параметры моделей.

Также водные растворы данного реактива с концентрацией 500 миллиграммов на килограмм способны минимизировать или тормозить потемнения и микробиальную порчу плодов (действуют больше на плесень, меньше на бактерии). Но, обратите внимание, что применение данного материала в пищепроме, а следовательно и введение его в любые продукты питания, запрещено. Этот консервант является сильнейшим канцерогеном, осуществляет большое токсическое воздействие на человеческий организм и блокирует работу щитовидки. Хотя в свое время его использовали для предотвращения преждевременной порчи цитрусовых.
Где еще применяем данный химикат? В текстильном производстве, металлургической индустрии, электронной промышленности, фармацевтической отрасли, медицине и др. Без него не обходится органический синтез (создание алифатических тиолов и гетероциклов). Из него производят лекарства, в частности сульфидин. Он выступает хорошим ингибитором кислотных коррозионных проявлений на сталях.
Вместо заключения. В каком бы из упомянутых направлений вам не понадобилось использовать тиокарбамид, помните: ему присвоен шестой класс опасности, а допустимая концентрация в воздушном пространстве составляет 0,3 мг/м. Используйте при работе спецодежду, респиратор, очки и перчатки. Храните, перевозите и применяйте этот продукт с осторожностью, согласно предписаниям технической документации.