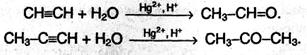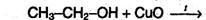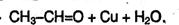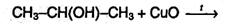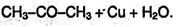температура кипения альдегидов ниже температуры кипения соответствующих спиртов так как
Большая Энциклопедия Нефти и Газа
Температура кипения альдегидов ниже температуры кипения соответствующих им спиртов. [1]
Температура кипения альдегидов и кетонов ниже температуры кипения соответствующих первичных и вторичных спиртов. [3]
Температура кипения альдегидов и кетонов более низкая, чем у соответствующих им спиртов. В гомологическом ряду с увеличением молекулярного веса температура кипения понижается. [4]
Температура кипения альдегидов и кетонов ( табл. 4.1 и 4.2) несколько выше, чем у углеводородов и простых эфиров равного молекулярного веса, но значительно ниже, чем у соответствующих спиртов. На примере спиртов и простых эфиров ( табл. 3.2) было выявлено, что плотность возрастает по мере увеличения числа функциональных групп в молекуле. Такая же зависимость наблюдается для карбонильных соединений. Присутствие в их молекуле ароматического ядра также повышает плотность. Монофункциональные альдегиды и кетоны представляют собой нейтральные вещества. [5]
Температура кипения трифторированных альдегидов в основном такая же, как и нефторирэванных альдегидов, за исключением трифторацетальдегида, который кипит приблизительно на 40 ниже ацетальдегида. [6]
Объясните, почему температуры кипения альдегидов ниже, чем у спиртов с тем же числом атомов углерода в молекуле. [7]
Температура в реакционной колбе поддерживается выше температуры кипения альдегида и ниже температуры кипения спирта. В условиях постоянного избытка спирта и отгонки альдегида по мере его образования удается избежать дальнейшего окисления до кислоты. Кетоны практически не подвержены дальнейшему окислению. [11]
Кроме того, отделение примесей кретонового альдегида от уксусной кислоты ( колонна 22, рис. 14.1) легче проводить в присутствии воды, так как кротоновый альдегид будет отгоняться в виде его гетероазеотропа с водой, имеющего температуру кипения 84 0 С, тогда как температура кипения чистого альдегида составляет 102 2 С. [13]
Получение. Карбонильные соединения не образуют водородных связей, поскольку в их молекулах нет атомов водорода с положительным зарядом. По этой причине температуры



Физические свойства
Карбонильные соединения не образуют водородных связей, поскольку в их молекулах нет атомов водорода с положительным зарядом. По этой причине температуры кипения альдегидов и кетонов значительно ниже, чем соответствующих спиртов. Низшие альдегиды и кетоны – легкокипящие жидкости (формальдегид – газ) с резким запахом, хорошо растворимы в воде.
1. Гидратация алкинов. Из ацетилена получают альдегид, из его гомологов – кетоны:
Из-за своей относительной дороговизны, а также из-за того, что: получаемые соединения загрязнены токсичными соединениями ртути, в настоящее время этот способ находит ограниченное применение.
2. Общий способ получения карбонильных соединений – окисление спиртов. В качестве окислителя можно использовать не только дихромат или перманганат калия, но и другие соединения, например, оксид меди (II) при нагревании:
3. При щелочном гидролизе дигалогеналканов, содержащих два атома галогена при одном атоме углерода, образуются двухатомные спирты, в которых две группы ОН соединены с одним атомом углерода. Эти вещества неустойчивы и отщепляют воду, превращаясь в карбонильные соединения:
4. Дегидрирование спиртов. Одним из промышленных способов получения альдегидов и кетонов является дегидрирование спиртов в газовой фазе над металлическими медью, серебром, хромом, никелем, оксидом цинка и др., например:
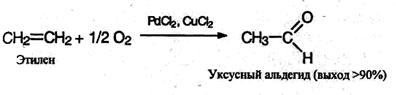
5. Окисление алкенов. Альдегиды и кетоны получают окислением углеводородов ряда этилена кислородом воздуха в присутствии хлоридов палладия (II) и меди. (II), например:
Этим экономичным способом в промышленности получают низшие альдегиды и кетоны.
6. Простейший кетон – ацетон – получают кумольным методом вместе с фенолом.