технология ниэрт что такое
Методика лечения
Историческая справка, научное обоснование и новизна метода
С 1986 года группой ученых Научно-Медицинского центра ООО «Био-Резонанс» совместно с ведущими НИИ МЗ РФ ведутся научные исследования в области низко-интенсивных электромагнитных излучений.
С 1990г. на базах различных Российских институтов проводились исследования по воздействию резонансными радиочастотами на биологические объекты.
В исследованиях принимали участие институт низких температур г.Харьков, институт биофизики и клетки г.Пущино, Радиологический центр г.Обнинск, НИИ онкологии г.Ростов-на-Дону, противочумный институт г.Ростов-на-Дону, центральная городская клиническая больница г.Мытищи Московской обл., городской онкоцентр г.Ростов-на-Дону.
Все разработки и исследования проводились на основе теоретических предпосылок Мельникова В.М. за счет частного инвестирования Дворядкиной Елены Владимировны и в 1998г. был зарегистрирован Научно-Медицинский центр ООО «Био-Резонанс».
На основе экспериментальных исследований создана новая модель молекул типа симметричного волчка с независимыми ортогональными вращательными уровнями. Использование принципов эфиродинамики позволило рассматривать молекулу, как хранитель энергетической и геометрической памяти. Разработаны принципы моделирования молекул и молекулярных структур не ковалентной связи, основы управляемого биосинтеза. Принципы, использованные в работе, позволяют получить вещества с заданными свойствами и методики лечения различных заболеваний.
Новизна метода заключается в получении необходимой температуры в молекуле на клеточном уровне, для разрушения или регенерации клеток, т.е. получении веществ с заданными свойствами, которые можно использовать в наукоемких технологиях промышленности и медицины.
Моделирование молекулярных структур для управления биосинтеза в живых организмах, позволили разработать методики лечения тяжелых заболеваний: различных форм онкологии, гематологии, вирусные, в том числе гепатит «С» и ВиЧ инфекции, сердечно сосудистые, и заболеваний иммунной системы.
Начало применения данной методики положили разработки с 1990г., когда был разработан метод лечения низкоинтенсивной электрорезонансной терапии (НИЭРТ) и созданы приборы «Мультиген-М-01М» и «Мультиген-М-02М», новизна которых подтверждена патентами на изобретения.
Программируемые аппараты «Мультиген-М-01М» и «Мультиген-М-02М» для лечения новообразований и других заболеваний, имеют государственную регистрацию № ФС 02262005/2501-05 нормативный документ ТУ 9444-001-56601421-2005, и № ФС 02262005/2502-05 нормативный документ ТУ 9444-002-56601421-2005, код ОКП 94 4490, также патенты RU 2134598 CI, RU 2139114 CI, RU 2140641 CI, RU 00-00047 (заявка на международный патент), RU 2163823 CI и др.
Указанные аппараты могут использоваться, как для индивидуального, так и для группового лечения пациентов с одинаковым диагнозом.
Данные приборы просты в обращении, не требуют специальных навыков младшего медицинского персонала и могут найти широкое применение не только онкологов, но и у терапевтов, кардиологов, вирусологов, инфекционистов.
Так же разработаны различные методики диагностики и лечения.
Например в онкологии: поскольку электромагнитное излучение производится объемно и безконтактно, то воздействию подвергаются не только очаги заболевания (опухоли), но и клетки по всему организму, в частности, метастазы ( МТЗ) независимо от их местонахождения.
Методика лечения и преимущество
К нам поступают на лечение пациенты, которым отказано в лечении, неэффективны методы общепринятой практики, как правило, пациенты с рецидивом заболевания, желающие избежать операции или неоперабельные.
Воздействие на человека радиоволнами происходит в диапазоне 0,01-18 ГГц определенными резонансными частотами (в зависимости от заболевания), выбранными аккордно (точность подачи каждой частоты до четвертого знака после запятой, сигнал сложномодулированный. Плотность потока, мощности, значительно ниже санитарных норм, что подтверждается заключением ВНИИМТ МЗ РФ и НИИ профзаболеваний и гигиены труда о безвредности данного излучения для населения.) из поддиапазонов прибора, на расстоянии от 2 до 5 метров от человека, что позволяет одновременно проводить сеансы группе людей, сеанс длится от 2 до 8 часов в зависимости от вида и тяжести заболевания.
Радиочастоты подобраны в зависимости от вида заболевания, и сформированы в сеансы, записанные на ЧИП (что исключает вмешательство «человеческого фактора», т.е. ошибок обслуживающего персонала), назначения номеров и количества сеансов делает лечащий врач, специально обученный методике применения НИЭРТ и инструкциям разработчика методики и приборов.
Принятие сеансов производиться безконтактно, воздействие электромагнитного излучения осуществляется тотально на весь организм, поэтому воздействию подвергаются раковые клетки, находящиеся как в опухоли, так и в участках метастазирования, независимо от их расположения. Применение НИЭРТ (Низко Интенсивная Электро Резонансная Терапия), ни в одном случае не вызвало каких-либо осложнений.
Метод НИЭРТ обладает следующими преимуществами:
Показания и противопоказания к применению метода
Применение метода показано для всех нозологических единиц заболеваний независимо от стадии заболевания, а так же вирусных и бактериальных инфекций. Метод безвреден и не имеет специфической токсичности, из-за нетепловой интенсивности электромагнитного поля радиодиапазона, не вызывает побочных явлений. Использование метода возможно и при отсутствии точных данных об онкологическом диагнозе. Метод может также применяться при следующих показаниях:
Внедрение данной методики НИЭРТ в самостоятельном и/или сочетанном виде позволит:
Внедрение данной методики дает возможность:
Внедрение в практику лечения НИЭРТ, а также нового способа применения дистанционной гамма-терапии, химиотерапии с одновременным воздействием низкоинтенсивным электромагнитным излучением радиодиапазона (НИЭРТ) позволит значительно увеличить эффективность лучевой терапии, химиотерапии, избавит пациентов от радикального оперативного вмешательства при удалении злокачественных опухолей. Улучшить качество жизни и социальную адаптацию больных, избавить от инвалидности.
Технология ниэрт что такое
В комплексной терапии онкологических заболеваний используются 4 метода лечения: хирургия, химиотерапия, лучевая терапия, иммунотерапия. Сейчас самое большое финансирование и все внимание брошены на лекарственную терапию. Но со следующего года грядут изменения и в лучевой. А это для Петербурга – самое больное место.
Как говорит профессор Сергей Новиков, заведующий отделением лучевой терапии НМИЦ онкологии им Петрова, за последнее десятилетие лучевая терапия сделала большой рывок и ее стремительное развитие не останавливается. Появились новые аппараты, новые технологии, а с ними — новая идеология лучевой терапии.
— Сергей Николаевич, правда ли, что новые технологии в лучевой терапии когда-то заменят хирургию?
— Вы имеете в виду лечение с помощью гамма-ножа и кибер-ножа?
— Для лечения какого вида рака они предназначаются, что умеют?
— Легче перечислить, что не умеют — не умеют облучать очень много очагов в головном мозге одномоментно, в отличие от гамма ножа. Но такая ситуация — редкость, а главное, пока нет доказательств целесообразности такой агрессивной терапии, она не продлевает жизнь.
С другой стороны, эти аппараты могут делать все в области высокотехнологичного облучения, когда требуется радиохирургия: используются в комплексном лечении новообразований в головном мозге, локализованных процессах в легких (немелкоклеточный рак), метастатических поражений легких, печени, надпочечников, костей, мягких тканей и т. д. Благодаря высокой точности направления воздействия, они незаменимы в лечении злокачественных новообразований головы и шеи. Например, опухоль языка — очень тяжелая патология, лечить ее хирургически или невозможно, или очень сложно. После операции пациента берем мы. Активно используем методы брахитерапии и стереотаксической лучевой терапии при раке предстательной железы.
Онкологи сегодня говорят, что иммунотерапия перевернула наше сознание в лечении некоторых видов рака. Но забывают упомянуть, что сочетание иммунотерапии с некоторыми видами лучевой терапии увеличивает эффективность практически в два раза. Поэтому трудно встретить протоколы лечения, в которых рекомендована иммунотерапия без лучевой терапии.
— Однако по-прежнему распространен миф о том, что лучевая терапия опасна, потому что может спровоцировать развитие лучевой болезни.
— Если под лучевой болезнью мы подразумеваем то, что происходит с организмом человека, оказавшегося в эпицентре взрыва ядерной бомбы, то даже в 1970 годы лучевая терапия ее не провоцировала. Другое дело, что когда использовали большие поля для облучения, это вызывало разного рода токсичность — развивались осложнения со стороны органов дыхательной или кроветворной системы, например. Я начал работать в 1980-е, и уже тогда были разработаны методы, которые позволяли избегать фатальной или очень серьезной токсичности. Хотя какие-то неприятности от лучевой терапии были, есть и будут. Например, если мы подводим очень высокие дозы в область опухоли предстательной железы, мы можем вызвать повреждения прямой кишки, если облучаем опухоль в легких, — повреждения легких, в мозге — здоровые ткани мозга. И иногда вынуждены рисковать, потому что понимаем: другой возможности спасти человека нет. Да, бывает, лучевая терапия балансирует между добром и злом, но зачастую альтернативы нет. Например, при метастазах в головном мозге — это пациенты, которым часто нейрохирурги уже помочь не могут, возможности химиотерапии, нередко, исчерпаны. А лучевая терапия у таких пациентов ассоциируется с 20-30% риском возникновения лучевого некроза. Но в оставшихся 70-80% случаев есть шанс, что мы поможем пациенту преодолеть на определенное время его проблемы.
— Стереотаксическая лучевая терапия – не самая распространенная технология в Петербурге, возможности для ее применения есть только у двух федеральных специализированных клиник и у одной негосударственной. Часто ли она востребована?
— Парадокс: при том, что в Петербурге можно получить самые современные виды лучевой терапии, петербуржцев направляют на лучевое лечение в клиники, в которых их нет. Более того, на 2020 год из средств петербургского фонда ОМС выделяется 1 млрд рублей на 3D-конформную терапию, выполнять которую в городских специализированных клиниках, можно сказать, не на чем.
— Только кто и на каком оборудовании будет ее проводить? В городских медицинских учреждениях нет современных ускорителей. Да и старые регулярно выходят из строя.
— Мы сражаемся за то, чтобы петербуржцы могли получать современное эффективное лучевое лечение. Но НМИЦ им. Петрова не может принять всех, хотя пока мы никому не отказывали.
Что касается стереотаксической лучевой терапии, которая есть в единичных клиниках Петербурга, мы примерно на 30% увеличиваем объемы ежегодно. И готовы взять на себя столько пациентов, сколько нужно. Поскольку у нас стереотаксическая лучевая терапия проводится на тех же аппаратах, на которых проводится и классическая, чтобы освободить их от загрузки стандартной 3D-конформной лучевой терапией, мы приобрели еще один линейный ускоритель, на котором и будем ее выполнять.
— В Городском онкологическом центре в Песочном и в Городском онкологическом диспансере недостаточно современных линейных ускорителей, на которых можно проводить 3D-конформную лучевую терапию. И мне кажется, что на аппаратах, которые там есть, невозможно использовать сложные технологии, например, радиохирургическое лечение и стереотаксическую лучевую терапию. Поэтому важно, чтобы руководители городской онкологической службы наладили сотрудничество с федеральными учреждениями, частными клиниками, которые готовы и могут помочь петербуржцам.
Конечно, нужно обновлять парк оборудования. Потому что на аппаратах 2001-2005 года, которые морально устарели, а многие уже сняты с производства, можно выполнять паллиативную лучевую терапию, использовать простые методики облучения, но современные достижения радиационной онкологии на них недоступны.
У городских клиник есть рентген-терапия, которой, кстати, у нас нет, в онкодиспансере есть интраоперационный ускоритель, которого больше нет ни у кого в нашем городе.
То есть Петербургу нужна грамотная маршрутизация. Но это очень болезненный вопрос для городских властей. Тут все должны понимать, что его нужно решать, и мы к этому готовы.
— До сих пор федеральные клиники лечили, конечно, петербуржцев, но – по федеральным квотам. И объясняли это тем, что тарифы ОМС на лучевую терапию слишком малы. А количество квот всегда ограничено.
— Те тарифы, что действуют в системе ОМС сейчас, рассчитаны на ту простую лучевую терапию, что есть в городских клиниках. Мы работаем в рамках программы ВМП, потому что используем технологии, которых нет в городских медучреждениях. Программа ВМП рассчитана на то, что люди могут получить помощь там, где ее могут оказать. И ее финансирование было достаточным, чтобы применять в лечении сложные технологии: закупать дорогие расходники, заниматься техническим обслуживанием оборудования. Теперь, насколько я знаю, запланированные на 2020 год тарифы петербургского фонда ОМС эквивалентны тарифам, действующим в программе ВМП.
— На 1 миллиард рублей запланировано 4 тысячи курсов 3Д-конформной терапии. 4 тысячи пациентов ее получат – это много или мало?
— Немало, но 4 тысячи курсов это не 4 тысячи пациентов. Потому что некоторым приходится проводить их повторно. Например, прошла женщина курс терапии по поводу опухоли в молочной железе, но обнаружился метастаз в лимфоузле или в другом месте, его тоже нужно облучать. Я думаю, что это 3-3,5 тысячи пациентов.
— Люди по-прежнему едут за рубеж, чтобы получить лечение радиоактивным йодом. Почему в России оно до сих пор дефицитное, а в Петербурге его и вовсе нет?
— Это не сложная технология, но для ее применения у нас действуют очень строгие требования, вплоть до строительства специальных очистных сооружений. Чтобы выполнить все, что нужно по нормативам, надо выиграть большое сражение, но сначала вложить в его подготовку огромные деньги. Сейчас предпринимаются усилия, чтобы сделать наше законодательство более демократичным — смягчить требования для применения этой технологии. А мы уже фактически готовы к тому, чтобы использовать ее, даже обсуждаем возможность открытия коек для пациентов, нуждающихся в терапии радиоактивными источниками. Эта терапия — это огромная перспектива на будущее.
— Сегодняшняя онкология построена на как можно большей целенаправленности. Часто пациенты слышат от химиотерапевтов о таргетной терапии, которая «бьет точно в цель», вы говорите о стереотаксисе… Действительно ли мы можем воздействовать на опухоль точечно, абсолютно не повреждая окружающие ткани?
— Магической пули, которая бьет только в цель пока нет. И при таргетной терапии избирательность условная, и при стереотаксическом — какая-то доза облучения все же приходится на здоровые ткани и они могут пострадать. Но все же воздействие современных лучей и химиотерапии, действительно, выигрывает в эффективности и точности направленного действия.
— Что нужно сделать, чтобы в лучевой терапии новые технологии появлялись не только в федеральных клиниках? Закупать новые аппараты?
— Я счастлив, что лучевая терапия в нашей стране начала осознано развиваться. Но это огромная машина, она не сдвинется с места мгновенно. Чтобы ее раскрутить, нужно потратить много сил и времени, грамотно использовать финансовые вложения.
То есть миллиарды сначала должны вкладываться не в оборудование, а в людей. Их нужно учить, в том числе за границей, нужно обеспечить их достойным заработком. А когда будут люди, способные работать на современном оборудовании, тогда и нужно его покупать.
— Сколько всего аппаратов для лучевой терапии работают у вас?
Технология ниэрт что такое
Вот на сайтике
http://www.bio-kvant.ru/
Биоквант, лечение рака методом НИЭРТ (Низко Интенсивная Электро Резонансная Терапия)
«Клинические испытания на людях проводились с 1996г. на основании представленных отчетов по воздействию на клеточные культуры и животных, разрешение МЗ РФ комитета по новой медицинской технике протокол №2 от 5.11.1996г., протокол №4 от 5.11.1999г., протокол №3 от 5.07.2001г.
На сегодняшний день имеются серьезные медицинские разработки и созданы промышленные образцы приборов «Мультиген-М-01М» и «Мультиген-М-02М», имеющих государственную регистрацию № ФС 02262005/2501-05 нормативный документ ТУ 9444-001-56601421-2005, и № ФС 02262005/2502-05 нормативный документ ТУ 9444-002-56601421-2005, код ОКП 94 4490, также патенты RU 2134598 CI, RU 2139114 CI, RU 2140641 CI, RU 00-00047 (заявка на международный патент), RU 2163823 CI и др.
Воздействие на человека радиоволнами происходит в диапазоне 0,01-18 ГГц определенными резонансными частотами (в зависимости от заболевания), выбранными аккордно (точность подачи каждой частоты до четвертого знака после запятой) из поддиапазонов прибора, на расстоянии от 2 до 10 метров от человека, что позволяет одновременно проводить сеансы группе людей, сеанс длится от 2 до 8 часов в зависимости от вида и тяжести заболевания.»
Никаких описаний этих приборов я не нащёл
Но вот тут кое что написано
http://www.infosan.com.ua/articles/article.php?ss=10&z=12
теоретические основы резонансной терапии
На основе экспериментальных исследований создана новая модель молекул типа симметричного волчка с независимыми ортогональными вращательными уровнями. Использование принципов эфиродинамики позволило рассматривать молекулу, как хранитель энергетической и геометрической памяти. Разработаны принципы моделирования молекул и молекулярных структур не ковалентной связи, основы управляемого биосинтеза. Принципы, использованные в работе, позволяют получить вещества с заданными свойствами и методики лечения различных заболеваний.
Живые системы рассматриваются на этом основании как природные лазеры с чрезвычайно высокой когерентностью излучения, хотя и с чрезвычайно низкой интенсивностью. Концепция когерентных колебаний в биологических системах была высказана и обоснована X. Фрелихом (Frohlich H., 1988). Для нас крайне интересно, что все эти осцилляции являются высоко чувствительными и способны к сильным реакциям в ответ на сверхслабые стимулы (Del Giudice E. et al, 1989; Smith C.W., 1994).
Как уже было сказано, любая патология начинается с более тонкого уровня биологической организации — нарушения «колебательного равновесия» (Lachovsky J., 1924), т.е. на информационном уровне. Поэтому воздействия, влияющие на колебательные характеристики организма, адресованы непосредственно к истокам нарушений (болезни), в то время, как современные аллопатические методы применяются чаще в расчете на коррекцию местных, более грубых нарушений, рассматриваемых в отрыве от волновой природы организма, и зачастую влекут за собой другие нарушения. Это принципиально разные подходы, отражающие две парадигмы,
Пионерскими работами об информационном действии слабых МП являются работы А.С.Пресмана, Н.И.Музалевской, Г.Ф.Плеханова, В.П.Казначеева.
В свое время А.С.Пресман, выдвигая идею информационного влияния МП, высказывал представление о том, что электромагнитное излучение — от инфранизких до сверхвысоких частот — несет информационную функцию, обеспечивая все необходимые для живого виды связи: с внешней средой, внутри организма, между организмами (Пресман А.С., 1968,1997).
Полагают, что ЭМП, помимо электромагнитной составлящей, имеет торсионную составляющую, т.к. любой магнит, даже постоянный, является носителем торсионного поля, которое может объяснять биологическое влияние МП (Ши¬пов Г.И., 1995; Акимов А.Е., 1995; Бинги В.Н., 1995). Биологическое действие МП может быть гораздо более глубоким, чем мы это представляем сегодня, если вспомнить о волновой природе генома, иммунитета, а также учесть, что многое о механизме взаимодействия поля и организма нам еще неизвестно.
Намешано много чего вместе, от Шноля до Горяева и Шипова с Акимовым.
Применяют эти методы для чего угодно.
Бор-нейтронoзахватная терапия рака: на финишной прямой
Несмотря на достигнутый за последние годы огромный успех в лечении онкозаболеваний, они до сих остаются одной из ведущих причин смертности в развитых странах, где растет продолжительность жизни. Многие злокачественные опухоли мозга, такие как глиобластомы, до сих пор считаются неизлечимыми: только в России от них ежегодно умирает около 4 тыс. человек. Идея облучать опухолевые клетки, насыщенные изотопом бора-10, потоком нейтронов определенного энергетического диапазона родилась много десятилетий назад. Но несмотря на свою кажущуюся простоту, эта методика «клеточного ядерного взрыва» оказалась настолько сложной в реализации, что в мире до сих пор нет ни одного специализированного комплекса для лечения рака с помощью бор-нейтронозахватной терапии. Благодаря работам новосибирского Института ядерной физики СО РАН, где был создан компактный ускорительный источник нейронов нового типа, у нашей страны есть все шансы стать мировым лидером в этой перспективной области терапии наиболее агрессивных раковых опухолей
Первый пучок нейтронов на нашей установке для бор-нейтронозахватной терапии рака (БНЗТ, BNCT) был получен в 2008 г. Главное достижение последних лет в том, что мы не только привели установку в рабочее состояние, но и поняли процессы, которые в ней происходят, и внесли соответствующие изменения в конструкцию. Это важно, потому что мы имеем дело с абсолютно новым типом ускорителя заряженных частиц.
На сегодня в мире используется десяток разных типов ускорителей, но ни на одном из них прежде не удавалось получить протонный пучок большого тока, необходимый для бомбардировки «мишени» – источника нейтронов с конкретными энергетическими характеристиками. При создании нашей установки мы не пошли проторенными путями и, похоже, это оказалось правильным решением. Конечно, в этой области было много гораздо более опытных специалистов, чем мы, но здесь сработал «эффект дилетанта»: появились совершенно новые, нестандартные идеи, которые помогли разрешить ряд казавшихся неразрешимыми проблем в создании компактных медицинских установок для БНЗТ.
Из России – с идеей
Все наши открытия и разработки запатентованы – российских патентов у нас более десятка. Пример наших разработок – нейтроногенерирующая мишень. Когда мы только начали заниматься созданием нашей установки, в одной научной статье уважаемых специалистов было сказано, что лучшей является литиевая мишень, но сделать ее не представляется возможным. У нас такая мишень прекрасно работает уже почти десять лет.
Наша история началась почти двадцать лет назад, когда Г. И. Сильвестрову, руководителю лаборатории ИЯФ СО РАН, позвонил его друг и сокурсник, который был участником конференции в Китае, посвященной перспективам и нуждам бор-нейтронозахватной терапии. Григорий Иванович часто говорил, что он многое знает и умеет как физик, но хотел бы сделать что-то осязаемо полезное для человечества. Увлекшись идеей создать ускорительный источник нейтронов для БНЗТ, он сформировал команду энтузиастов. Сам Сильвестров умер в 2003 г., когда еще никакого «железа» не существовало – только идеи, расчеты да первые эксперименты на прототипах, но работа продолжилась. Уже в 2007 г. ускоритель обрел зримые очертания, а на следующий год был получен первый нейтронный пучок
Недавно произошел примечательный казус, когда меня пригласили в Институт науки и технологий Окинавы – японский аналог нашего Сколково, в который были вложены безумные средства. Одна из задач лаборатории, которую возглавил бывший директор КЕКа (знаменитого японского ускорительного комплекса), – создание нейтроногенерирующей мишени. Изучив этот вопрос, японский руководитель также пришел к мысли, что такую мишень сделать невозможно, но мои друзья и его коллеги из КЕКа убедили его, что еще как можно! И я на их лабораторном семинаре рассказал, что есть совсем простая альтернативная идея, как ее сделать. До сих пор помню потрясенное выражение их лиц… Сейчас подобные мишени делаются во всем мире: в первой статье обычно ссылаются на наши работы, потом забывают. Это нормально: чтобы защитить свои идеи, надо не топтаться на месте, а придумывать что-то новое.
В октябре 2016 г. в г. Колумбия американского штата Миссури состоялся Конгресс по нейтрон-захватной терапии, который проводится раз в два года. Там собираются все – химики, биологи и физики, всего около 200 человек. В этот раз от России было два представителя – я и В. И. Брегадзе из Института элементоорганических соединений им. А. Н. Несмеянова РАН (Москва), который занимается созданием соединений адресной доставки бора. Это показывает, какие отечественные команды достигли реальных успехов в этой области.
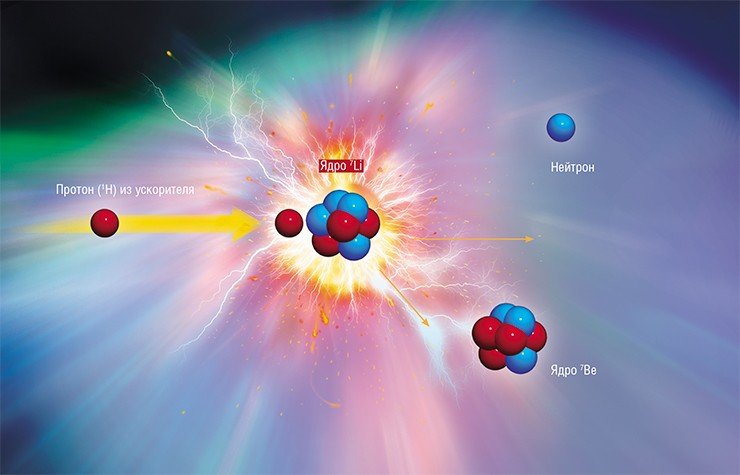
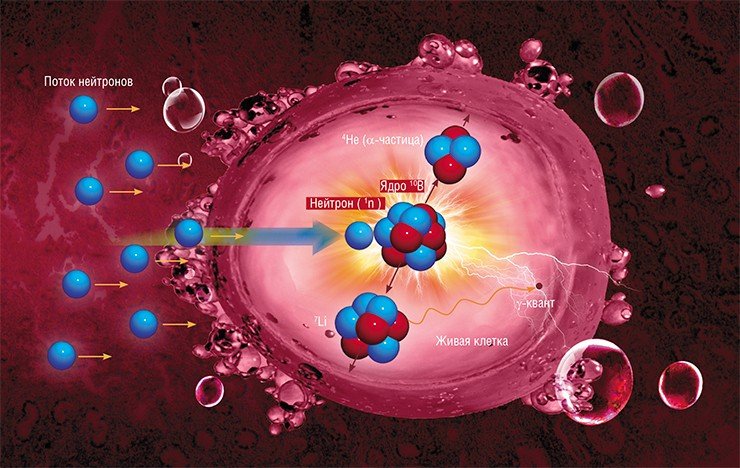
ВЗРЫВ В КЛЕТКЕ Идея бор-нейтронозахватной терапии была впервые предложена еще в 1936 г. – спустя 4 года после открытия нейтрона. Суть ее в том, что раковые клетки, насыщенные стабильным изотопом бора-10, облучают потоком тепловых нейтронов. Ядро бора-10 способно очень эффективно захватывать такой нейтрон, даже когда он «пролетает» мимо на расстоянии в десятки и сотни раз большем размера самого ядра. При поглощении нейтрона происходит образование двух массивных частиц. Благодаря быстрому торможению продуктов распада бора около 80 % энергии этой ядерной реакции выделяется внутри раковой клетки, что приводит к ее необратимому разрушению. Поток нейтронов должен иметь достаточную плотность, а максимум их поглощения должен приходиться на глубину, где расположена опухоль. Лучше всего этим требованиям соответствуют так называемые эпитепловые («промежуточные») нейтроны с энергией от 0,5 эВ до 10 кэВ. При этом распределение по энергии должно быть предельно узким, чтобы вклад сопутствующих потоков медленных и быстрых нейтронов, а также гамма-лучей был минимальным
Я знаю в мире еще лишь две группы, которые, как говорят, получили пучок с нужными параметрами на ускорителях другого типа, одна бельгийско-японская, другая американская, но только наши результаты на сегодняшний день опубликованы. На том же конгрессе от российской стороны было представлено 7 докладов, три из которых докладывали японцы. И на первом же выступлении прозвучал вопрос: зачем они вообще поехали в Сибирь? Ответ был прост: там единственный источник нейтронов, который реально работает.
Из российских специалистов я бы хотел отметить еще В. Н. Митина, руководителя ветеринарной клиники при Российском онкологическом научном центре им. Н. Н. Блохина, который с помощью БНЗТ довольно успешно лечил собак на учебном ядерном реакторе соседнего МИФИ. После его смерти 11 лет тому назад эти работы прекратились.
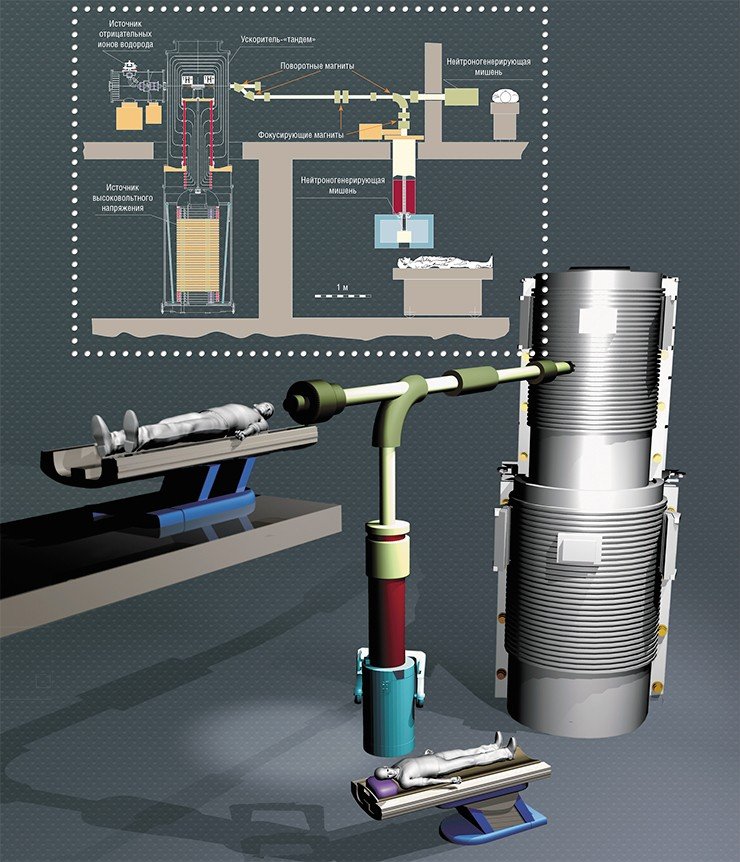
В обычных ускорителях заряженные частицы накачивают энергией в ускорительной трубке, представляющей собой ряд металлических колец – электродов, на которые подается последовательно возрастающий потенциал. Они разделены кольцами их диэлектрика, на которые при большом токе попадают вторичные частицы и ультрафиолетовое излучение, что может вызывать пробои. Это снижает энергетическую эффективность и стабильность устройства.
В новом ускорителе-тандеме вместо стандартной ускорительной трубки используется конструкция в виде «кочана капусты», где на «кочерыжке»-изоляторе в вакууме висят «листы»-электроды. Пучок отрицательно заряженных протонов проходит через центр «кочана» под углом 90 ° к «кочерыжке». Так как электроды в этом случае не разделены изоляторами, их можно расположить ближе друг к другу, что обеспечивает больший темп ускорения частиц
Кстати сказать, подобное лечение очень недешевое: стоимость препаратов адресной доставки бора довольно высока, так как при достаточно сложном производстве спрос невелик. Сегодня доза препарата, необходимая для лечения одного больного, обойдется в случае борфенилаланина примерно в 0,25 млн рублей, боркаптата – раза в 4 больше. Но 15 лет назад эти препараты стоили еще на порядок дороже, а сейчас на каждой конференции по БНЗТ предлагаются и обсуждаются сотни новых препаратов адресной доставки бора. Правда, каждый раз новые… В России таких соединений вообще не выпускают, мы используем препараты, произведенные чешской компанией Katchem.
Если же перейти к глобальным вещам, то, по моему мнению, физики свою работу сделали. Сейчас мы проводим модернизацию нашей машины, чтобы к лету 2017 г., независимо от финансирования, получить нейтронный пучок, который пригоден для терапии пациентов, с большей глубиной проникновения и т. п. И этот пучок будет идеальным в моем понимании – я не вижу принципиальных идей, которые позволят сделать его лучше. Недаром я добавляю к английскому названию нашего проекта BNCT букву i от слова «идеальный» – iBNCT. Возможно, технически что-то еще можно сделать лучше, но улучшить качество нейтронного пучка на сегодняшнем уровне развития укорительной техники невозможно. Хватит улучшать – пора внедрять!
Физики свое дело сделали
Когда мы еще только планировали свой ускоритель, мы поставили задачу достичь тока протонного пучка 10 мA, а получили поначалу в 100 раз меньше. Такая же история год назад приключилась с нашими японскими коллегами из Университета Цукубы, которым компания Mitsubishi делает подобную машину, но на другом типе ускорителя: при той же плановой цифре они вообще получили 0,1 % от желаемого.
Главная моя мечта тогда была – достичь хотя бы 3 мA, чтобы можно было начать лечить людей. И вот к началу 2015 г. мы получили сразу 5 мA, в 50 раз увеличив ток! Фактически сегодня уже не конструкция ускорителя лимитирует возможность дальнейшего увеличения тока. К тому же, по моему мнению, этих характеристик более чем достаточно для медицинских целей. Тем не менее в следующем году мы планируем достичь заявленной цифры – это уже дело принципа.
ИДЕАЛЬНАЯ МИШЕНЬ Воздействие мощного протонного пучка приводит к разогреву облучаемого материала, а так как температура плавления металлического лития составляет всего 182 °С, требуется очень эффективный теплосъем. Первоначально для охлаждения мишени использовали жидкий галлий, но впоследствии ограничились обычной водой. В результате удалось подобрать условия, позволявшие сохранять литий в твердом состоянии, что ограничило распространение радиоактивного изотопа бериллия-7, неизбежно образующегося вместе с нейтронами.
Еще одна ахиллесова пята литиевой мишени – сопутствующее паразитное гамма-излучение. Эффективная генерация эпитепловых нейтронов происходит только в очень узком поверхностном слое лития, поэтому по мере продвижения протонов вглубь нейтроны перестают генерироваться, а гамма-кванты по-прежнему излучаются. Оказалось, что уровень гамма-радиации существенно уменьшается, если дальнейшее торможение протонов происходит не в литии, а в более тяжелом металле. Для этого тонкий (50—100 мкм) слой металлического лития наносят на подложку.
Однако протоны, «проскочившие» литиевый слой, при торможении почти не рассеиваются и «застревают» практически на одной глубине, где со временем накапливается водород. При росте давления газа поверхность мишени начинает вспучиваться. В ходе экспериментов исследователям удалось подобрать максимально устойчивый материал подложки – при клиническом использовании такую мишень достаточно менять раз в неделю
Следующей мечтой стало доказать пригодность нашей машины с точки зрения не только физики, но и потребителя. Для этого нужно было поработать с клеточными культурами и лабораторными животными. Чтобы решить первую задачу, мы завели дружбу с японским Университетом Цукуба, при котором есть известная медицинская клиника. О ней могу лишь сказать, что протонная терапия рака, которая в прошлом году заработала в подмосковном наукограде Протвино, о чем было гордо доложено В. В. Путину, в прайсе этой клиники появилась еще в 1983 г., т. е. 33 года назад! А в 2001 г. японцы заменили протонную установку на более современную.
И вот в июне 2015 г. я встретился с директором клиники Акиро Мацумура, который в числе прочего рассказал, что Mitsubishi никак не может запустить ускоритель для БНЗТ. Так мы договорились о совместной работе. Это сотрудничество – взаимовыгодное. У нас – установка, у японцев – большой опыт проведения подобных исследований и, более того, лечения людей методом БНЗТ на реакторе JRR-4 (Токай), который впоследствии закрыли.
БОРНАЯ «ВЗРЫВЧАТКА» В качестве препаратов нейтронозахватной терапии рака сейчас используются соединения, которые содержат атомные ядра стабильного (нерадиоактивного) изотопа бора-10. Основные требования к таким соединениям – возможность селективного накопления бора в клетках опухоли по сравнению со здоровыми тканями, низкая токсичность и способность растворяться в воде.
Сегодня для БНЗТ обычно используется боркаптат (борный сульфгидрил) и борфенилаланин на основе ароматической аминокислоты. В последние годы в мире активно ведется поиск и синтез новых потенциальных боросодержащих препаратов. В качестве носителей бора тестируются самые разные вещества, как низкомолекулярные (производные аминокислот, предшественника и аналога нуклеиновых кислот, дипептиды, производные сахаров и др.), так и высокомолекулярные, такие как антитела и их фрагменты. Основной задачей по-прежнему остается решение проблемы селективной доставки бора в клетки опухоли и накопление его там в необходимых количествах (около 109 атомов бора на клетку). Для доставки бора в опухоль можно использовать также наночастицы в виде липосом – замкнутых пузырьков с водным содержимым и липидными стенками. Борсодержащие препараты могут включаться как во внутреннюю полость липосом, так и в их оболочку (Шмалько и др., 2013). Недавно ИЯФ СО РАН запатентовал способ доставки борсодержащих препаратов для БНЗТ внутрь опухолевой клетки с помощью модифицированных липосом, в липидную часть которых введен люминесцентный краситель одного цвета, а в водную часть – другого. Контроль доставки препарата производится сопоставлением изображений, полученных в разном цвете (Таскаев и др., 2016)
Для наших исследований были приобретены в Институте цитологии РАН (Санкт-Петербург) четыре клеточные культуры, включая две стандартные контрольные и две – «опухолевые» – глиом и глиобластом человека. С помощью японских коллег и специалистов Института молекулярной и клеточной биологии СО РАН (Новосибирск) были проведены серии экспериментов по облучению этих клеточных культур. Чтобы точно знать концентрацию бора в тканях и клетках – с прицелом на возможную будущую терапию – мы экипировались дорогим (стоимостью около 10 млн рублей) масс-спектрометром японского производства для измерения концентрации растворенных веществ. Купили его на средства гранта РНФ, которые и тратятся преимущественно на приобретение необходимого оборудования.
В конце концов мы получили практически идеальный результат, когда при определенной, достаточно большой дозе облучения выживаемость здоровых клеток падала всего на 5 %, а раковых, в которых накапливался бор, – на 98 %! Этот результат свидетельствует о высоком качестве нейтронного пучка, основную часть которого составляют «правильные» эпитепловые нейтроны, которые захватываются преимущественно атомами бора.
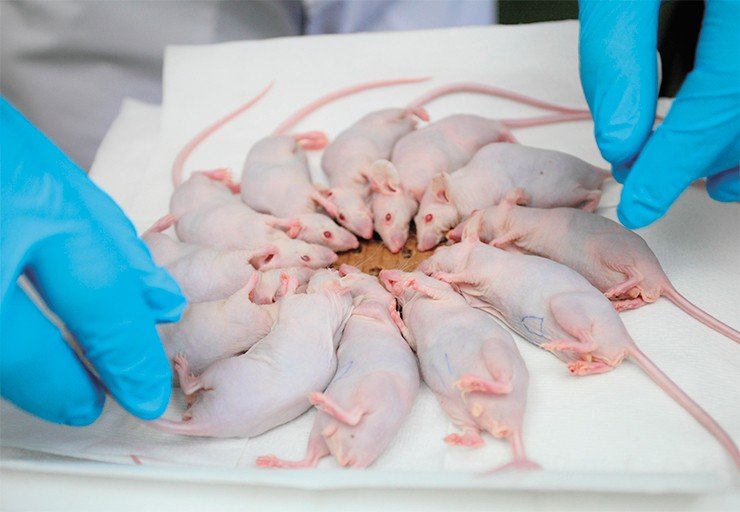
Параллельно со специалистами из Института цитологии и генетики СО РАН (Новосибирск) были проведены эксперименты уже на животных – иммунодефицитных лабораторных мышах, которым в мозг была привита «человеческая» опухоль – глиобластома. Обычно примерно через пять недель такие мыши погибали. Мы решили облучить их (правда, без особой надежды) за 5 дней до дня предполагаемой смерти. Для экспериментов были сделаны специальные контейнеры, с подогревом, куда помещались усыпленные животные.
СТАДИЯ – ДОКЛИНИЧЕСКАЯ На ускорителе ИЯФ проводятся доклинические исследования влияния как нейтронного облучения, так и собственно бор-нейтронозахватной терапии на опухолевые клеточные культуры, а также на лабораторных животных (мышей с врожденным иммунодефицитом).
В исследованиях на клеточных культурах используются различные линии как здоровых, так и опухолевых клеток, которые представлены преимущественно опухолями головного мозга. Клетки инкубируют в среде, обогащенной изотопом бор-10, а после этого облучают на ускорителе. После облучения проводят клоногенный анализ: проверяется жизнеспособность клеток, в частности, их способность делиться и образовывать новые колонии.
На основе экспериментов по облучению животных уже дана оценка последствий воздействия бор-нейтронозахватной терапии в зависимости от дозы облучения. Задача измерения дозы, которую получает пациент при проведении БНЗТ, является одной из самых сложных, поскольку суммарная доза состоит из нескольких компонент, измерение каждой из которых затруднено: от сопутствующих гамма-квантов из литиевой мишени и ускорителя, от быстрых нейтронов, от тепловых нейтронов и от захвата нейтрона бором. Каждая из этих компонент зависит от текущей геометрии литиевой мишени, а также от параметров протонного пучка. Плюс к этому доза от захвата нейтрона бором также зависит еще и от типа, формы и расположения опухоли, а также от распределения бора в ней и в окружающих тканях.
Расчет всех четырех дозовых компонент и предсказание воздействия на здоровые и опухолевые ткани при проведении БНЗТ являются значительно более сложными задачами, чем определение доз в традиционной лучевой терапии, которое обычно опирается на полуэмпирические алгоритмы и измерения в водном фантоме. Одним из вариантов создания эмпирического алгоритма планирования терапии являются эксперименты на лабораторных животных, для которых хорошо известны кривые доза–эффект. То есть по биологическим последствиям облучения в тканях животных можно более точно определять полученную дозу, чем с помощью расчетов.
Все животные без опухоли после облучения остались живы, признаков патологического воздействия на здоровые ткани не обнаружено. Сейчас более углубленно изучается влияние облучения на клеточном уровне, включая процессы кроветворения, состояние тканей жизненно-важных органов и воздействия борсодержащих препаратов на организм животного, чтобы подобрать оптимальную дозу.
После окончательной отработки технологии на животных планируется перейти к клиническим испытаниям, т. е. терапии на пациентах, больных раком.
В самом удачном испытании у трех из пяти животных опухоль рассосалась полностью, что было подтверждено результатами томографии, и животные стали здоровыми – они прожили в виварии еще два месяца и были усыплены просто потому, что результат эксперимента был достигнут. Это поистине фантастический результат. Ведь борфенилаланин, который мы вкалываем, накапливается не только в опухоли, но и в печени и почках. При этом мышь – животное маленькое, поэтому, в отличие от человека, ее облучают целиком, из-за чего больше страдают здоровые ткани. Нужно еще учитывать, что на поздних стадиях развития опухоли в результате гибели раковых клеток может возникнуть масштабный некроз. Но даже при всех этих отягчающих обстоятельствах мы вылечили животных!
Пора внедрять!
БНЗТ на сегодня является новой для нашей страны, перспективной и, главное, проверенной методикой лечения раковых опухолей, так что со стороны государства и крупного бизнеса будет большой глупостью ее не поддержать. Та же Япония сейчас развивает пять вполне успешных проектов по БНЗТ на разных типах ускорителей в рамках сотрудничества государства и таких индустриальных гигантов, как Mitsubishi и Toshiba. Фактически, все это государственные вложения.
Самый короткий и простой для нас путь обеспечить финансирование строительства терапевтической установки БНЗТ – получить грант в рамках прорывного научного проекта на базе программы САЕ (стратегических академических единиц) Новосибирского государственного университета. Согласно проекту, в течение очень небольшого срока (государственное софинансирование рассчитано на 4 года) мы должны будем построить установку непосредственно для медицинского использования и пролечить не менее 10 пациентов. Это достаточно амбициозный план, который будет непросто выполнить, но нам не привыкать ставить перед собой цели, на первый взгляд кажущиеся невыполнимыми. Фактически подготовительная работа по реализации этого проекта уже началась.
Из лекции д.х.н., профессора В. И. Брегадзе (Институт элементоорганических соединений им. А. Н. Несмеянова РАН, Москва):
Нам нужно смотреть в будущее и искать соединения, которые будут более селективно накапливаться в опухоли. Основной принцип их получения – создавать молекулярные конъюгаты из борсодержащего компонента и части, отвечающей за адресную доставку в клетки опухоли. При этом особую важность имеет расстояние между ними, так как активная часть коньюгата может негативно отражаться на свойствах «транспортера».
На роль транспортной молекулы в первую очередь претендуют аминокислоты, а также другие низкомолекулярные соединения (порфирины, нуклеотиды и нуклеозиды, липопротеины и т. п.). Все эти соединения востребованы опухолевыми клетками, имеют к ним сродство и, соответственно, в них накапливаются.
Мы уже получили конъюгаты производных полиэдрических соединений бора с различными порфиринами, конкретно с хлорином Е6. Все синтезированные нами соединения мы отдаем на тестирование в Институт биоорганической химии им. академиков М. М. Шемякина и Ю. А. Овчинникова (Москва), чтобы оценить их накопление в опухолях и здоровых тканях. Исследования показали, что интенсивность накопления борсодержащего конъюгата в клетках карциномы легкого действительно выше в случае большего расстояния между борной частью и молекулой хлорина Е6.
Максимальное соотношение концентраций препарата в опухолевой и здоровой ткани, которого нам удалось добиться на сегодня, равно 5 : 1. Это лучше, чем для использующегося сегодня борфенилаланина (3 : 1),но надо стремиться к большему
В рамках проекта также планируется разработка улучшенного препарата адресной доставки бора – российского аналога борфенилаланина. Этим будет заниматься Институт органической химии СО РАН (Новосибирск), у которого есть свое опытное производство, совместно с Институтом элементоорганических соединений им. А. Н. Несмеянова РАН (Москва).
Как известно, НГУ планирует подать заявку на вторую очередь строительства, которая будет включать создание клиники, где будет практиковаться и БНЗТ. Но это – дело туманного будущего, поэтому в заявке по прорывному проекту университета изложен и другой сценарий. Согласно «запасному» варианту ИЯФ модернизирует одно из своих зданий, где будет размещен ускоритель, а также помещения для приема и лечения больных. Пропускная способность такой установки будет достаточно большой, так как сама процедура БНЗТ длится час, а делается обычно однократно.
Пока мы занимались созданием своей установки – искали идеальные решения, нам «попутно» пришлось решить много проблем, далеко выходящих за рамки ускорительной физики. Вместе с нейрохирургом Владимиром Каныгиным из Дорожной клинической больницы на ст. Новосибирск-Главный ОАО «РЖД» мы разработали и запатентовали систему формирования правильного пучка нейтронов, позволяющую менять его направление. Простое техническое решение, которое удалось найти, не только позволило облучать пациента с любой стороны, но и улучшило качество пучка.
В беседах с нашими японскими коллегами родилась абсолютно новая идея дозиметрии для БНЗТ, на которую уже тоже получен патент. А однажды на лыжне мы разговорились с коллегой по институту Андреем Соколовым, в результате чего появился патент на генерацию монохроматических нейтронов для поиска темной материи. Сейчас вместе с Александром Шмаковым из Института катализа СО РАН и Сергеем Громиловым из Института неорганической химии СО РАН обсуждаем возможность приспособить нашу машину для нейтронной дифрактометрии, которая позволит определять структуру легких элементов вещества.
Все эти идеи, которые мы патентуем, по большому счету очень тривиальны, но почему-то они приходят в голову лишь тому, кто не обогащен грузом опыта, т. е. дилетанту. Как я уже упоминал, именно так была создана наша установка, и я, будучи изначально специалистом по плазме, а не ускорительщиком, честно говоря, до сих пор удивляюсь, как у нас все это получилось.
За последние пять лет мы из специалистов, потенциально привлекательных в области БНЗТ, превратились в реальных игроков на этом поле деятельности. Последний же год мы фактически работали на потребителя. И это очень важно, ведь физики часто думают: вот, мы сделали что-то очень хорошее, почему же пользователи не бегут и не отхватывают это с руками? С таким подходом ничего не получится: надо самому прикладывать много усилий, чтобы работа по внедрению в практику твоих идей и разработок принесла конкретные плоды.
На сегодня в мире с помощью БНЗТ пролечено около двух тыс. человек, для чего использовались уже существующие исследовательские и учебные ядерные реакторы, многие из которых уже не работают. Важность же подобной терапии не нужно объяснять: с ее помощью можно лечить такие практически неизлечимые на сегодня опухоли, как глиобластомы и раковые метастазы. Но до сих пор эта методика остается, по сути, экспериментальной, и специалисты должны приложить еще немало усилий по разработке адекватных стратегий и методик лечения.
Наша установка на сегодня является единственным в мире работающим компактным источником пучка нейтронов, пригодного для БНЗТ. Мы готовы создать действующий медицинский ускоритель, на котором можно будет лечить пациентов уже в ближайшие годы. Но оба наших гранта – от Минобрнауки России на усовершенствование установки и от РНФ для проведения биологических исследований – заканчиваются в декабре этого года. Что будет завтра?
Neutron Capture Therapy: Principles and Applications. Eds.: W. Sauerwein, A. Wittig, R. Moss, Y. Nakagawa. Springer, 2012. 533 p.
Таскаев С. Ю., Каныгин В. В. Бор-нейтронозахватная терапия. Новосибирск: Изд-во СО РАН, 2016. 216 с.
В публикации использованы фото Александра Макарова