Профилактика тэо это что такое
Профилактика венозных тромбоэмболических осложнений при хирургическом лечении пациенток с гинекологическими заболеваниями
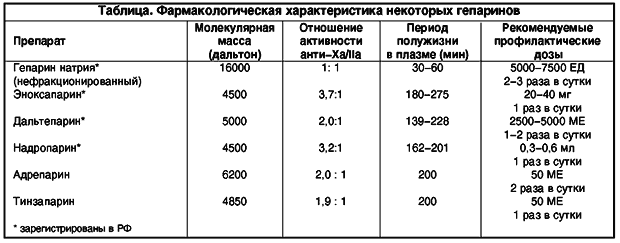
Статья посвящена существующим на настоящий момент мерам профилактики тромбоэмболических осложнений и их эффективности при хирургических вмешательствах, в том числе и в гинекологии в соответствии со стратегией риска. Наибольшие успехи достигнуты при исполь
Венозные тромбоэмболические осложнения (ВТЭО) — собирательное понятие, объединяющее собой тромбоз подкожных и глубоких вен, а также тромбоэмболию легочной артерии (ТЭЛА). В клинической практике врача любой специальности, особенно хирургической, крайне важное значение имеют, в первую очередь, тромбоз глубоких вен (ТГВ) и ТЭЛА, возможности их своевременной диагностики и лечения и, конечно, мер профилактики. Венозный тромбоэмболизм представляет собой одну из наиболее серьезных и, к сожалению, не до конца решенных проблем современной медицины. ВТЭО оказывают значительный социальный и экономический ущерб, характеризуясь высокими показателями как распространенности, так и летальности по всему миру. Ежегодно в мире диагностируется более 900 тыс. эпизодов ТГВ и ТЭЛА, которые становятся причиной около 300 тыс. смертей [1]. После инфаркта миокарда и инсульта тромбоэмболические осложнения являются третьей ведущей причиной смерти среди сердечно-сосудистых заболеваний. Так, по данным E. Oger (2000), J. A. Heit и соавт. (2001), R. H. White и соавт. (2005), ежегодная частота возникновения ТГВ составляет 90–220 случаев на 100 тыс. населения. Точные статистические данные по заболеваемости и смертности от ТЭЛА на сегодняшний день не известны, во многом из-за высокой частоты нефатальных и асимптомных форм. Однако по данным 25-летнего популяционного исследования M. D. Silverstein и соавт. (1998), проведенного в штате Миннесота (США), примерная распространенность ТЭЛА оценивается как 1 случай на тысячу человек населения в год. Другие исследования определяют этот показатель от 0,5 до 2,08 на тысячу населения в год. В США от легочной эмболии как непосредственной причины смерти погибают около 200 тыс. человек в год. Отмечено, что риск ТЭЛА резко возрастает у лиц, находящихся на стационарном лечении, причем независимо от диагноза. P. D. Stein (2004) показал, что среди госпитализированных пациентов распространенность ТЭЛА в США составляет уже 0,4%, по некоторым данным — достигает 12–15% по результатам аутопсии пациентов, умерших в больнице, у онкологических пациентов — на каждой второй аутопсии обнаруживаются признаки тромботических осложнений (Kakkaretal, 1999). Смертность при ТЭЛА достигает 30%, однако адекватная тактика ведения пациента с точной диагностикой и своевременно начатым лечением позволяет снизить этот показатель до 2–8%. В то же время ВТЭО являются потенциально предотвратимыми, подчеркивая значимость профилактических мероприятий.
На сегодняшний день установлено, что ВТЭО является многофакторным заболеванием со сложными механизмами развития. Среди факторов риска — артериальная гипертензия, сахарный диабет, курение, возраст, беременность и роды, злокачественные новообразования, антифосфолипидный синдром, наследственные тромбофилии и др. Для профилактики тромбоэмболических осложнений в настоящее время разработан алгоритм, который включает определение степени риска с учетом общего состояния пациента, его индивидуальных особенностей и соматического здоровья, анамнеза и наследственности, а также оценку объема предстоящей манипуляции или операции и проведение профилактических мероприятий, соответствующих степени риска. Оценку хирургического вмешательства, его длительность и объем необходимо обязательно проводить, так как операция сама по себе значительно повышает риск тромботических осложнений. Более 30% случаев тромбоэмболии легочной артерии и тромбозов глубоких вен непосредственно связаны с общехирургическими вмешательствами, при ортопедических операциях их частота составляет уже около 50% [5]. В 1960-х гг. В. Каккар, используя йод-125-меченный фибриноген, продемонстрировал естественную картину развития тромботических осложнений у 132 больных после оперативного вмешательства. Автором было показано, что тромбы (подтвержденные также флебографически) сформировались в первые 1–3 дня после операции у 40 больных (30%). У 14 из них тромб спонтанно лизировался в течение последующих 72 часов, а у 26 пациентов лизиса не было отмечено. В последней группе из 26 пациентов у 4 развилась ТЭЛА. В настоящее время механизмы тромбообразования изучены более детально. Обширные оперативные вмешательства, как и любой другой род травмы, включают механизм системной воспалительной реакции, заключающийся в выработке и выделении в кровь большого количества биологически активных веществ. Каскад цитокинов активирует лейкоциты и способствует их адгезии к эндотелию сосудов. Выделяемые активированными лейкоцитами мощные оксиданты вызывают гибель эндотелиальных клеток с последующим обнажением субэндотелиального слоя. Кроме того, тромбообразованию способствует выброс тканевого тромбопластина в кровоток непосредственно при иссечении тканей, который существенно активируют систему свертывания, и длительная иммобилизация больных в послеоперационном периоде, способствующая стазу крови в венозном русле [2, 3]. В исследовании White и соавт. (2003), охватившем более 1,6 млн хирургических процедур, было установлено, что важнейшими предикторами развития ВТЭО в первые 3 мес после операции являются возраст (относительный риск (ОР) — 1,1 на каждые 5 лет), венозная тромбоэмболия (ВТЭ) в анамнезе (ОР 6,2) и наличие злокачественного новообразования (ОР 1,7). Хирургическое лечение, применяемое у больных со злокачественными новообразованиями, — дополнительный фактор риска развития тромбоэмболических осложнений, поскольку у таких пациентов система свертывания крови уже оказывается предактивированной ко времени операции. Связь ВТЭО с раком подтверждена документально. Еще в 1865 г. в лекции Арман Труссо описал 3 случая сочетания тромбофлебита и рака. Риск тромбоза среди пациентов с онкологическими заболеваниями приблизительно в 4 раза выше, чем в популяции, и этот риск возрастает в 6–7 раз при проведении как консервативного (химио-, гормоно- и лучевой терапии), так и оперативного лечения. Что же определяет наклонность онкологических больных к тромбозам? В целом ряде случаев это сочетание причин. Многие опухолевые клетки продуцируют тканевой тромбопластин и опухолевый прокоагулянт (цистеиновой транспептидазы). Борьба организма с опухолью сопровождается ростом содержания в крови провоспалительных цитокинов (фактора некроза опухоли альфа, интерлейкинов, интерферона гамма), способных повреждать клетки эндотелия, снижая его противотромботические свойства. Прогрессии тромбоза способствует цитостатическая и гормональная терапия, повреждающая как эндотелий, так и опухолевые клетки с выходом прокоагулянтных субстанций в кровоток [9]. Кроме того, сам по себе рост опухоли может создавать условия для тромбообразования за счет замедления кровотока при сдавлении сосудов и их инфильтрации. Оперативные вмешательства в значительной мере увеличивают риск тромбоза. Исследования, проведенные в ГУ РОНЦ им. Н. Н. Блохина РАМН, показали, что под влиянием оперативного вмешательства уже в начале операции отмечается активизация системы гемостаза, которая нарастает в наиболее травматичный момент и к концу операции. Усиливается общая свертывающая способность крови, повышается содержание маркеров внутрисосудистого свертывания крови и тромбообразования, агрегационная активность тромбоцитов. В послеоперационном периоде гиперкоагуляция нарастает, развивается гиперкомпенсированная форма хронического внутрисосудистого свертывания крови. Указанные изменения способствуют тромбообразованию в глубоких венах нижних конечностей и микроциркуляторном русле жизненно важных органов [1, 4]. Таким образом, оперативные вмешательства на органах малого таза у пациенток с гинекологическими и онкогинекологическими заболеваниями сопряжены с повышенным риском возникновения тромбоэмболических осложнений и требуют обязательного применения мер тромбопрофилактики.
В настоящее время оптимальным следует признать подход, согласно которому профилактику ВТЭО проводят всем больным хирургического профиля, но характер применяемых профилактических мер определяется стратегией риска. Отнесение пациентки к группе с низким, умеренным или высоким риском осуществляется на основании существующих балльных шкал, учитывающих планируемый объем и продолжительность оперативного лечения, соматический статус, анамнез пациентки и другие факторы риска возникновения тромбоэмболических осложнений [2, 7]. В существующих на данный момент протоколах по профилактике тромботических осложнений во всех случаях рекомендуется наиболее ранее прекращение постельного режима и активизация больных после оперативного лечения. Однако у больных с повышенным риском венозного тромбоза (> 0,5%, по шкале Rogers > 7, по шкале Caprini > 0) подобный подход не должен быть единственным способом профилактики, так как не обеспечивает достаточной защиты. У пациенток с низким риском ВТЭО (1,5%, по шкале Rogers 7–10, по шкале Caprini 1–2) рекомендуется использование механических методов профилактики интраоперационно и в послеоперационном периоде. Механические методы включают в себя использование специального противоэмболического компрессионного трикотажа у пациентов с длительным постельным режимом и обычного лечебного и профилактического трикотажа у мобильных больных, обеспечивающие адекватный венозный отток. Эластические бинты могут быть использованы только в случае, когда бандаж создан врачом или обученной медицинской сестрой, владеющими правильной техникой бинтования. В любом другом случае использование эластических бинтов не может считаться методом профилактики ВТЭО и недопустимо в клинической практике. Среди существующих методов механической тромбопрофилактики во всем мире эксперты отдают предпочтение переменной пневматической компрессии, с использованием манжет, воздействующих как только на стопу, так одновременно на стопу и голень. У пациенток с умеренным риском ВТЭО (3,0%, по шкале Rogers > 10, по шкале Caprini 3–4) рекомендуется использование фармакологических методов профилактики (низкомолекулярные гепарины — уровень доказательности 1В) либо механической профилактики (уровень 2С), вместо отсутствия профилактики [6]. У пациенток с высоким риском ВТЭО необходимо использовать фармакологическую профилактику, которую рекомендуется одновременно дополнить механическими методами компрессии. К фармакологическим средствам профилактики тромбозов относятся лекарственные препараты из группы антиагрегантов и антикоагулянтов. Профилактическая эффективность антиагрегантов (ацетилсалициловая кислота) не имеет достаточной доказательной базы, а по имеющимся данным не превышает таковую по сравнению с антикоагулянтами, поэтому их применение не рекомендуется в качестве единственного способа профилактики. В отношении антикоагулянтной терапии доказано, что она позволяет существенно сократить частоту фатальных случаев ТЭЛА, а также снизить риск рецидивов ВТЭО и поздних осложнений. Наибольшие успехи достигнуты при использовании препаратов из класса низкомолекулярных гепаринов (НМГ). По данным многочисленных исследований эти препараты зарекомендовали себя как эффективные и безопасные лекарственные средства по сравнению с другими антикоагулянтными препаратами для профилактики ВТЭО у пациентов не только хирургического, но и терапевтического профиля. НМГ обладают рядом потенциальных преимуществ перед нефракционированным гепарином (НФГ), включая высокую анти-Xa активность, прогнозируемый антикоагулянтный эффект, более длительный период полувыведения, лучшую биодоступность и меньшую частоту развития кровотечений. В рандомизированном многоцентровом исследовании с участием 184 пациентов хирургического профиля низкого и среднего риска развития ВТЭО сравнили эффективность НМГ (бемипарина) со стандартным НФГ. Бемипарин вводился подкожно по 2500 МЕ каждые 24 ч, начиная с первой дозы за 2 ч до начала операции. НФГ назначался в дозе 5000 МЕ подкожно каждые 12 ч. Продолжительность антикоагулянтной терапии составляла в обеих группах 7 дней. В итоге ни в одной группе ТГВ и ТЭЛА отмечено не было, однако были выявлены преимущества бемипарина в плане безопасности использования: уменьшение частоты случаев кровотечений, требующих переливания крови (0 против 9%, p
А. О. Духин, доктор медицинских наук, профессор
В. А. Любешкина 1
ФГБОУ ВПО РУДН, Москва
Abstract. The paper devoted to currently existing measures of prevention of thromboembolic complications and effectiveness in line with the strategy of risk. The greatest success achieved by the use of low-molecular-weight heparins.
Профилактика венозных тромбоэмболических осложнений у госпитальных больных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
РГМУ имени Н.И. Пирогова
Не будет преувеличением сказать, что в госпитальных отделениях любого профиля без труда можно обнаружить пациентов с ВТЭО. При этом клинически диагностируемые тромбозы и эмболии зачастую представляют лишь видимую «вершину айсберга», поскольку в ряде случаев венозный тромбоз протекает бессимптомно, либо диагностируется уже после выписки больного из стационара, а статистические данные учитывают, в основном, массивную легочную эмболию, приведшую к летальному исходу.
Экономические затраты на диагностику и лечение ВТЭО значительны и имеют стойкую тенденцию к увеличению во всем мире. Кроме того, к ним необходимо приплюсовать материальные и моральные потери от длительного и не всегда успешного лечения хронической венозной недостаточности и постэмболической легочной гипертензии, инвалидизации больных, значительного снижения их социальной активности и уровня качества жизни. Классическое утверждение о том, что любую болезнь легче предупредить, чем лечить, в полной мере относится к венозным тромбозам, учитывая их широкое распространение, возможные тяжелые осложнения, серьезные последствия, экономическую и социальную значимость. Между тем эта аксиома пока не стала руководством к действию для всех врачей по отношению к ВТЭО.
Прежде чем говорить о программе профилактики ВТЭО, целесообразно остановиться на группах риска, т.е. тех пациентах, у которых реальна угроза возникновения тромбоза глубоких вен нижних конечностей. Это же определяет возможность развития эмболии легочных артерий, так как тромбоз в системе нижней полой вены служит основным ее источником.
Многочисленные клинические исследования показали, что опасность ВТЭО особенно велика у пациентов:
• в послеоперационном периоде
• с травматическими повреждениями костей и суставов
• соблюдающих постельный режим
• с генетически обусловленными тромбофилиями
• принимающих гормональные препараты, содержащие эстрогены
• беременных (особенно в III триместре) и рожениц.
В свою очередь, на вероятность развития венозного тромбоза в каждой из групп влияют многие факторы: ожирение, возраст, сопутствующие заболевания, принимаемые лекарственные препараты, приобретенные тромбофилические состояния различного генеза и пр. У оперированных больных огромное значение имеют длительность хирургического вмешательства, его объем и травматичность, локальное сдавление сосудов, вид анестезии, степень ограничения подвижности пациента в послеоперационном периоде.
Планируя профилактические мероприятия, которые подразделяют на физические (механические) и фармакологические, следует предусмотреть использование всех возможностей коррекции факторов, определяющих развитие венозного тромбоза.
В первую очередь это относится к послеоперационным тромбозам. Данные анкетирования, проведенного на IX Всероссийском съезде хирургов (Волгоград, 2000 г.), показали, что тромбоэмболии легочной артерии больше, чем кровотечения, опасаются 73% опрошенных. Вместе с тем оценку риска ВТЭО перед операцией всегда проводят лишь 47% клиницистов. Только 19% хирургов в обязательном порядке используют эластическую компрессию нижних конечностей (доступную меру предупреждения тромбоза). Обычно (73%) применение компрессии ограничивают случаями выраженного варикозного расширения вен. К профилактическому назначению антикоагулянтов при высоком риске тромбоза прибегают 63% хирургов. Весьма отрадный факт, тем более что еще несколько лет назад этот показатель не превышал 15%. Тем не менее, еще многие хирурги относятся к массивной тромбоэмболии легочных артерий, развившейся в послеоперационном периоде, как к фатальной неизбежности, не считая ее «своим» осложнением.
В Российской Федерации ежегодно производят свыше 8 миллионов операций, что дает возможность представить, сколь велика совокупность больных, подвергающихся опасности ВТЭО в связи с хирургическим вмешательством. Очевидно, что не у всех оперируемых больных опасность тромбообразования одинаково высока. Соответственно, и объем профилактических мер требуется различный. Для практических целей оправдано подразделение больных на группы низкого, умеренного и высокого риска ВТЭО, в зависимости от состояния больного и факторов, связанных с хирургической агрессией.
Необходимость профилактических мер существует у всех без исключения больных. Однако их объем должен быть адекватен клинической ситуации и экономически оправдан. Целесообразно соблюдать следующие правила:
• Не следует прибегать к антикоагулянтам при отсутствии показаний (реального риска ВТЭО), учитывая возможные осложнения
• При выборе способа профилактики ВТЭО целесообразно учитывать его стоимость и экономическую оправданность.
Меры профилактики должны быть задействованы уже в предоперационном периоде, продолжаться во время и после операции.
Перед плановой операцией эффективной и доступной мерой является активное поведение больного. На это следует обязательно обращать внимание, т.к. небольшое пространство отделения больницы резко ограничивает подвижность пациента. Целесообразно проведение лечебной физкультуры, использование простых тренажеров, частые прогулки хотя бы по коридору отделения. Больного следует заранее предупредить о крайней важности ранней активации в ближайшем послеоперационном периоде, необходимой в первую очередь для ритмичного сокращения икроножных мышц.
Активное поведение больного способствует ускорению кровотока и предупреждает венозный стаз. Этой же цели служит эластическая компрессия ног: эластические бинты или чулки, оказывающие постепенно снижающее от периферии в проксимальном направлении давление.
В группе низкого риска (не осложненные операции продолжительностью до 45 мин. у сравнительно здоровых пациентов) этих неспецифических профилактических мер у подавляющего числа больных оказывается достаточно. Превентивная антикоагулянтная терапия в таких условиях представляется неоправданной по соотношению риск/польза и экономически затратной.
Применение с профилактической целью НФГ возможно, но менее желательно, поскольку он обладает существенно меньшей биодоступностью и мало предсказуемым антикоагулянтным эффектом, чаще вызывает гепарининдуцированную тромбоцитопению и остеопороз. НФГ используют в дозе 5 000 ЕД 2-3 раза в день под кожу живота.
Грубой ошибкой следует признать начало антикоагулянтной профилактики тромбоза через 2-3 дня после операции, как это иногда рекомендуется, т.к. флеботромбоз начинает развиваться раньше, зачастую уже на операционном столе. Лишь в ограниченном числе случаев, при высоком риске интраоперационного кровотечения, можно отложить введение гепарина на несколько часов. В экстренной хирургии, когда не известен коагуляционный потенциал больного, допустимо назначение антикоагулянтов после операции, но не позднее 12 часов после ее окончания.
Воздержаться от введения антикоагулянтов в этой группе пациентов целесообразно лишь при нейрохирургических и офтальмологических вмешательствах, когда даже минимальное кровотечение несет высочайшую опасность. У этих больных следует активно использовать перемежающуюся пневмокомпрессию, тренажеры икроножных мышц.
Существуют еще и так называемые особые случаи, когда хирургическое вмешательство производится на фоне уже имеющегося венозного тромбоза или легочной эмболии. В такой ситуации при флотирующих, эмболоопасных тромбах выполняют имплантацию кава-фильтра или пликацию нижней полы вены, а НМГ или обычный гепарин следует использовать в лечебных дозах.
Считаем необходимым обратить внимание и на чрезвычайную важность максимально ранней активизации больного в послеоперационном периоде, продолжения использования эластической компрессии. В плановой хирургии найдется немного вмешательств, после которых (разумеется, при адекватном обезболивании) нельзя было бы поднять больного на следующие сутки и сделать с ним хотя бы десяток шагов по палате.
Серьезное значение имеет метод анестезиологического пособия. Так, использование регионарной анестезии значительно облегчает течение послеоперационного периода и в несколько раз снижает вероятность развития ВТЭО.
Все вышесказанное служит еще одним аргументом в пользу расширения практики лечения в условиях стационара одного дня, увеличения числа и круга малоинвазивных эндоскопических вмешательств.
Применяющиеся в настоящее время профилактические меры не позволяют в 100% случаев исключить формирование тромбоза в глубоких венах нижних конечностей, однако при их использовании реально минимизировать частоту тромботических осложнений, что позволяет предотвратить, по крайней мере, 2 из 3 летальных легочных эмболий. В Российской Федерации, к сожалению, систематическое профилактическое применение современных антикоагулянтов (НМГ) пока скорее исключение, чем правило. Ссылки на возможность кровотечений на фоне профилактических доз НМГ не имеют аргументированных доказательств, хотя, действительно, в 1-3% случаев возможно возникновение таких осложнений, главным образом в виде раневых гематом. Более тщательный гемостаз решает эту проблему. Вероятность кровотечений не идет ни в какое сравнение с частотой ВТЭО и тяжестью их последствий.
Принципы профилактики ВТЭО в травматологии сходны с таковыми у оперированных больных, поскольку в патогенезе тромбообразования очень много общего. Хочется лишь напомнить, что и без оперативных вмешательств до 10% больных старше 50 лет с переломом шейки бедра умирают от массивной ТЭЛА. Высокий риск развития венозного тромбоза после серьезных травм является основанием для антикоагулянтной профилактики. Ее начинают в течение 36 часов после травмы. Применение НМГ также является предпочтительным по сравнению с обычным гепарином, поскольку они в значительно меньшей степени вызывают остеопороз. Продолжительность использования НМГ не должна быть менее 10 дней. Наряду с этим активно используют массаж стоп и голеней, ранние движения конечностей, максимальное сокращение постельного режима. Применение перемежающейся пневматической компрессии при травмах нижних конечностей иногда невозможно или затруднено.
Обязательно ношение (с I триместра) эластичных бинтов или хорошо подобранного по размеру медицинского компрессионного трикотажа I-II компрессионных классов, значительно улучшающих отток по глубоким венам и препятствующих варикозной трансформации вен подкожных с возможным развитием тромбофлебита. С той же целью рекомендуют подъем ножного конца кровати на 10-15 см. Эластическая компрессия нижних конечностей обязательна и во время родов, а также в послеродовом периоде (4-6 недель).
Немаловажным является предупреждение эмоциональных стрессов у беременных. Стрессовая реакция может вызвать активацию тромбогенного потенциала системы гемостаза и торможение фибринолиза.
После родов гепарин постепенно заменяют на антивитамины К и терапию продолжают, по крайней мере, 4-6 недель, хотя оптимальная длительность этого лечения еще не установлена. В послеродовом периоде следует рекомендовать возможно более раннюю активизацию и лечебную физкультуру.
Наиболее сложной представляется задача предотвращения ВТЭО у больных с генетически обусловленными тромбофилическими состояниями. Задачей, стоящей на повестке дня, следует считать биохимический скрининг таких нарушений. При перенесенном венозном тромбозе у пациентов с некоторыми тромбофилиями (например, дефицит AT-III), возможно, оправдано пожизненное применение наименее токсичных кумаринов (варфарина).
В заключение коснемся экономической стороны проблемы ВТЭО. Антикоагулянтную профилактику многие считают неоправданно дорогой. Действительно, стоимость Клексана на стандартный профилактический курс составляет около 52 долларов США. Однако стоимость лишь консервативного лечения флеботромбоза (не менее 300 долларов), а тем более тромбоэмболии легочных артерий (более 900 долларов), превышает таковую во много раз, даже если не рассматривать затраты на лечение хронической венозной недостаточности в отдаленном посттромботическом периоде. Целенаправленная профилактика ВТЭО позволяет не только сохранить жизнь и здоровье многих тысяч пациентов, но и значительные бюджетные средства российского здравоохранения.
Профилактика тэо это что такое
ГБОУ ВПО «Первый МГМУ им. И.М. Сеченова», Москва Автор для связи: Д.А. Напалков – д.м.н., проф. кафедры факультетской терапии № 1 Первого МГМУ им. И.М. Сеченова; e-mail: dminap@mail.ru
Хроническая сердечная недостаточность (ХСН) характеризуется повышенным риском развития тромбоэмболических осложнений (ТЭО). Этот риск в основном связан с наличием у данной группы пациентов фибрилляции предсердий (ФП) и особенностями их гемостаза. Чем тяжелее СН, тем больше вероятность нарушения ритма сердца. В зависимости от выраженности систолической дисфункции левого желудочка (ЛЖ) частота ФП варьируется от 5 % при легкой степени СН до 50 % у больных тяжелой СН. В соответствии с этим риск развития ТЭО у пациентов с ХСН увеличивается с прогрессированием заболевания [1].
Особенности гемостаза у пациентов с ХСН
Равновесие между факторами, стимулирующими и ингибирующими тромбообразование, является комплексным и многофакторным. Вследствие нарушения систолической функции ЛЖ изменения гемодинамики также являются предрасполагающим фактором к нарушению коагуляции, изменению реологических свойств крови, активации нейрогуморальных факторов, изменению тромбоцитов.
Нарушение реологических свойств крови
У пациентов с систолической дисфункцией ЛЖ изменения реологических свойств крови заключаются в усилении вязкости и развитии стаза крови. Представляется важным наличие патогенетической взаимосвязи между замедлением системного кровотока при систолической ХСН и активацией эндотелийзависимых факторов гемостаза. Снижение скорости кровотока сопровождается уменьшением т. н. напряжения сдвига (shear stress) – скользяще-прижимающего давления потока крови на стенку сосуда, выраженность которого определяет активность эндотелиальной NO-синтетазы – энзима, катализирующего процесс образования эндотелиоцитами оксида азота. В условиях дефицита последнего осуществляется активация молекул адгезии, стимулирующих тромбоцитарное звено гемостаза [2].
Нарушение коагуляции
К нарушениям коагуляции у пациентов с ХСН можно отнести повышение уровня фибриногена комплексов тромбин–антитромбин III, увеличение содержания фибринопептида А- и D-димера.
Повышение вязкости крови, характерное для пациентов с ХСН, связано с возрастанием количества циркулирующего фибриногена [3, 4]. В данном случае его повышение является показателем не только активации свертывающей системы, но и одним из проявлений синдрома иммуновоспалительного ответа [5]. Однако в терминальной клинической фазе ХСН нередко развивается гипофибриногенемия, обусловленная нарушением синтеза фибриногена в печени на фоне гепатоцеллюлярной недостаточности, что можно рассматривать как маркер неблагоприятного прогноза [6].
Фибринопептид А – это пептид, отщепляющийся от фибриногена во время его превращения в фибрин под влиянием тромбина, что приводит к увеличению уровня циркулирующего фибрина. Именно это наблюдается у пациентов с ХСН [7]. Повышенное содержание циркулирующих комплексов тромбин–антитромбин ІІІ отражает степень активации тромбина [8].
Для ХСН различной этиологии характерно возрастание концентрации циркулирующего D-димера – показателя интенсивности расщепления конечного продукта тромбообразования – перекрестно связанного фибрина [7, 8]. Важно, что при ХСН активации ключевого фактора фибринолиза – тканевого активатора плазменогена – сопутствует пропорциональное увеличение активности его ингибитора [9]. В реализации последнего феномена играет роль активация ренин-ангиотензиновой системы, поскольку известно, что ангиотензин ІІ стимулирует ингибитор тканевого активатора плазменогена [10].
Нейрогуморальная активация
В активации коагуляционного каскада при ХСН существенная роль принадлежит повышению активности провоспалительных цитокинов (интерлейкина-1, фактора некроза опухоли α), стимулирующих выработку эндотелиоцитами и макрофагами тканевого тромбопластина – пускового фактора т. н. внешнего пути тромбинообразования [11].
У пациентов с ХСН выявляется постоянная активация ряда факторов первичного гемостаза – эндотелиальных и тромбоцитарных. Повышение в плазме крови концентрации фактора Виллебранда играет ключевую роль в адгезии тромбоцитов к стенке сосуда и участвует в процессе их агрегации. Примечательно, что у больных ХСН выявлена тесная корреляция уровня циркулирующего фактора Виллебранда как с величиной легочно-сосудистого сопротивления и выраженностью дисфункции ЛЖ, так и с концентрацией в плазме эндотелина-1. Последний является одним из ведущих эндотелиальных факторов нейрогуморальной активации при ХСН и одновременно – чувствительным маркером клинического прогноза таких пациентов [7]. При ХСН наблюдают повышение содержания в плазме секретируемых эндотелием молекул адгезии – VCAM-1, E-селектина, а также PECAM-1 – молекулы адгезии, секретируемой как эндотелием, так и тромбоцитами. Активация вышеуказанных факторов отражает изменение т. н. эндотелиального фенотипа при ХСН, являясь элементом системной дисфункции эндотелия, имеющей место при данном синдроме [12].
Изменения свойств тромбоцитов
Уровень циркулирующих маркеров активации тромбоцитов, в частности β-тромбоглобулина, растворимых Р-селектина и остеонектина при ХСН также возрастает. В то же время секреция тромбоцитарного IV фактора (т. н. гепариннейтрализующего протеина) при ХСН, по имеющимся данным, не претерпевает изменений [13].
Вопрос о том, насколько влияет изменение гемостаза на риск развития ТЭО у пациентов с систолической дисфункцией ЛЖ, остается в настоящее время актуальным и недостаточно изученным. Также актуален вопрос о необходимости проведения профилактики ТЭО у пациентов с систолической недостаточностью ЛЖ и сохраненным синусовым ритмом.
Профилактика ТЭО у больных ХСН с сохраненным синусовым ритмом
До настоящего времени не проводились клинические исследования эффективности и безопасности антикоагулянтной терапии пациентов с ХСН неишемической этиологии без ФП.

Новые пероральные антикоагулянты, превосходящие варфарин по соотношению пользы и риска, могут выглядеть более привлекательными для проведения профилактики ТЭО у больных ХСН и синусовым ритмом, но это должно быть подтверждено в клинических исследованиях [15].
Хроническая сердечная недостаточность и фибрилляция предсердий
Обновленные рекомендации ESC по лечению ФП рассматривают систолическую дисфункцию ЛЖ как один из клинически значимых, «небольших» факторов риска ТЭО. Буква «C» в аббревиатуре CHA2DS2-VASc относится к документально подтвержденной умеренной или тяжелой систолической дисфункции ЛЖ, т. е. СН со сниженной фракцией выброса, или к пациентам с недавно возникшей декомпенсацией СН, требующей госпитализации вне зависимости от величины фракции выброса [16]. Методика оценки риска развития инсульта и системных ТЭО по шкале CHA2DS2-VASc представлена в таблице.
Однако проведенный во Франции ретроспективный анализ, в котором сравнивался риск развития ТЭО у пациентов с ФП и ХСН с сохраненной фракцией выброса и систолической недостаточностью ЛЖ, не показал значимого различия риска ТЭО в зависимости от выраженности систолической недостаточности ЛЖ [17].
Сочетание ФП и ХСН, без сомнения, требует проведения профилактики ТЭО. Однако, переходя к выбору конкретного препарата, необходимо учитывать особенности пациентов с ХСН.
Так, необходимо отметить, что при прогрессировании ХСН с развитием гепатоцеллюлярной недостаточности, обусловленной хроническим венозным застоем (а при терминальной ХСН – и гипоперфузией печени), угнетается печеночный биосинтез факторов свертывания крови, в т. ч. и вышеупомянутых, что может обусловливать потенцирование эффекта непрямых антикоагулянтов с соответствующим резким возрастанием риска возникновения жизнеугрожающих кровотечений. Иногда возможна и обратная ситуация: по мере стабилизации гемодинамических показателей, устранения гиперволемии и, соответственно, улучшения функционального состояния печени прежняя доза варфарина может стать недостаточной для поддержания международного нормализованного отношения (МНО) на целевом уровне и поэтому необходима осторожная коррекция дозы в сторону ее увеличения.
В настоящее время в арсенале врача для проведения антикоагулянтной терапии имеются следующие препараты: антагонисты витамина К (варфарин), прямые ингибиторы тромбина (дабигатран), прямые ингибиторы фактора Ха (ривароксабан и апиксабан), причем наличие нарушения систолической функции ЛЖ не влияет на индивидуальный выбор препарата в каждом конкретном случае. В крупных рандомизированных исследованиях по новым антикоагулянтам в подгруппах пациентов, имевших сниженную фракцию выброса ЛЖ, польза от их применения была сопоставимой с пользой от данных препаратов в целом.
На базе Первого МГМУ им. И.М. Сеченова в рамках реализации гранта Президента РФ планируется изучение эффективности и безопасности использования пероральных антикоагулянтов старого и нового поколений для пациентов с ФП и ХСН, требующих профилактики ТЭО из-за высокого риска их возникновения и тщательной оценки безопасности данной терапии из-за высокого риска кровотечений.
Данная публикация выполнена в рамках реализации гранта Президента РФ для поддержки молодых ученых – докторов наук (МД-417.2013.7).