фовеолярная депрессия сетчатки глаза что это такое
Гипоплазия фовеа

Развитие нормальной фовеа
Фовеолярная бессосудистая зона (ФАЗ)
Макулярный пигмент появляется примерно на 17 неделе гестационного возраста и, как полагают, способствует формированию ФАЗ. Его пространственное распределение коррелирует с размером ФАЗ. Ямка состоит из колбочек и клеток Мюллера, палочки в этой зоне отсутствуют. Клетки Мюллера подавляют миграцию астроцитов в центральную ямку, так что образуется зона, свободная от астроцитов, которая играет важную роль в формировании ФАЗ, потому что астроциты вызывают миграцию сосудистых клеток сетчатки.
Развитие фовеолярной ямки
Развитие фовеолярной ямки связано с двунаправленным движением нейронов внутренней и наружной сетчатки. Клетки внутренней сетчатки смещаются центробежно, образуя фовеолярную ямку, а колбочки смещаются центростремительно, так что их плотность в ямке увеличивается.
Заболевания, связанные с гипоплазией фовеа
Альбинизм
Глазокожный альбинизм (ОСА) описывает группу аутосомно-рецессивных наследственных нарушений биосинтеза меланина, которые характеризуются общим снижением пигментации волос, кожи и глаз и различными глазными нарушениями, в т.ч. нистагмом, снижением остроты зрения и светобоязнью. Варианты данного заболевания: OCA1A (наиболее тяжелая форма), OCA1B, OCA1-минимально пигментированная (OCA1-MP), OCA1-чувствительная к температуре (OCA1-TS), OCA2, OCA3, OCA4, OCA5, OCA6 и OCA7.
Глазной альбинизм (X-связанный рецессивный ГА/тип Неттелшопа-Фоллса — Nettleshop-Falls type) затрагивает только глаза. У пациентов с ГА 1 нормальная кожа, которая, однако, может быть несколько бледнее, чем у ближайших родственников. Глазные проявления ГА 1: сниженная острота зрения, аномалии рефракции, гипопигментация глазного дна, отсутствующий фовеолярный рефлекс, косоглазие, прозрачность радужки и задний эмбриотоксон у 30 % пациентов (дисгенез переднего сегмента).
Локус Xp22.3, болеют только мужчины, женщины являются носителями, Следовательно, у мужчин фенотип проявляется полностью, а у женщин-носителей может быть пятнистое глазное дно и гипопигментированные линии на периферии и прозрачная радужка.
Неизвестно, связана ли гипоплазия фовеолярной области в глазах с ГКА и ГА с аномальным синтезом меланина. У пациентов с альбинизмом отсутствует зона без палочек, которая необходима для специализации колбочек. Также недостаточна пигментация макулы, что, как полагают, связано с плохим зрением.
Аниридия
Аниридия вызывается мутациями в гене PAX6. Помимо характерного дисгенеза радужной оболочки симптомы включают низкое зрение и нистагм. Ген PAX6 представляет собой фактор транскрипции, который кодирует ключевой регулятор развития глаза и нерва. Как и у пациентов с альбинизмом, отсутствие макулярного пигмента также характерно для глаз с аниридией.
У пациенты с аниридией часто присутствует гипоплазия фовеа, за исключением гипоморфных мутаций в гене PAX6. У пациентов с фовеолярной гипоплазией были усеченные мутации, то есть нонсенс мутации, сдвиг рамки считывания, сплайсинг или мутации С-концевого удлинения, или делеции генов. Разные ОКТ-изображения волоконного слоя Генле отражают разные степени зрелости фовеа в отношении остроты зрения в глазах с аниридией и изолированной гипоплазией фовеа.
Изолированная гипоплазия фовеа
Это состояние, при котором отсутствуют какие-либо другие глазные проявления. Известно, что гипоморфные мутации гена PAX6 вызывают изолированную фовеолярную гипоплазию, которая имеет аутосомно-доминантное наследование. Пациенты с ОА с мутацией GPR143 могут иметь изолированную гипоплазию фовеа. Недавно были идентифицированы мутации в гене SLC38A8, вызывающие аутосомно-рецессивную изолированную фовеолярную гипоплазию. Ген кодирует предполагаемый натрий-зависимый переносчик аминокислот / протонов. На данный момент было зарегистрировано 11 мутаций в гене SLC38A8 из 11 семейств, и во всех случаях наблюдалась типичная фовеолярная гипоплазия.
Ретинопатия недоношенных
РН – это мультифакторное заболевание, частота возникновения и тяжесть проявления которого обусловлены влиянием множества перинатальных факторов, оказывающих неблагоприятное воздействие на незрелую сетчатку недоношенного ребенка и приводящих к нарушению ее нормального васкулогенеза. Основными из них, показавшими стабильно значимую связь в механизме возникновения РН, являются низкая масса тела при рождении, малый гестационный возраст, длительное дополнительное воздействие кислорода во время выхаживания ребенка, а также медленное увеличение массы тела, развитие респираторного дистресс-синдрома, бронхолегочной дисплазии, сепсиса и других сопутствующих патологий.
Вторичная фиброваскулярная пролиферация приводит к тракционной отслойке сетчатки, которая может привести к слепоте. Высокая экспрессия фактора роста эндотелия сосудов в тканях сетчатки связана с прогрессированием патологии.
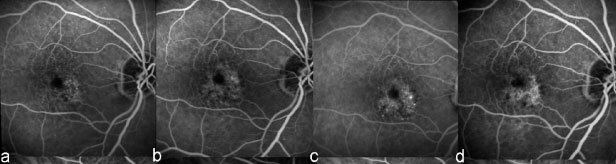
На ОКТ пацеинтов с РН обнаруживаются морфологические аномалии в макулярной области, включая сохранение внутренних слоев сетчатки и отсутствие фовеолярной ной ямки, а также отек макулы. Перифовеолярные капилляры образуются на поздних сроках беременности и недоношенность может повлиять на развитие фовеа. Фоторецепторный слой в ямке тонкий, а диаметр ФАЗ уменьшен. Снижение остроты зрения коррелирует с наличием миопии, а не со структурными изменениями, видимыми на ОКТ. У недоношенных детей отсутствует макулярный пигмент; однако его отношение к остроте зрения неизвестно.
Синдром Блоха-Шульцбергера (синдром недержания пигмента)
Это Х-сцепленное (мутации в гене IKBKG) доминантное заболевание сетчатки, характеризующееся патогномоничными кожными высыпаниями на туловище и конечностях. Заболевание поражает различные ткани эктодермального происхождения, включая сетчатку и центральную нервную систему. Сущность процесса в коже заключается в том, что базальные эпителиальные клетки утрачивают способность удерживать пигмент. Более чем 90 % больных составляют лица женского пола.
Глазные симптомы наблюдаются примерно у каждого третьего больного и отличаются большим разнообразием: микрофтальм, нистагм, птоз, косоглазие, голубые склеры, помутнение роговицы и хрусталика, синехии, атрофия радужки, экссудативный хориоретинит, псевдоглиома, ретролентальная фиброплазия, атрофия зрительных нервов. Нередко основным офтальмологическим проявлением болезни оказывается ретролентальная фиброплазия, осложненная отслойкой сетчатки.
Заболевание связано с окклюзионными изменениями сосудистой сети сетчатки. Макулярные аномалии включают аномальный сосудистый рисунок в парафовеа и фовеальную гипоплазию. Однако более 90% пациентов с синдромом недержания пигмента имеют нормальное зрение, а частоту, тяжесть и нарушения зрения при гипоплазии фовеа еще предстоит определить.
Ахроматопсия
Ахроматопсия – аутосомно-рецессивное заболевание, характеризующееся снижением остроты зрения, нистагмом, повышенной светочувствительностью и отсутствием или снижением цветовосприятия. Состояние вовлекает все три класса колбочек и связано с мутациями в генах CNGB3 и CNGA3, кодирующих катионные каналы, PDE6C и PDE6HI, кодирующих фосфодиэстеразы, и GNAT2, кодирующего альфа-2 субъединицу гуанозин, связывающего G-белки.
Гипоплазия фовеа была обнаружена у 50-80% пациентов с ахроматопсией. Не обнаружено существенных различий в возрасте, контрастной чувствительности, чувствительности сетчатки и стабильности фиксации между пациентами с фовеолярной гипоплазией и без нее. Утолщения внешнего ядерного слоя не наблюдалось. Примечательно, что слой фоторецепторов в ямке был нарушен, включая отсутствие эллипсоидов внутреннего сегмента, гипорефлективной зоны и наличие атрофии.
Гипоплазия зрительного нерва
Семейная экссудативная витреоретинопатия
Семейная экссудативная витреоретинопатия (СЭВРП) — это прогрессирующее наследственное заболевание, обусловленное преждевременной остановкой нормального васкулогенеза на периферии сетчатки у недоношенных детей, которое с течением времени приводит к возникновению отслойки сетчатки. СЭВРП имеет ряд проявлений: от наличия небольшой по площади аваскулярной зоны на периферии сетчатки до выраженной ее аваскулярности с признаками неоваскуляризации, кровоизлияниями в сетчатку, наличием экссудата, тракционной отслойки и амблиопии. В целом клиническая картина СЭВРП в значительной степени повторяет клиническую картину ретинопатии недоношенных (РПН).
Гены, вызывающие СЭВРП, очень гетерогенны, и, помимо очень редких причинных генов, известно, что четыре гена, FZD4, LRP5, TSPAN12 и NDP, вызывают СЭВРП. Основные причинные гены относятся к передаче сигналов Wnt, ключевой регулятор клеточной пролиферации и дифференцировки, а мутации в этих генах составляют
Вторичные пролиферативные изменения на периферии могут повлиять на структуру макулы, что проявляется в виде эктопии макулы и серповидных складок сетчатки. Деформирование макулы затрудняет обнаружение микроструктурных изменений в глазах с СЭВРП. Около 20% глаз с СЭВРП 1 и 2 стадии, т.е. наиболее легкие формы, не сопровождающиеся отслойкой сетчатки, имели сохранение внутренних слоев сетчатки в фовеа, что соответствует легкой фовеолярной гипоплазии. Сохранение внутреннего слоя сетчатки, по-видимому, не вызывает снижения остроты зрения, когда нижележащие наружные структуры сетчатки остаются нетронутыми. Поскольку большинство легких случаев СЭВРП протекает бессимптомно, трудно оценить точную частоту фовеолярной гипоплазии у пациентов с СЭВРП.
Синдром Стиклера (наследственная прогрессирующая артроофтальмопатия) – является наследственным заболеванием соединительной ткани, глазные проявления которого проявляются, как правило, в раннем школьном возрасте. Постепенно развивается миопический астигматизм, имеющих прогрессирующее течение со сферическим эквивалентом близорукости высокой степени. Обычно у детей с данной патологией характерный внешний вид: эпикантус или легкий экзофтальм, низкая переносица, короткий нос и гипоплазия верхней челюсти.
82% глаз с синдромом Стиклера по данным ОКТ имеют постоянство внутренних слоев сетчатки с уменьшенной или отсутствующей фовеолярной ямкой. Кроме того, ОКТ-ангиография показала снижение площади ФАЗ и нарушение капиллярной сети вокруг фовеа. При этом сохраняется довольно хорошая острота зрения, а гипоплазия ограничивается 1 или 2 степенью. Достоверной корреляции между остротой зрения и степенью фовеолярной гипоплазии не выявлено.
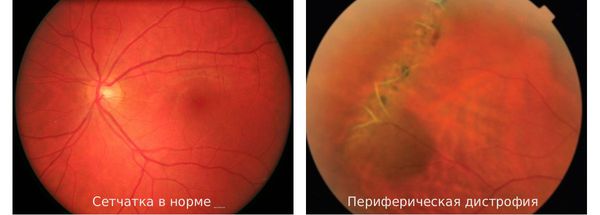
Что такое периферическая дистрофия сетчатки (ПХРД и ПВХРД)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сысоева М. В., офтальмолога-хирурга со стажем в 19 лет.
Определение болезни. Причины заболевания
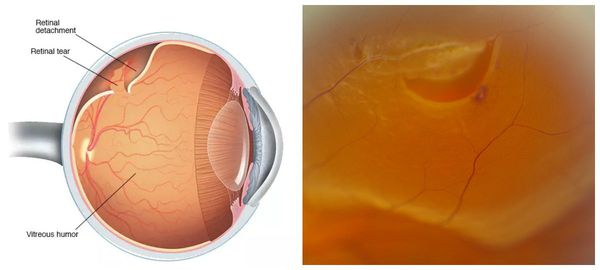
Периферическая дистрофия сетчатки — это патологический процесс, протекающий на периферии глазного дна, в который вовлечены сетчатка глаза, его сосудистая оболочка, а иногда и стекловидное тело. Опасность этого заболевания состоит в высоком риске возникновения отслойки сетчатки.
Причины возникновения периферической дистрофии сетчатки различны. Основная — нарушение гемодинамики (кровообращения) глаза. Так, в связи с растяжением оболочки глазного дна и снижением гемодинамики в области периферии сетчатки у людей с миопией (близорукостью) риск возникновения периферической дистрофии больше, чем у остальных. Это приводит к обменным нарушениям и возникновению дистрофий.
По данным исследований последних лет, нарушения гемодинамики сетчатки с одинаковой частотой встречаются и у лиц с миопией, и у людей с нормальной рефракцией, т. е. тех, кто способен чётко различать отдалённые предметы.
Зрительные перегрузки, физические упражнения, стрессы и другие провоцирующие факторы (например, потужной период в родах) могут привести к дальнейшему истончению сетчатки в уже существующих местах дистрофий и затем к самому грозному осложнению — регматогенной отслойке сетчатки.
Другими причинами, создающими условия для возникновения периферической дистрофии сетчатки, являются:
Во время беременности на фоне гормональной перестройки происходят различные офтальмологические изменения, которые при наличии близорукости также могут в разной степени повлиять на её прогрессирование и появление периферической дистрофии сетчатки:
Симптомы периферической дистрофии сетчатки
Периферическая дистрофия сетчатки является скрытой угрозой здоровью глаз. Её большая опасность состоит в практически полном отсутствии симптомов.
Зачастую человек замечает снижение зрения и может пожаловаться на чёрную пелену перед глазом только тогда, когда отслойка сетчатки захватит макулярную область, которая отвечает за центральное зрение.
Периферическую дистрофию на ранней стадии можно выявить только при врачебном осмотре глазного дна в условиях расширения зрачка. Причём зачастую обнаружение этой патологии происходит случайно, т. е. тогда, когда пациент обращается к офтальмологу по поводу других жалоб.
В некоторых случаях периферические дистрофии сетчатки могут проявлять себя симптомами, на которые мало кто обращает внимание: плавающие “мушки”, полосы, сверкания, вспышки или ”чёрный” дым. Всё это следует рассматривать как повод для скорейшего обращения к специалисту и осмотра глазного дна. [22] [24] [25]
Патогенез периферической дистрофии сетчатки
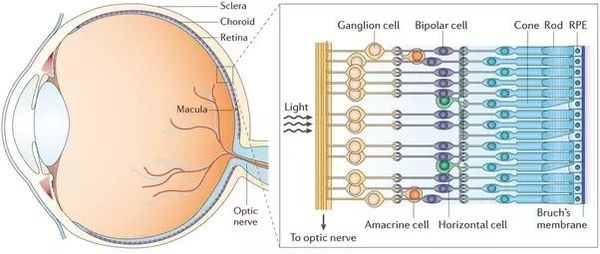
Сетчатка — это внутренняя тонкая оболочка глазного яблока, которая отвечает за зрительное восприятие. Она включает в себя десять слоёв, которые состоят из нервных клеток и их отростков.
Слои сетчатки не везде одинаково плотно прикреплены друг к другу. Внешние и внутренние слои сетчатки прочно соединены между собой в области макулы и вокруг диска зрительного нерва. В остальных зонах соединение слабое, что и создаёт предпосылки для отслойки сетчатки. [7] [14] [16] [21] [23] [28]
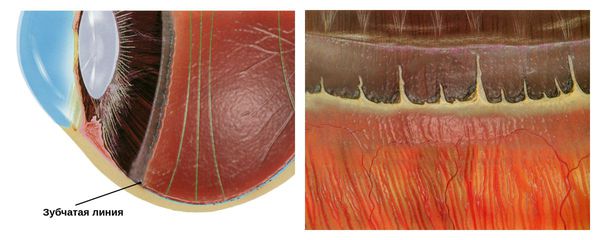
Чаще всего периферическая дистрофия сетчатки локализуется в области зубчатой линии. За её пределами оптическая часть сетчатки заканчивается и переходит в слепую часть.
С некоторыми местами сетчатки, в том числе и в области зубчатой линии, плотно соединена гиалоидная мембрана, покрывающая стекловидное тело. Поэтому при действии неблагоприятных факторов — физической нагрузке, подъёме тяжестей, потужного периода в родах и других — в зоне дистрофии может усилиться тракция (натяжение) со стороны стекловидного тела.
В дальнейшем из-за этого натяжения стекловидное тело «отрывает» часть сетчатки, куда затем начнёт поступать жидкость из супрахориоидального пространства, вызывая отслойку сетчатки, которая будет увеличиваться по площади. При этом подобное состояние, возникающее на периферии сетчатки, не будет давать явных ощутимых симптомов.
Классификация и стадии развития периферической дистрофии сетчатки
Существую разные классификации периферических дистрофий сетчатки. Наиболее подробная, учитывающая вовлечённость стекловидного тела, риски отслойки сетчатки и показания к лазерной коагуляции, является следующая классификация, предложенная Ю.А. Иванишко и соавторами.
По патоморфологии процесса выделяют:
По наиболее вероятному прогнозу периферические дистрофии делят на:
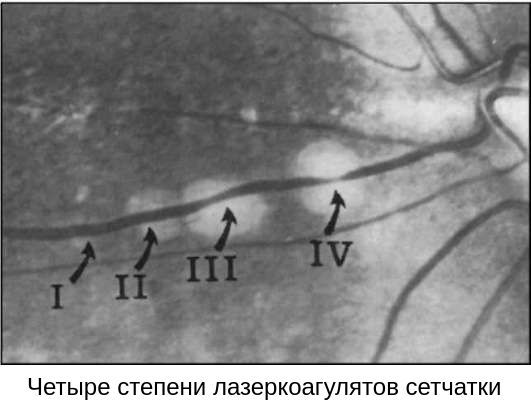
По степени выраженности изменений различают пять стадий.
Виды периферической хориоретинальной дистрофии:
Стадии ПХРД:
Виды периферической витрео-хориоретинальной дистрофии:
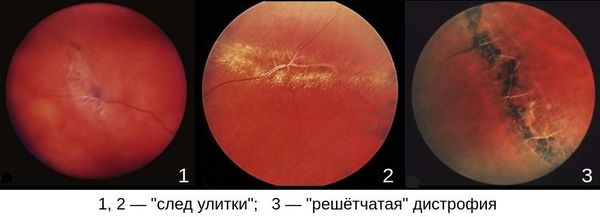
Наиболее опасными являются “решетчатая” дистрофия и дистрофия “след улитки”. [5] [8] [11] [27] [29]
Стадии ПВХРД:
Осложнения периферической дистрофии сетчатки
Возможные осложнения при беременности
Наиболее ранними признаками патологической беременности является ангиопатия — поражение капилляров сетчатки. По мере нарастания сосудистых изменений глазного дна на фоне подъёма общего артериального давления появляются изменения и в зрительном нерве (отёк диска зрительного нерва) и ткани сетчатки (кровоизлияния на сетчатке и фигура «звезды» — тромбоз мелких сосудов, расположенных рядом с макулой, который в дальнейшем может привести к частичному и полному сужению просвета сосуда). Это является «зловещим» признаком и может привести к необратимому снижению зрения. Также в результате выраженных изменений на глазном дне может возникнуть экссудативная отслойка сетчатки. Если же отслойка всё же произошла, то тогда это следует расценивать как абсолютное показание к досрочному прерыванию беременности.
В связи с этим грозным осложнением при близорукости различной степени и периферической дистрофии сетчатки, вызванной миопией, осмотр беременных пациенток должен проводиться в четыре этапа:
Диагностика периферической дистрофии сетчатки
Диагностика периферической дистрофии сетчатки заключается в осмотре периферии глазного дна в условиях мидриаза — расширения зрачка с помощью капель-мидриатиков. Благодаря этим препаратам для осмотра доступны все области сетчатки, вплоть до зубчатого края.
При выраженном мидриазе (6,5-7,0 мм) даже начинающий врач-офтальмолог увидит изменения на периферии сетчатки. Если он не уверен в правильности трактовки и оценке риска выявленных дистрофий, то офтальмолог направляет пациента на консультацию к лазерному хирургу, который уточнит вид дистрофии и определит показания к лазерному лечению. Для этого ему потребуются дополнительные инструменты: трёхзеркальная линза Гольдмана или бинокулярный офтальмоскоп Скепенса.
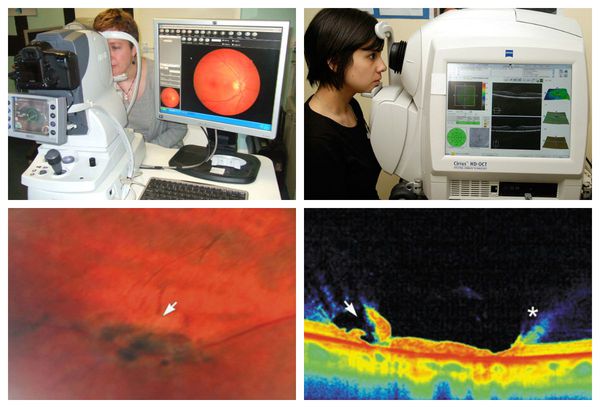
При наличии фундус-камеры лазерный хирург может сфотографировать участок сетчатки, где были выявлены периферические дистрофии, для дальнейшего наблюдения в динамике. Также дополнительную информацию о послойном строении сетчатки в месте дистрофии даст оптическая когерентная томография (ОКТ или ОСТ). [9]
Лечение периферической дистрофии сетчатки
Так как ПХРД указывает лишь на сосудистые и дистрофические изменения сетчатки, возникшие в связи с нехваткой питания, не связана со стекловидным телом и, как правило, не приводит к развитию отслойки сетчатки, то при её обнаружении врач-офтальмолог назначает препараты для улучшения состояния сетчатки (например, витаминно-минеральные комплексы, сосудоукрепляющие и другие группы препаратов).
Для лечения ПВХРД прибегают к отграничительной лазерной коагуляции (ОЛК). Её цель — «склеивание» возможных мест отслоения сетчатки.
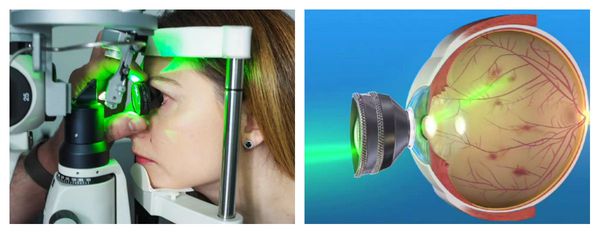
Сама процедура ОЛК выполняется в амбулаторных условиях: пациент сидит за щелевой лампой, к которой присоединён лазерный фотокоагулятор. Предварительно врач проверяет работу аппарата, выставляет рабочие параметры: мощность излучения, длительность экспозиции и диаметр лазерного пятна. В конце процедуры он оценивает полученное количество коагулятов (микроспаек).
Параметры лазерного воздействия подбираются с учётом индивидуальных особенностей: пигментации глазного дна и прозрачности преломляющих сред. Так, при наличии помутнений в хрусталике мощность излучения будет больше.
После закапывания в глаз анестетиков на глаз устанавливается специальная трёхзеркальная линза Гольдмана, поворачивая которую лазерный хирург находит нужный участок периферической дистрофии и производит саму лазерную коагуляцию.
ВАЖНО: в момент проведения процедуры нельзя делать резких движений глазом или отклоняться нужно чётко выполнять все команды хирурга. Иначе луч может попасть в другое место сетчатки, повредив его.
Как правило, среднее время лазерной коагуляции составляет от 5 до 15 минут в зависимости от количества зон периферической дистрофии, прозрачности сред и места расположения зон дистрофии. Сама процедура легко переноситься пациентом. Иногда возможны ощущения в виде кратковременных “покалываний” внутри глаза.
После проведения лазерной коагуляции производится инстилляция противовоспалительных капель и корнеопротектерных гелей. Пациенту выдается памятка с назначениями и рекомендациями в послеоперационном периоде, которые нужно соблюдать, как правило, до двух недель. В этот период обязательно:
Через две недели лазерный хирург повторно проводит осмотр глазного дна в условиях расширения зрачка и на основании оценки состояния лазерных коагулятов выносит решения о дальнейших рекомендациях.
В случае если все зоны периферической дистрофии сетчатки отграничены несколькими рядами хорошо пигментированных лазерных коагулятов (II-III степень пигментации), лечение считается завершённым, но при этом необходим осмотр глазного дна в динамике через несколько месяцев.
Тактика ведения родов у беременных с периферической дистрофией
Оптимальный сроки проведения лазерной коагуляции сетчатки при беременности — до 37 недели, так как, по мнению многих авторов, после этого периода отсутствует достаточный срок для образования прочной спайки между сетчаткой и сосудистой оболочкой.
При выявлении ПВХРД после 37 недели рекомендуются проведение родоразрешения через естественные родовые пути с исключением или ограничением потужного периода, а у беременных с ПВХРД, выявленными после 37 недели, сочетающимися с низкой акустичной плотностью склеры и снижением микроциркуляции, рекомендуется родоразрешение с медикаментозным снижением интенсивности потуг с помощью эпидуральной анестезии. [20]
Прогноз. Профилактика
При своевременном выявлении периферической дистрофии и проведении лазерной коагуляции сетчатки прогноз относительно хороший, так как всё это позволяет предотвратить тяжёлые осложнения (прежде всего, отслойку сетчатки). В некоторых случаях — при наличии множественных зон ПВХРД, неполной зоны коагуляции или слабой выраженности коагулятов — может потребоваться проведение дополнительной лазерной коагуляции:
Чтобы предотвратить периферическую дистрофию ещё на этапе её формирования, необходимо принимать меры по профилактике прогрессирования миопии и её лечению, особенно в школьном возрасте:
Беременным женщинам с близорукостью обязательно нужно пройти осмотр офтальмолога для уточнения наличия ПХРД или ПВХРД.
Возрастная макулярная дегенерация
Возрастная макулярная дегенерация (возрастная макулярная дистрофия, ВМД) – заболевание органа зрения, поражающее центральную область сетчатки (макулу), приводящее к потере центрального зрения.
Факторы риска ВМД
ВМД занимает одну из лидирующих позиций среди причин слепоты и слабовидения у взрослого населения. Среди факторов риска возникновения заболевания рассматриваются:
Симптомы ВМД
На ранних стадиях заболевания человек может не замечать никаких симптомов, но с прогрессированием заболевания могут отмечаться:
Формы ВМД
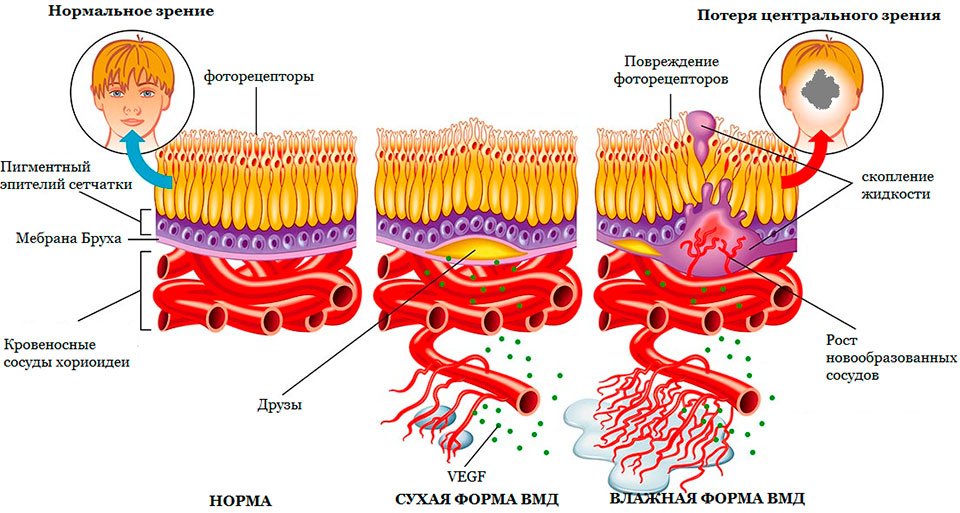
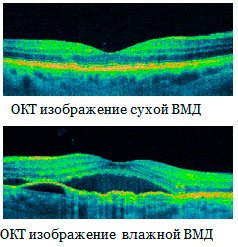
Различают 2 формы ВМД: сухую и влажную.
Под сетчаткой располагается сосудистый слой (хориоидея), состоящий из множества сосудов различного калибра, участвующих в кровоснабжении сетчатки. При ВМД повреждения начинаются с самых наружных слоев сетчатки (пигментного эпителия и мембраны Бруха).
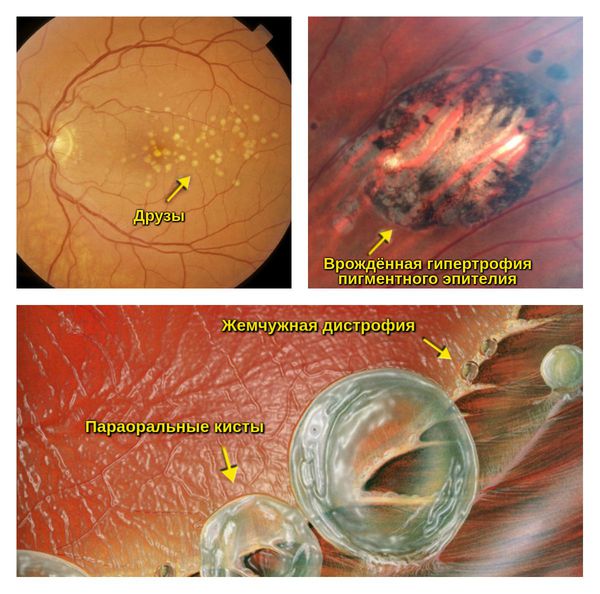
По мере старения в сетчатке накапливаются «продукты жизнедеятельности» глаза, называемые друзами сетчатки – друзы. Они представляют собой скопление желтоватого субстрата под пигментным эпителием сетчатки. Появление множества мелких друз или крупной друзы являются первыми признаками формирования сухой формы ВМД.
Стенки новообразованных хориоидальных сосудов несостоятельны и через них начинает пропотевать плазма крови, вызывая отек сетчатки. Они могут в любой момент разорваться и вызвать кровоизлияние под сетчаткой или в ее слоях. Скапливающаяся жидкость и/или кровь оказывают повреждающее воздействие на фоторецепторы сетчатки, что приводит к снижению зрения, появлению искривлений, искажений изображения. В случае несвоевременно оказанной помощи (или ее отсутствия) возникшее кровоизлияние может спровоцировать формирование рубцовой ткани, что приведет к необратимой потере центрального зрения (темное пятно перед глазом).
Диагностика
В случае возникновения вышеописанных симптомов ВМД следует в срочном порядке обратиться к офтальмологу.
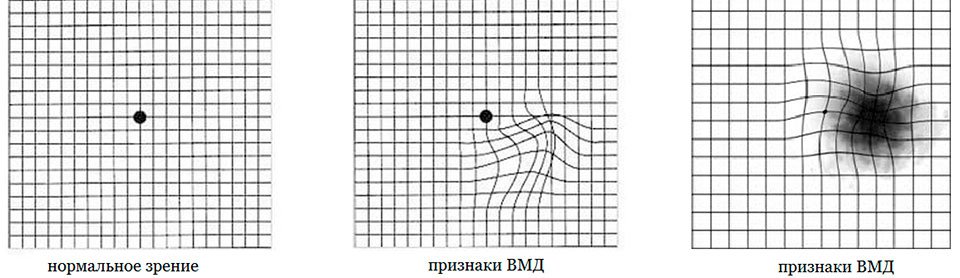
Тест Амслера
Тест Амслера проводится следующим образом:
Если вы заметили, что где-то линии сетки искривлены, изогнуты, форма квадратов деформирована, размеры квадратов неодинаковые, имеются зоны выпадения в сетке, срочно обратитесь к офтальмологу.
Данные изменения могут быть признаками макулодистрофии (ВМД).
Лечение возрастной макулярной дегенерации
В вопросах лечения влажной формы ВМД важным фактором является своевременность оказания врачебной помощи. При промедлении эффективность проводимой терапии снижается, что, в конечном счете, может привести к потере центрального зрения.
Офтальмологи клиники Рассвет проведут все необходимые диагностические обследования. В случае подтверждения диагноза ВМД вам будут даны рекомендации по лечению, в зависимости от формы и стадии течения заболевания. Мы не назначаем курсы так называемого «поддерживающего лечения» сетчатки путем болезненных инъекций в/под глаза препаратов с недоказанной эффективностью. Все рекомендации по лечению и динамическому наблюдению за ВМД даются согласно общепринятым во всем мире стандартам ведения данного заболевания.
Начальные проявления сухой формы ВМД, как правило, не требуют лечения. Рекомендовано динамическое наблюдение за состоянием сетчатки.
Важно отказаться от курения, так как уже доказано, что курение повышает риск возникновения ВМД более чем в 2 раза!
Также рекомендуется придерживаться диеты, богатой антиоксидантами (витамин С, Е, каротиноиды), минералами (селен, цинк), Омега-3 жирными кислотами. К продуктам, которые их содержат, относятся: свежие фрукты и овощи, зелень, жирные сорта рыбы, молочные продукты (творог, сыр, молоко), орехи, бобовые.
Учитывая повреждающее воздействие повышенной солнечной инсоляции на сетчатку, рекомендуется максимальная защита глаз (очки со специальными УФ-фильтрами, головные уборы и другие средства защиты).
В случае дальнейшего прогрессирования заболевания (при более продвинутых стадиях сухой формы ВМД) для снижения рисков перехода во влажную форму возможно применение витаминно-минеральных комплексов с содержанием Лютеина, Зеаксантина, Омега-3 жирных кислот (согласно формулам AREDS 2, Age-Related Eye Disease Study 2).
Влажная форма ВМД – более угрожающее для зрения состояние, чем сухая.
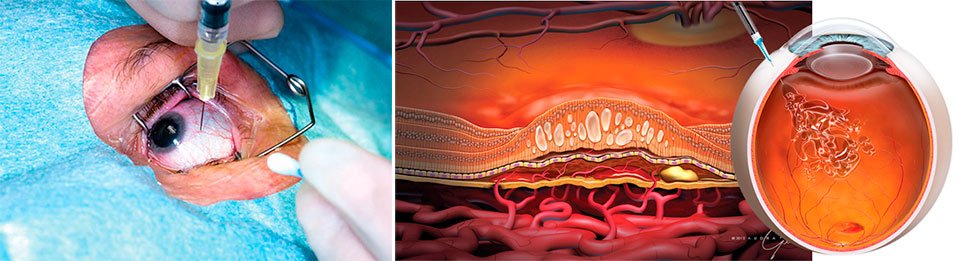
Золотым стандартом лечения влажной формы ВМД являются инъекции в глазное яблоко (так называемые интравитреальные инъекции) специальных лечебных препаратов (ингибиторов ангиогенеза, anti-VEGF препаратов). Стандарт лечения – 3 загрузочные инъекции, которые вводятся с интервалом в 1 месяц первые 3 месяца. В дальнейшем необходимость повторных инъекций решается в индивидуальном порядке согласно течению заболевания и ответной реакции со стороны сетчатки.
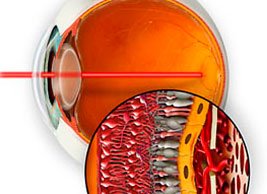
Альтернативным видом лечения определенных видов влажной формы ВМД является фотодинамическая терапия (ФДТ). Суть лечения заключается в ведении в кровоток специального препарата (Вертепорфин/Визудин), который накапливается в патологических новообразованных сосудах. Под воздействием лазерного излучения происходит активация препарата в просвете патологических сосудов, что приводит к их «запаиванию».
Важно понимать, что в вопросе лечения влажной формы ВМД эффективность проводимой терапии определяется сроками оказания лечения.
Чем раньше проведено лечение, тем выше благоприятный исход.
И наоборот, промедление с лечением может привести к необратимой потере центрального зрения. Стоит разъяснить, что в случае ВМД речь не идет о полной потере зрения (полная слепота). При неблагоприятных исходах сохраняется периферическое зрение. Но отсутствие центрального зрения, несомненно, сказывается на его качестве, да и на качестве жизни в целом.
Как лечат ВМД в клинике Рассвет?
Гасанова Замира Эльмановна
офтальмолог