фолликулярный аппарат не развит что это значит
Что такое снижение овариального резерва? Причины возникновения, диагностику и методы лечения разберем в статье доктора Каменецкого Б. А., репродуктолога со стажем в 30 лет.
Определение болезни. Причины заболевания
Распространение вспомогательных репродуктивных технологий привело к тому, что овариальный резерв и его снижение рассматриваются с позиций ответа яичника на воздействие гонадотропных препаратов. Гонадотропины — группа препаратов, оказывающих влияние на половые железы, в том числе способствующие созреванию фолликулов в яичниках. Нормальный овариальный резерв — адекватному ответ яичников на стимуляцию. Под адекватным ответом понимается требуемый рост фолликулов и получение достаточного количества ооцитов. Достаточное количество определяется не столько числом получаемых ооцитов, сколько количеством полученных после оплодотворения эмбрионов с правильным хромосомным набором.
В зависимости от возраста женщины для получения одного нормального эмбриона требуется разное количество ооцитов:
Причины развития СОР можно условно разделить на две группы:
Симптомы снижения овариального резерва
Снижение овариального резерва — процесс, растянутый во времени, которые чаще всего протекает без симптомов. Причиной, заставляющей женщину обратиться к врачу, является отсутствие беременности (бесплодие).
Патогенез снижения овариального резерва
К другим причинам, оказывающим негативное влияние на уровень овариального резерва, относятся:
Классификация и стадии развития снижения овариального резерва
С накоплением данных стало понятно, что в группу пациентов со сниженным овариальным резервом, а как следствие с неадекватным ответом на стимулирующую терапию, включены женщины с разными причинами возникновения и механизмами развития патологии. Это затрудняло планирование адекватной терапии. В связи с этим в 2016 году была сформирована рабочая группа POSEIDON ( Patient-Oriented Strategies Encompassing Individualize Oocyte Number) [37] по разработке новых критериев и классификации пациентов со сниженным овариальным резервом и бедным ответом яичников на стимуляцию.
Чтобы представить более детальную картину, были предложены клинически значимые критерии, которые могут помочь врачу в ведении пациентов. Для определения групп с низким прогнозом на стимуляцию предложены две новые категории [37] :
Первая группа включает количество получаемых при стимуляции ооцитов:
Вторая группа объединяет «качественные» и «количественные» параметры, а именно:
В результате введения этих категорий выделяют четыре группы пациентов со сниженным овариальным резервом и низким ответом на стимулирующую терапию:
Выделение отдельных групп решает практическую задачу — планирование терапии с учётом детальных критериев для пациентов разных этиопатогенетических групп.
Осложнения снижения овариального резерва
Вторым по значимости осложнением является преждевременное истощение яичников и, как следствие, нарушение менструальной функции вплоть до её полного угасания. Снижение овариального резерва приводит к критическому снижению количества ооцитов и нарушение менструального цикла по типу:
Диагностика снижения овариального резерва
Диагностика строится на совокупности анамнестических и клинико-лабораторных данных. Наиболее важным является возраст. Клинические проявления снижения овариального резерва зачастую начинают проявляться после 35 лет.
Очень часто в анамнезе есть упоминания о раннем наступлении климакса у ближайших родственников по женской линии (мать, старшие сестры).
Основными жалобами являются нарушение (чаще сокращение продолжительности и интенсивности) менструального цикла и бесплодие.
Из объективных критериев:
Лечение снижения овариального резерва
Патогенетического лечения не существует. Терапия направлена прежде всего на устранение последствий снижения овариального резерва, а именно преодоления бесплодия.
В программах вспомогательной репродукции в зависимости от принадлежности пациентки к той или иной группе по критериям POSEIDON рассматриваются различные стратегии стимулирующей терапии для получения большего количества ооцитов.
Для первой и второй групп применяется пять основных стратегий отдельно или в комбинациях:
Стратегии, предложенные для стимуляции пациенток третьей и четвёртой групп:
При невозможности получения достаточного количества ооцитов рекомендовано использование донорских ооцитов.
Прогноз. Профилактика
Для профилактики бесплодия рекомендовано:
Профилактика ятрогенных осложнений:
Фолликулометрия
| Наименование услуги | Стоимость |
|---|---|
| Ультразвуковое исследование фолликулогенеза | 1500 руб. |
Уважаемые пациенты! С полным перечнем и стоимостью услуг вы можете ознакомиться в регистратуре или по телефонам
8 (499) 184-55-11, 8 (499) 184-55-77.
Ультразвуковой мониторинг, также называемый «фолликулометрия» — наблюдение за изменениями во внутренних половых органах женщины во время менструального цикла. Оно позволяет узнать произошла ли в течении изучаемого цикла овуляция, а также точный день, когда она случилась. Наблюдение касается также процесса созревания и роста слизистой матки. Чаще всего к ней прибегают при нарушениях менструального цикла, при неудачных попытках забеременеть в течение более 6 месяцев. Для проведения процедуры ультразвукового мониторинга используют ультразвуковой сканер и датчик. В статье подробно описано, что такое фолликулометрия: как ее делают, как подготовиться, показатели.
Для чего проводят УЗ-мониторинг
Подготовка к процедуре
Никаких специальных действий перед процедурой проводить не нужно. Необходимо лишь исключение продуктов, вызывающих сильное газообразование в кишечнике. Абдоминальное УЗ требует наполнение мочевого пузыря. Необходимо за час до исследования выпить литр воды. В случае использования вагинального датчика пить не требуется, напротив, необходимо опустошить мочевой пузырь, так что перед процедурой следует сходить в туалет.
Способы проведения
Существует два типа проведения данного исследования в Москве. Трансабдоминальное (абдоминальное) и с помощью вагинального датчика. В случае первого типа исследования вам надо будет лечь на спину и открыть живот от груди до лобковой части. Датчик водят по стенкам живота. Вагинальный датчик вводят во влагалище с надетым на него презервативом.
Когда проводится
Точное время исследования назначает врач. Он вычисляет его по менструальному циклу. Всего проводится 4 и более таких исследований. При 28 дневном цикле исследовании назначается на 7-10 день после его начала. То есть минимум спустя неделю после начала месячных. Далее процедура исследования проводится спустя 1-2 дня и так несколько раз подряд. В случае если цикл длиннее, исследование проводят на 10 день, промежуток между процедурами остается таким же.
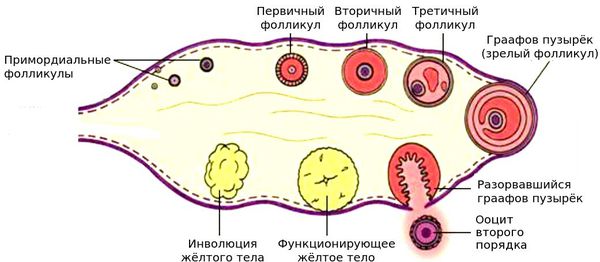
Репродуктивная система
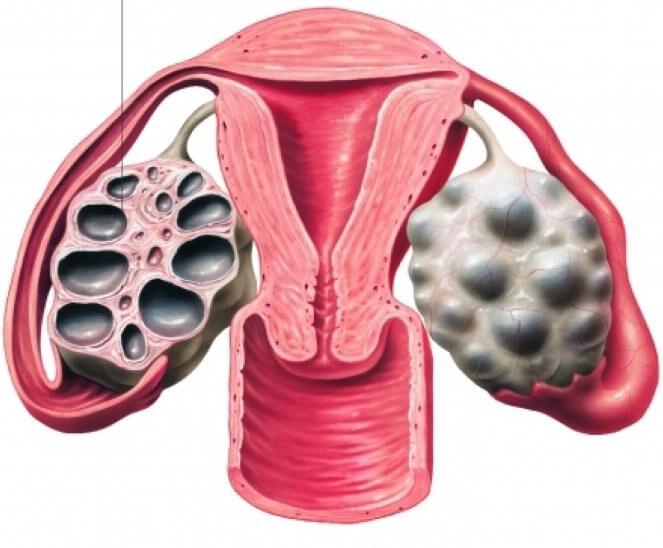
Фолликулярным аппаратом называется несколько сотен несозревших фолликулов. В организме женщины они появляются еще в утробе. В любой из циклов менструации к овуляции начинает подходить небольшое их количество, затем один фолликул начинает быть потенциальным производителем яйцеклетки. Такие фолликулы называются доминантными. Из яичника он попадает в брюшную полость, где ждет встречи со сперматозоидом. Овуляцией называют вывод созревшей яйцеклетки из яичника. Фолликул при овуляции лопается, на этом месте появляется тело, называемое временной эндокринной железой. Ее функционирование продолжается до наступления месячных, либо до появления плаценты при возникновении беременности. Во время некоторых циклов яйцеклетка не созревает, беременность в это время невозможна. Если УЗ-наблюдение показало «обедненный фолликулярный аппарат», это означает, что в яичниках женщины малое количество фолликулов. Чтобы создать возможность забеременеть, необходимо выявление и лечение причин этого явления в Москве.
Расшифровка результатов
Подобное исследование помогает сделать вывод не только об эхографических изменениях в репродуктивных органах, но и включает в себя анализ половых гормонов, а также гормонов щитовидной железы. Врач делает заключение на основании уз и лабораторного исследования. Заключения могут быть следующими:
Согласно отзывам, данное исследование полезно для желающих забеременеть женщин. Ультразвуковой мониторинг позволяет с точностью определить шансы забеременеть и причины, по которым беременность не происходит. Оно гораздо эффективнее устаревших методов. Лечение бесплодия также успешно контролируется при помощи данного исследования.
Фолликулометрия
Фолликулометрия — это один из самых эффективных способов определения овуляции, ее рекомендуют пройти женщинам, страдающим бесплодием или нарушениями менструального цикла. Этот метод диагностики применяют тогда, когда другие не подходят.
Что такое фолликулометрия? Это наблюдение в динамике за изменениями в органах женской репродуктивной системы в течение всего менструального цикла.
Диагностика позволяет определить, был данный цикл овуляторным или нет, в какой день овуляция имела место. Также проводится наблюдение за созреванием и ростом эндометрия, то есть функциональной слизистой оболочки матки.
Для диагностики используется ультразвуковой сканер и датчик. Процедура ничем не отличается от УЗИ, которое применяется в акушерстве и гинекологии.
Цели проведения фолликулометрии:
Сроки проведения процедуры
Обычно фолликулометрия проводится с 7 по 10 день цикла. Обычно нужно несколько исследований с интервалом 1-2 дня (по результатам предыдущего исследования).
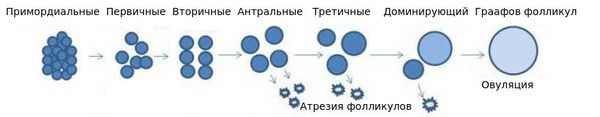
Физиология женской репродуктивной системы
Каждый менструальный цикл процесс подготовки к овуляции начинает проходить сначала несколько фолликулов. Затем, под воздействием гормонального фона, главным кандидатом в производители яйцеклетки становится только один из них (реже – несколько).
Он называется доминантным. Он выходит из своего «убежища» в яичнике в брюшную полость, должен быть уловленным ворсинками маточных труб и попасть в их полость, где и встретиться со сперматозоидом. Процесс выхода зрелой уже яйцеклетки из яичника называется «овуляция».
На месте фолликула, лопнувшего в результате овуляции, развивается желтое (лютеиновое) тело – временная эндокринная железа. Оно функционирует или до наступления менструации, или, если беременность возникла, до появления плаценты (на 12-16 неделе).
Бывают циклы, когда созревания яйцеклетки не происходит. Они называются «ановуляторными», с возрастом их становится все чаще. Во время такого цикла забеременеть невозможно.
Заключение УЗИ «обедненный фолликулярный аппарат» означает, что под воздействием таких причин:
в яичниках находится мало фолликулов. Для того, чтобы беременность наступила, нужно эту причину обнаружить и пролечить (или исключить воздействие вредных факторов, отменить препараты).
Это исследование включает в себя не только наблюдение за эхографической картиной изменений в матке и яичниках. Проводится также лабораторное определение уровня женских половых и некоторых других гормонов (например, тех, которые вырабатывает щитовидная железа). На основании ультразвукового и лабораторного исследований врач выдает заключение, которое может быть таким:
Нормальная овуляция. Для нее характерны такие признаки:
Персистирующий фолликул. Этот диагноз означает, что хоть и доминантный фолликул полностью созрел, овулировать он не стал. Такая ситуация может сохраняться и после месячных. Признаки этого состояния:
Киста фолликулярная. Это состояние, когда фолликул не только не овулировал, но и вырос в размерах (больше, чем 25 мм). Признаки такой кисты:
Лютеинизация фолликула: фолликул образовался, не овулировал, но на его месте все равно образовалось желтое тело. Признаки:
Нет развития фолликулов:
Фолликулометрия позволяет контролировать эффективность лечения по поводу бесплодия.
Синдром поликистозных яичников или мультифолликулярные яичники
Врачи на УЗИ нередко видят достаточно типичную картину, которую называют мультифолликулярными яичниками. Для некоторых пациенток мультифолликулярные яичники — синоним поликистоза, при котором также много фолликулов. Между тем, это совершенно разные понятия.
Для начала опишем УЗИ-картину яичников при поликистозе:
Однако описанная картина иногда бывает лишь ошибочно похожа на поликистозные яичники. Например, весьма похожая картина может быть в 1 фазе цикла (на 5-7 день) вследствие чисто физиологических изменений, которые естественно протекают в половой системе женщины. Кроме того, подобные изменения бывают у женщин на фоне длительного приема оральных контрацептивов, в рамках гипогонадотропной аменореи и, наконец, у девушек в периоде полового созревания.
Таким образом, мультифолликулярные яичники — лишь ультразвуковой симптом менструального цикла в рамках нормы. Однако, учитывая, что картина может быть нечеткой, что есть определенные варианты течения поликистоза яичников, при выявлении картины мультифолликулярных яичников необходимо провести дифференциальную диагностику. Для этого исследуют содержание в крови ЛГ и ФСГ, тестостерона, инсулина. При мультифолликулярных яичниках уровень этих гормонов находится в пределах нормы. А при поликистозе яичников соотношение ЛГ/ФСГ больше 2,5-3, увеличен уровень общего и свободного тестостерона, а также инсулина. Кроме того, о наличии поликистозных яичников свидетельствует также и клиническая картина заболевания.
То же относится и к девушкам периода полового созревания, у которых состояние называют также «формирующийся синдром поликистозных яичников». У них специфическую ультразвуковую картину сопровождают специфические гормональные и внешние изменения.
Таким образом, мультифолликулярные яичники — диагноз не заболевания, а определенного состояния, которое само по себе не является причиной бесплодия, нарушений менструального цикла и т.д. Но проводить дифференциальный диагноз с более тяжелыми состояниями все-таки необходимо.
Для дифференциальной диагностики мультифолликулярных и поликистозных яичников можно использовать следующие признаки:
Часто мультифолликулярные яичники принимают за поликистозные яичники, однако мультифолликулярные яичники следует рассматривать как вариант нормы, а поликистоз яичников — заболевание.
Женские половые органы – яичники, маточные трубы, матка, подвержены изменениям в зависимости от фазы менструального цикла. В начале менструального цикла в яичниках начинают созревать 5-7 фолликулов, но дозревает только один из них. При картине мультифолликулярных яичников одновременно дозревают более 7 фолликулов. Мультифолликулярные яичники часто встречаются в начале полового созревания, когда только устанавливается менструальная функция, у женщин длительно принимающих пероральные контрацептивы, а также на 5-7 день нормального менструального цикла. Иногда синдром мультифолликулярныхяичников может сопровождаться нарушениями менструального цикла, чаще всего это связано с недостаточностью лютеинизирующего гормона, что может быть вызвано резкой потерей веса, или наоборот его набором. При этом может наблюдаться аменорея или олигоменорея. Нарушения менструального цикла, сопровождающие мультифолликулярные яичники, может свидетельствовать о начальной стадии поликистоза яичников.
Часто, только лишь по данным УЗИ, бывает сложно отдифференцировать синдром мультифолликулярный яичников от синдрома поликистозных яичников. В таких случаях, необходимо динамическое наблюдение у гинеколога и определение гормонального фона. Однако, есть ряд УЗИ-признаков, отличающих мультифолликулярные яичники от поликистозных. Главным отличительным признаком является размер яичника, при синдроме мультифолликулярных яичников он нормальный, при поликистозных яичниках увеличен. Количество фолликулов при синдроме мультифолликулярных яичников 8-10, диаметр фолликулов 4-8 мм, приполикистозе более 10, диаметр фолликулов более 10 мм. Мультифолликулярные яичники не сопровождаются гормональными нарушениями, в отличии от поликистозных яичников.
Причины СПКЯ
СПКЯ – часто распространенное гормональное расстройство среди женщин репродуктивного возраста, приводящее к стойкому бесплодию. Несмотря на актуальнось проблемы, точные причины возникновения СПКЯ до сих пор неизвестны.
Помимо гормональных причин, к предрасполагающим факторам, ведущим к развитию СПКЯ, относят:
Симптомы СПКЯ
Молочные железы развиты правильно, у каждой третьей женщины имеет место фиброзно-кистозная мастопатия, развивающаяся на фоне хронической ановуляции и гиперэстрогении.
Практически все пациенки с СПКЯ имеют повышенную массу тела. При этом излишки жира откладываются, как правило,на животе (“центральный” тип ожирения). Поскольку уровень инсулина при СПКЯ повышен, довольно часто заболевание сочетается с сахарным диабетом 2 типа. СПКЯ способствует раннему развитию сосудистых заболеваний, таких какгипертоническая болезнь и атеросклероз.
Поскольку симптомов заболевания много, СПКЯ легко можно перепутать с любым дисгормональным нарушением. В молодом возрасте жирную кожу, угри и прыщи принимают за естественные возрастные особенности, а повышенная волосатость и проблемы с лишним весом зачастую воспринимаются как генетические особенности. Поэтому если менструальный цикл не нарушен и женщина еще не пробовала беременеть, то к гинекологу такие пациентки обращаются редко. Важно знать,что любые подобные проявления не являются нормой и при обнаружении у себя подобных симптомов следует очно проконсультироваться у гинеколога-эндокринолога.
Диагностика СПКЯ
Структурные изменения яичников при СПКЯ характеризуются:
Диагностика СПКЯ включает:
После пробы с дексаметазоном содержание андрогенов незначительно снижается, примерно на 25% (за счет надпочечниковой фракции).
Проба с АКТГ отрицательная, что исключает надпочечниковую гиперандрогению, характерную для адреногенитального синдрома. Отмечено также повышение уровня инсулина и снижение ПССГ в крови.
В клинической практике простым и доступным методом определения нарушения толерантности глюкозы к инсулину является сахарная кривая. Определяется сахар крови сначала натощак, затем — в течение 2 ч после приема 75 г глюкозы. Если через 2 ч уровень сахара крови не приходит к исходным цифрам, это свидетельствует о нарушенной толерантности к глюкозе, т. е. об инсулинрезистентности, что требует соответствующего лечения.
Критериями для постановки диагноза СПКЯ являются:
Лечение СПКЯ
Лечение СПКЯ определяется с учетом выраженности симптомов и желанием женщины забеременеть. Обычно начинают с консервативных методов лечения, при неэффективности показано хирургическое лечение.
Если у женщины имеется ожирение, то лечение следует начать с коррекции массы тела. В противном случае консервативное лечение у таких пациенток не всегда дает желаемый результат.
При наличии ожирения проводятся:
Консервативное лечение СПКЯ
При нарушенном углеводном обмене лечение бесплодия начинают с назначения гипогликемических препаратов из группы бигуанидов (Метформин). Препараты корректируют уровень глюкозы в крови, курс лечения составляет 3-6 месяцев, дозы подбирают индивидуально.
Для стимуляции овуляции применяют гормональный препарат-антиэстроген Кломифен-цитрат, который стимулирует выход яйцеклетки из яичника. Препарат применяют на 5-10 день менструального цикла. В среднем, после применения Кломифена овуляция восстанавливается у 60 % пациенток, беременность наступает у 35 %.
При отсутствии эффекта от Кломифена, для стимуляции овуляции применяют гонадотропные гормоны, такие как Пергонал, Хумегон. Стимуляция гормонами должна проводится под строгим контролем гинеколога. Эффективность лечения оценивают при помощи УЗИ и показателей базальной температуры тела. Если женщина не планирует беременность, для лечения СПКЯ назначают комбинированные оральные контрацеативы (КОК) с антиандрогенными свойствами для восстановления менструального цикла.Такими свойствами обладают КОКи Ярина, Диане-35, Жанин, Джес. При недостаточном антиандрогенном эффекте КОКов, возможно совместное применение препаратов с антиандрогенами (Андрокур) с 5 по 15-й день цикла. Лечение проводят с динамическим контролем показателей гормонов в крови. Курс лечения составляет в среднем от 6 месяцев до года.
Высоким антиандрогенным свойством обладает калийсберегающий диуретик Верошпирон, который также используют при поликистозе яичников. Препарат снижает синтез андрогенов и блокирует их действие на организм. Препарат назначают минимум на 6 месяцев.
Стимуляция овуляции при СПКЯ
Кломифен относится к нестероидным синтетическим эстрогенам. Механизм его действия основан на блокаде рецепторов эстрадиола. После отмены кломифена по механизму обратной связи происходит усиление секреции ГнРГ, что нормализует выброс ЛГ и ФСГ и, соответственно, рост и созревание фолликулов в яичнике. Таким образом, кломифен не стимулирует яичники непосредственно, а оказывает воздействие через гипоталамо-гипофизарную систему. Стимуляция овуляции кломифеном начинается с 5-го по 9-й день менструального цикла, по 50 мг в день. При таком режиме повышение уровня гонадртропинов, индуцированное кломифеном, происходит в то время, когда уже завершился выбор доминантного фолликула. Более раннее назначение кломифена может стимулировать развитие множества фолликулов и увеличивает риск многоплодной беременности. При отсутствии овуляции по данным УЗИ и базальной температуры дозу кломифена можно увеличивать в каждом последующем цикле на 50 мг, достигая 200 мг в день. Однако многие клиницисты полагают, что если нет эффекта при назначении 100-150 мг кломифена, то дальнейшее увеличение дозы нецелесообразно. При отсутствии овуляции при максимальной дозе в течение 3 месяцев пациентку можно считать резистентной к кломифену.
Критериями эффективности стимуляции овуляции служат:
При наличии этих показателей рекомендуется введение овуляторной дозы 7500-10000 МЕ человеческого хорионического гонадотропина — чХГ (профази, хорагон, прегнил), после чего овуляция отмечается через 36-48 ч. При лечении кломифеном следует учитывать, что он обладает антиэстрогенными свойствами, уменьшает количество цервикальной слизи («сухая шейка»), что препятствует пенетрации сперматозоидов и тормозит пролиферацию эндометрия и приводит к нарушению имплантации в случае оплодотворения яйцеклетки. С целью устранения этих нежелательных эффектов препарата рекомендуется после окончания приема кломифена принимать натуральные эстрогены в дозе 1-2 мг. или их синтетические аналоги (микрофоллин) с 10-го по 14-й день цикла для повышения проницаемости шеечной слизи и пролиферации эндометрия.
При недостаточности лютеиновой фазы рекомендуется назначить гестагены во вторую фазу цикла с 16-го по 25-й день. При этом предпочтительнее препараты прогестерона (дюфастон, утрожестан).
Частота индукции овуляции при лечении кломифеном составляет примерно 60-65%, наступление беременности — в 32-35% случаев, частота многоплодной беременности, в основном двойней, составляет 5-6%, риск внематочной беременности и самопроизвольных выкидышей не выше, чем в популяции. При отсутствии беременности на фоне овуляторных циклов требуется исключение перитонеальных факторов бесплодия при лапароскопии.
При резистентности к кломифену назначают гонадотропные препараты — прямые стимулятороы овуляции. Используется человеческий менопаузальный гонадотропин (чМГ), приготовленный из мочи женщин постменопаузального возраста. Препараты чМГ содержат ЛГ и ФСГ, по 75 МЕ (пергонал, меногон, менопур и др.). При назначении гонадотропинов пациентка должна быть информирована о риске многоплодной беременности, возможном развитии синдрома гиперстимуляции яичников, а также о высокой стоимости лечения. Лечение должно проводится только после исключения патологии матки и труб, а также мужского фактора бесплодия. В процессе лечения обязательным является трансвагинальный УЗ-мониторинг фолликулогенеза и состояния эндометрия. Овуляция инициируется путем однократного введения чХГ в дозе 7500-10000 МЕ, когда имеется хотя бы один фолликул диаметром 17 мм. При выявлении более 2 фолликулов диаметром более 16 мм. или 4 фолликулов диаметром более 14 мм. введение чХГ нежелательно из-за риска наступления многоплодной беременности.
При стимуляции овуляции гонадотропинами частота наступления беременности повышается до 60%, риск многоплодной беременности составляет 10-25%, внематочной — 2,5-6%, самопроизвольные выкидыши в циклах, закончившихся беременностью, достигают 12-30%, синдром гиперстимуляции яичников наблюдается в 5-6% случаев.
Хирургическое лечение СПКЯ
Несмотря на достаточно высокий эффект при стимуляции овуляции и наступлении беременности, большинство врачей отмечают рецидив клинической симптоматики СПКЯ примерно через 5 лет. Поэтому послебеременности и родов необходима профилактика рецидива СПКЯ, что важно, учитывая риск развития гиперпластических процессов эндометрия. С этой целью наиболее целесообразно назначение КОК, предпочтительнее монофазных (марвелон, фемоден, диане, мерсилон и др.). При плохой переносимости КОК, что бывает при избыточной массе тела, можно рекомендовать гестагены во вторую фазу цикла: дюфастон в дозе 20 мг. с 16-го по 25-й день цикла.
Женщинам, не планирующим беременность, после первого этапа стимуляции овуляции кломифеном, направленного на выявление резервных возможностей репродуктивной системы, также рекомендуется назначение КОК или гестагенов для регуляции цикла, уменьшения гирсутизма и профилактики гиперпластических процессов.
Физиотерапия и фитнесс для лечения СПКЯ
Физиотерапевтические процедуры также показаны при СПКЯ. Применяют гальванофорез лидазы для активации ферментативной системы яичников. Электроды устанавливают в надлобковой области. Курс лечения-15 дней ежедневно.
Лечение поликистоза яичников длительное, требующее тщательного наблюдения у гинеколога-эндокринолога. Всем женщинам с СПКЯ рекомендуется, по возможности, как можно раньше беременеть и рожать, поскольку симптомы заболевания, увы, с возрастом довольно часто прогрессируют.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.