фистула затромбировалась что делать
Диагностика и лечение артериовенозной фистулы
Автор материала
Профессор Капранов С.А. — Доктор медицинских наук, дважды Лауреат Государственных Премий Правительства Российской Федерации в области науки и техники, Лауреат Премии Ленинского Комсомола, автор более 350 научных работ по медицине, 7 монографий, и 10 патентов на изобретения по медицине, за 30 лет личного опыта провел более чем 10 000 различных эндоваскулярных операций
Как уже отмечалось, врожденные фистулы в основном имеют свойства проявляться ярко выраженными косметическими изъянами (багровые кожные покровы и непрезентабельный внешний вид).
При этом, если артериовенозную фистулу значительного размера своевременно не излечить, возникает варикозное расширение вен и тромбоз. В некоторых случаях развивается сердечная недостаточность. Как правило, диагноз определяется в ходе осмотра врачом и проведения ряда дополнительных методов обследования. Обязательно осуществляется проведение ультразвукового дуплексного сканирования. В случае, когда артериовенозная фистула сформировалась между сосудами, расположенными глубоко, определить ее возможно только при осуществлении ангиографии или МР-ангиографии.
Удаление небольших врожденных артериовенозных фистул осуществляется с помощью методики лазерной коагуляции. Данное сосудистое вмешательство проводят только эндоваскулярные хирурги, обладающие высокой квалификацией. Крайне сложные операции по удалению артериовенозных фистул, расположенных в области глаз, головного мозга или других жизненно важных органов. Как правило, все эти вмешательства заранее планируются.
Диагностика приобретенных артериовенозных фистул должна быть проведена немедленно. Лечение этой патологии обычно проводится в экстренном порядке. Перед началом оперативного вмешательства обязательно осуществление ангиографического исследования, при котором просматривается степень поражения сосудов. Исходя из полученных исследований и определяется тактика лечения.
При этом артериовенозная фистула может быть устранена эндоваскулярным путем. На данном этапе одним из самых популярных методов сосудистого лечения фистул является эмболизация (закупорка) кровеносных сосудов.
В данном случае при проведении этой малоинвазивной процедуры в пораженный сосуд под контролем новейшего рентгеноборудования вводят специальное вещество, закупоривающее патологическое артериовенозное сообщение.
В особо сложных случаях специалисты считают целесообразным осуществление хирургической операции. В некоторых случаях проводят открытые микрохирургические вмешательства, при которых закрывают артериовенозную фистулу после осуществления небольшого разреза. Если у пациента поражен мозг, необходима трепанация черепа. В ряде случаев, когда травмированы легкие, параллельно с закрытием фистулы, проводят удаление прилегающей легочной ткани.
Тромбоз артерио-венозной фистулы: тромбэктомия или реконструкция?
Авторы
Калинин Р.Е., Сучков И.А., Егоров А.А., Климентова Э.А.
ФГБОУ ВО Рязанский государственный медицинский университет имени академика И.П. Павлова, Рязань
Аннотация
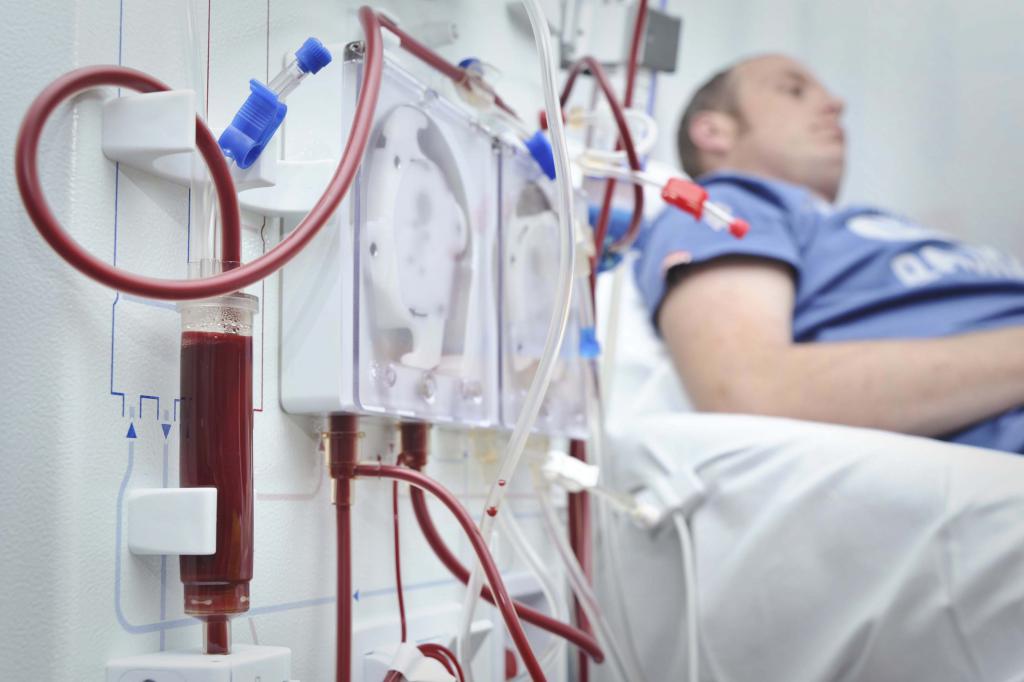
Программный гемодиализ, на сегодняшний день, является основным методом в лечении пациентов с терминальной хронической болезнью почек. Для проведения адекватного гемодиализа необходимо формирование постоянного сосудистого доступа (как правило, это артерио-венозная фистула). Одной из основных причин прекращения его функционирования является тромбоз.
Цель исследования: выявление причин тромбоза артерио-венозных фистул и выбор оптимального способа диагностики и хирургической коррекции.
Материалы и методы. В данное исследование включено 70 пациентов, с тромбозом нативных артерио-венозных фистул. Всем пациентам в качестве диагностики выполнялось ультразвуковое дуплексное сканирование, ангиография по показаниям. Проводилось гистологическое исследование стенозов фистульных вен и анастомозов. Все пациенты подвергались хирургическому лечению в объеме тромбэктомии, реконструкции артерио-венозные фистулы, либо формирования нового доступа.
Результаты. Все пациенты были разделены на три группы в зависимости от вероятной причины тромбоза и вида операции: тромбоз на неизмененных сосудах — 5 пациентов (7%); тромбоз, вследствие гиперплазии неоинтимы, в местах пункций фистульной вены — 25 пациентов (43%); тромбоз, вследствие гиперплазии неоинтимы артериовенозного анастомоза — 35 пациентов (50%).
Данные причины были выявлены с помощью ультразвукового дуплексного сканирования и периферической ангиографии. Всем больным проводилось оперативное лечение, направленное на восстановление постоянного сосудистого доступа. Участки тромбированных вен и анастомозов подвергались гистологическому исследованию, где наблюдалась гиперплазия неоинтимы, которая гемодинамически значимо суживала просвет сосуда и служила причиной тромбоза.
Заключение. В ходе проведенного исследования клинически и гистологически было подтверждено, что основной причиной тромбоза нативной артерио-венозной фистулы является гиперплазия неоинтимы анастомоза, либо фистульной вены, которая требует обязательного хирургического вмешательства.
Ключевые слова: постоянный сосудистый доступ, артерио-венозная фистула, гемодиализ, неоинтима, тромбоз.
Список литературы
1. Калинин Р.Е., Сучков И.А., Егоров А.А. Возможности рентгенэндоваскулярной и гибридной коррекции постоянного сосудистого доступа у диализных пациентов // Наука молодых (Eruditio Juvenium). — 2018. — Т.6. — №4 — С. 561–568. [Kalinin RE, Suchkov IA, Egorov AA. Possibilities of roentgen-endovascular and hybrid correction of permanent vascular access in dialysis-dependent patients. Science of the young (Eruditio Juvenium). 2018;6(4):561–568. (In Russ).] Doi: 10.23888/HMJ201864561-568.
2. Gottmann U, Sadick M, Kleinhuber K. Central vein stenosis in a dialysis patient: a case report. J Med Case Rep. 2012;6:189. Doi: 10.1186/1752-1947-6-189.
3. Leivaditis K, Panagoutsos S, Roumeliotis A, et al. Vascular access for hemodialysis: postoperative evaluation and function monitoring. Int Urol Nephrol. 2014;46(2):403–409. Doi: 10.1007/s11255-013-0564-2.
4. Oleśkowska-Florek W, Połubinska A, Baum E, et al. Hemodialysis-induced changes in the blood composition affect function of the endothelium. Hemodial Int. 2014;18(3):650–656. Doi: 10.1111/hdi.12148.
5. Arnold WP. Improvement in hemodialysis vascular access outcomes in a dedicated access center. Semin Dial. 2000;13(6):359–363. Doi: 10.1046/j.1525-139x.2000.00106.x.
6. Higuchi T, Okuda N, Aoki K. Intravascular ultrasound imaging before and after angioplasty for stenosis of arteriovenous fistula in hemodialysis is patients. Nephrol Dial Transplant. 2001;16(1):151–155. Doi: 10.1093/ndt/16.1.151.
7. Paun M, Beach K, Ahmad S, et al. New ultrasound approaches to dialysis access monitoring. Am J Kidney Dis. 2000;35(3):477–481. Doi: 10.1016/s0272-6386(00)70201-0.
8. Rodriguez JA, Armadans L, Ferer E, et al. The function of permanent vascular access. Nephrol Dial Transplant. 2000;15(3):402–408. Doi: 10.1093/ndt/15.3.402.
9. Roy-Chaudhury P, Kelly BS, Miller MA, et al. Venous neointimal hyperplasia in polytetrafluoroethylene dialysis grafts. Kidney Int. 2001;59(6):2325–2334. Doi: 10.1046/j.1523-1755.2001.00750.x.
10. Heikkinen M, Salenius JP, Auvmen O. Projected workload for a vascular service in 2020. Fur J Vase Endovasc Surg. 2000;19(4):351–355. Doi: 10.1053/ejvs.2000.1074.
11. Stehman-Breen CO, Sherrard DJ, Gillen D, Caps M. Determinants of type and timing of initial permanent hemodialysis vascular access. Kidney Int. 2000;57(2):639–645. Doi: 10.1046/j.1523-1755.2000.00885.x.
Фистула затромбировалась что делать
Если почка – второе сердце человека (так много функций выполняет этот орган), то для пациента на гемодиализе эту роль в какой-то степени выполняет фистула. Незнакомое для большинства людей слово означает «сосудистый доступ» — место, откуда берется значительное количество крови для очистки в аппарате «искусственная почка» и куда оно возвращается уже в очищенном от токсинов виде. Обычно это рука, предплечье, хотя при крайней необходимости могут быть и другие органы человека.
Так вот, нормальная работа организма подразумевает течение кровотока от сердца по артериям в капилляры, затем движение происходит по венам обратно. Артериовенозная фистула представляет собой искусственно созданное соустье артерии и вены, они «сшиваются» — в итоге кровь движется по сообщению между веной и артерией, минуя капиллярную сеть. Естественно, поток крови увеличивается, вена набухает – что дает возможность быстро перекачивать кровь посредством специальных игл.
— Можно ли обойтись без операции?
Операция по формированию фистулы считается несложной, если сосуды достаточно развиты и нет сопутствующих заболеваний, то она продлится минут 40. При этом пациент остается в полном сознании, операция проводится под местной анестезией.
Если же естественное формирование фистулы по каким-то причинам невозможно, то используются специальные сосудистые протезы – трубочки, заменяющие часть вены. Их можно пунктировать уже через сутки после операции. Фистулу, сформированную «естественным» путем, нужно беречь. Колоть в нее не рекомендуется по крайней мере месяц. Фистула должна «созреть», набухнуть кровью. Иначе искусственно созданное соустье артерии и вены может нарушиться, фистула «остановится».
— Готовьтесь к диализу заблаговременно
Учитывая значение фистулы для всей дальнейшей жизни диализного пациента, специалисты рекомендуют формировать фистулу заблаговременно, планово, за несколько месяцев до начала диализа. Это гарантирует многолетнюю работу фистулы и отсутствие дополнительных проблем на гемодиализе.
Правда, большая часть больных попадают на диализ слишком поздно — тогда, когда организм уже отравлен токсинами из-за плохо работающих почек и когда счет идет уже на недели, а то и дни. Поэтому им приходится срочно обеспечивать временный сосудистый доступ – через катетеры в центральных венах – подключичной или яремных, располагающихся на шее и уносящих кровь от шеи и головы.
— Почему она так шумит?
Новичка с только что сформированной фистулой узнать довольно легко – как правило, пациент то и дело ее «выслушивает». Для этого достаточно прижать прооперированную руку к уху. Этот пульсирующий, чуть свистящий звук трудно спутать с чем-то другим. Некоторым людям он напоминает шум работающих прессов или машин. Это перекачивается кровь по набухшим венам. Шум должен быть ритмичным и всегда одним и тем же. При любом изменении звука необходимо срочно показать лечащему врачу. А если вдруг шум пропал, срочно отправляйтесь в диализный центр – фистула могла остановиться, затромбироваться. Иногда тромбы удается убрать хирургическим путем или медикаментозно.
— Из истории создания фистулы
Не зря говорят, что все гениальное просто. Несмотря на кажущуюся простоту, идея создания артериовенозной фистулы не сразу пробилась среди других научных изобретений. В первые годы применения диализа ученым пришлось изрядно намучаться с этой проблемой. Поначалу в качестве сосудистого доступа использовали канюлю — трубку, которую хирургическим путем закрепляли, «приживляли» к сосудам пациента.
Началом эпохи хронического гемодиализа считается 1960 год, когда Белдингу Скрибнеру и Вейну Квинтону из американского города Чикаго удалось решить проблему долгосрочного сосудистого доступа. У них долговременный сосудистый доступ обеспечивался путем имплантации в лучевую артерию и подкожную вену двух тонкостенных тефлоновых трубок. Наружные концы шунта соединялись изогнутой тефлоновой трубкой, которая на время проведения гемодиализа удалялась, а к шунтам подключался гемодиализатор.
Фистула затромбировалась что делать
В целом в Москве около 3600 человек получает лечение программным гемодиализом. Наилучшей стратегией с точки зрения комфорта пациента и минимизации осложнений является осуществление гемодиализа через сформированную артерио-венозную фистулу (АВФ) в качестве постоянного сосудистого доступа.
Осложнение при длительно существующих АВФ
Срок функционирования артерио-венозных фистул ограничен многими факторами. В частности, венозная часть фистулы подвергается дегенерации и стенозированию, что существенно сокращает срок службы сосудистого доступа и затрудняет проведение гемодиализа. Довольно часто встречается сужение или окклюзия центральных вен вследствие длительно стоящих центральных венозных катетеров или многократных пункций центральных вен у этой категории пациентов. К сожалению количество возможных анастомозов ограниченно доступными сосудами. Таким образом, дисфункция артериальной или венозной части приводит к необходимости формировать новую фистулу, что не всегда возможно в условиях длительной заместительной почечной терапии. В тоже время окклюзия центральной вены приводит к потере возможности формирования сосудистого доступа на этой конечности.
Современные эндоваскулярные технологии позволяют осуществлять малотравматичную эффективную реконструкцию сосудистого доступа и центральных вен, что ведет к сохранению существующей фистулы и удлинению срока функционирования сосудистого доступа.
В нашу клинику поступила пациентка, находящаяся на заместительной почечной терапии в течении 2-х лет. В последние полгода отмечает массивный отек правой руки, на которой сформирована артерио-венозная фистула для проведения гемодиализа. К моменту госпитализации отек увеличился настолько, что существующий сосудистый доступ стал недоступен для пункции и проведения гемодиализа. Пациентка жаловалась на потерю подвижности правой руки вплоть до пальцев, боль и эстетический дискомфорт.
Раньше одним из методов борьбы с подобной проблемой было лигирование, то есть перевязка сформированного артерио-венозного анастомоза с потерей возможности формирования новой фистулы на этой конечности. Такой подход неоправдан в условиях ограниченного количества мест, подходящих для формирования сосудистого доступа, а потеря всей конечности становится катастрофой для пациентов, зависящих от гемодиализа.
Врачи-эндоваскулярные хирурги выполнили прямую фистулографию, на которой выявлена окклюзия правой подключичной вены, что и явилось причиной массивного отека. В течении 6,5 часов мы предпринимали попытки реканализации этой окклюзии, однако несмотря на применение различных методик пройти через окклюзию в истинный просвет верхней полой вены не удалось. Несколько раз проводник уходил в субинтимальное пространство, однако нащупать истинный ход правой подключичной вены не удалось ни антеградно ни ретроградным доступом. Спустя 6,5 часов от дальнейших попыток было решено отказаться. Однако, принимая во внимание субинтимальный канал, сформированный во время попыток реканализации вены, было принято решение взять пациентку на повторную реканализацию спустя две недели.
На повторной фистулографии мы убедились в том, что протяженность окклюзии сократилась, и предприняли попытку повторной реканализации правой подключичной вены. Коронарный проводник при поддержке микрокатетера удалось провести через зону окклюзии в верхнюю полую вену. Затем коронарным баллоном диаметром 2,5 мм и длиной 15 мм выполнена дилатация в зоне окклюзии и сформирован канал, по которому был проведен диагностический катетер и осуществлена смена проводника. Процедура закончилась успешной имплантацией саморасширяющегося стента в область окклюзии правой подключичной вены, и восстановлением магистрального кровотока. На следующие сутки пациентка отметила существенное уменьшение отека правой руки, возвращение подвижности в пальцах и локтевом суставе. А через несколько дней отек полностью исчез и рука приобрела нормальный размер. Таким образом эндоваскулярная реконструкция позволила сохранить сосудистый доступ на правой руке, сохранить правую руку для формирования повторных артерио-венозных анастомозов в случае необходимости. И что важно — позволила сохранить высокое качество жизни пациентке на заместительной почечной терапии.
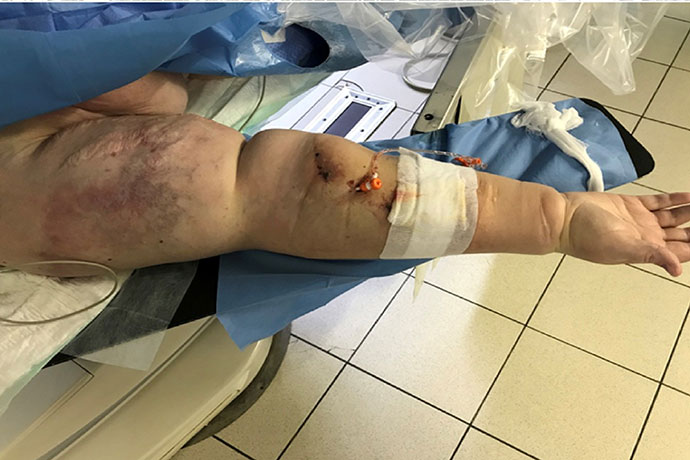
Правая рука до реконструкции сосудистого доступа
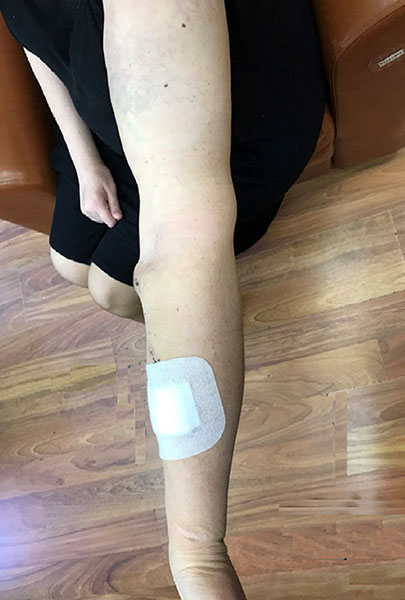
Правая рука на 3-й день после реконструкции
Лечение стенозов и тромбозов фистулы и протезов
При стенозе в области анастомоза на предплечье показана хирургическая коррекция. Чрескожная ангиопластика также осуществима, но дает менее долгосрочные результаты. Дилятация анастомоза на плече более 6 мм часто приводит к синдрому обкрадывания и ишемии конечности. Чрескожная ангиопластика – метод выбора вмешательства на венах плеча (v.cephalica или v.basilica). Чрескожной ангиопластике подвергаются стенозы области соединения поверхностных и глубоких вен. При установке стента в конечный отрезок v.cephalica он не должен выступать в подключичную вену, поскольку может спровоцировать формирование стеноза, что исключит возможность использования более дистальных вен.
Для визуализации зоны стеноза выполняется ангиография ретроградным пунктированием плечевой артерии в случае проблем с анастомозом или антеградным пунктированием непосредственно вены выше анастомоза, если предполагаются проблемы с венозным оттоком. В настоящее время нельзя отдать предпочтение рентген-хирургическим методам или открытой хирургии при протяженных стенозах, но при коротких стенозах (менее 2 см) исходы чрескожной ангиопластики лучше, чем для протяженных стенозах (более 2 см). Некоторые стенотические ткани не удается расширить обычным баллоном, в таких случаях используют режущие баллоны и баллоны ультравысокого давления (до 32 атм).
Повторные стенозы также могут лечиться как рентгенохирургическими, так и открыто-хирургическими методами. Выбор зависит часто от состояния пациента с учетом степени инвазивности вмешательства. Иногда, несмотря на полное расправление баллона, после его удаления наступает повторное спадение вены, в таких случаях требуется установка стента, особенно в центральных венах.
Тромбоз фистулы требует немедленного вмешательства, предпочтительно в течение 48 часов. Длительность, место тромбоза и тип сосудистого доступа являются определяющими предикторами исходов лечения. Тромбоз может начаться с постанастомотического сегмента вены или от места пункций иглами. Когда тромб локализуется в анастомозе, отводящая вен может остаться проходимой за счет тока по коллатералям; в этих условиях можно наложить более проксимальный анастомоз. Тромбоз перемещенной v.basilica обычно приводит к распространению тромбоза на всю вену. Тромболизис можно произвести механически или фармакомеханически. Годичная вторичная выживаемость (после восстановления проходимости) достигает 80% для фистул на предплечье и 50% на плече. Комбинация тромболитических агентов (урокиназа или тканевой активатор плазминогена) с баллонной ангиопластикой дает немедленный результат в 90% случаев и проходимость сосуда через год в 70%. Хирургическую тромбэктомия проводят с помощью катетера Фогерти. Полезным может стать ручное ретроградное выдавливание тромба. После восстановления проходимости вены оправдано интраоперационная ангиография реканализированной вены и центральных вен для того, чтобы найти/исключить дополнительные стенозы и остаточные тромбы. Идентификация и коррекция причин тромбоза является существенной частью любого вмешательства по восстановлению проходимости сосудистого доступа.
Уменьшение диаметра просвета протеза вместе с существенным снижением кровотока рассматривается как показание к вмешательству. Как и в случае фистулы, большинство артериальных стенозов удается исправить чрескожной ангиопластикой, если стеноз ограничивается только афферентной артерией и участком протеза. Если стеноз захватывает и эфферентный участок артерии, велика вероятность развития ишемии конечности. В этом случае Чрескожная ангиопластика может оказаться недостаточно эффективной и потребуется хирургическое вмешательство.
Стеноз срединного участка протеза обычно фиксируют в зоне пункций. Он обусловлен избыточным ростом фиброзных тканей через пункционные отверстия. Возможна чрескожная ангиопластика, механическое очищение просвета или замена участка протеза.
Наиболее частой причиной дисфункции протеза является стеноз венозного анастомоза. Поскольку протезы следует устанавливать только у пациентов с исчерпанными возможностями периферических вен, восстановление проходимости протеза следует проводить по максимально вено-сберегаюшим методикам – чрескожной ангиопластикой или закрытием дефектов заплатами, хотя продление протеза в центральную вену дает большую частоту восстановления проходимости. При повторных неудачах чрескожной ангиопластики следует рассмотреть возможность стентирования. Только следующим этапом должно стать продление протеза до более проксимального участка венозной системы. В 20-30% случаев чрескожная ангиопластика не приводит к увеличению потока крови более 600 мл/мин, что указывает на недостаточную дилятацию баллоном малого размера или на невыявленный и нескорректированный стеноз, расположенный более проксимально или в области артериального анастомоза.
Лечение в случае тромбоза протеза следует начинать возможно быстрее и в пределах 48 часов. Раннее удаление тромба позволяет немедленно продолжить лечение без использования центральных катетеров и связанных с ними рисков. Как правило, тромб представляет собой компактную «артериальную пробку». Старые тромбы (более 5 дней) часто фиксированы к стенке сосуда, что делает хирургическую экстракцию более трудной. Хирургическая тромбэктомия выполняется с помощью тромбэктомического катетера. Целесообразно проводить интраоперационную ангиографию с заполнением артериальной и венозной ветви протеза для исключения остаточных тромбов и выявления причины тромбоза. Поиск причин должен стать неотъемлемой частью любой хирургической или ангиологической процедуры. Альтернативой открыто-хирургическому методу могут стать различные чрескожные методики, включающие в себя тромбоаспирацию, использование тромболитических агентов, механическую тромбэктомию и механические тромбэктомические устройства. Восстановление проходимости достигают в 75% случаев, а первичная проходимость сохраняется через 1 и 3 месяца в 30% и 25% случаев. Поэтому так существенно выявлять причины тромбообразования, которыми часто становятся стенозы. Исключительно важно после вмешательства провести ангиографию для выявления (и коррекции) стенозов зон притока, срединных участков и оттока из протеза.