ферритин что это такое у детей норма
Что сдавать при подозрении на анемию: гемоглобин или ферритин?
Наиболее распространенные симптомы анемии встречаются у многих людей, однако большинство «списывает» их на хроническую усталость, планируя выспаться в отпуске или на праздниках. Игнорируя первые признаки анемии, можно сильно навредить своему организму. В этой статье мы расскажем, какие анализы помогут в её диагностике и в чём их отличия.
Что такое анемия?
Если врач ставит диагноз анемия, то это также означает наличие в организме скрыто протекающих патологических процессов, поскольку анемия не является самостоятельным заболеванием, а лишь указывает на другие проблемы. Условно говоря, анемию можно назвать «симптомом» инфекционного, воспалительного, онкологического или другого заболевания.
Причины и классификация анемии
Врачи классифицируют много видов анемии, которые для простоты понимая можно разделить на три группы.
К первой относятся состояния кровопотери, когда человек в результате несчастного случая потерял очень много крови или в организме происходит желудочно-кишечное или другое хроническое кровотечение. Ко второй категории анемии относятся состояния, при которых нарушается производство нормальных эритроцитов и синтез гемоглобина. К третьей – когда происходит ускоренное разрушение эритроцитов по каким-либо причинам.
Наиболее распространенной в мире считается железодефицитная анемия, которая составляет около 70-90% от всех случаев. К другим причинам развития анемии можно отнести дефицит витамина В12 и А, фолиевой кислоты, острые и хронические воспаления, а также другие патологические процессы в организме, которые влияют на синтез гемоглобина.
Симптомы, которые могут указывать на анемию
Для большинства видов анемии на первых этапах развития болезни в основном характерны следующие внешние симптомы:
Лабораторная диагностика анемии
Различные показатели в анализе могут указывать на дефицит железа в организме, однако установить диагноз анемия можно только по комплексу лабораторных исследований. Обычно при подозрении на анемию пациенту назначается общий и биохимический анализы крови, где главными показателями являются:
Железо сыворотки – этот показатель отражает количество железа в кровотоке, резервный уровень запасов железа в тканях;
Ферритин – биомаркер железодефицитных состояний. В белке ферритине скапливаются запасы железа, которые не были использованы эритроцитами. Уровень этого резерва очень важно знать, поскольку истощение запасов постепенно приводит к развитию анемии. Хорошая новость заключается в том, что снижение ферритина происходит постепенно и ранняя диагностика человеку не допустить прогрессирования анемии;
Трансферрин – укажет на метаболизм железа, причину и вид развивающейся анемии;
Витамин В12 – поможет выяснить, всасывается ли поступающее из пищи железо. Длительный дефицит В12 опасен, поскольку витамин необходим для формирования клеток крови и правильной работы нервной системы;
Общая железосвязывающая способность сыворотки (ОЖСС) – определяет количество железа в организме и его взаимосвязи с другими белками. ОЖСС считается стабильным показателем, которые указывает на циркуляцию железа независимо от питания в течение дня (в течение суток уровень железа меняется, поэтому важно правильно интерпретировать общую «картину» в организме);
Показатели уровня гемоглобина и эритроцитов – среднее количество гемоглобина в эритроцитах. Изменения в этих показателях являются первыми «звоночками» для пациента и врача о патологических изменениях в организме.
В зависимости от общего состояния и жалоб пациента врач может назначить выполнение отдельных показателей крови или всего комплекса анализов.
Профилактика и лечение анемии
Ранние стадии железодефицита можно скорректировать специальной диетой и приемом витаминов, однако важно вовремя обнаружить проблему, правильно подобрать дозировку витаминов и изменить рацион в сторону продуктов, богатых железом – мяса, рыбы и морепродуктов, яиц (желтков), бобовых, злаковых, орехов, семечек, свежих фруктов и овощей, а также сухофруктов.
Нередко для улучшения всасываемости железа из пищи врач назначает прием комплекса витаминов, который ускорит лечебный процесс. Рацион считается основным источником железа, однако организм не всегда может усвоить необходимое ему количество железа.
Тяжелые формы анемии лечатся комплексно и помимо витаминов и изменения рациона включает лекарственную терапию.
В лаборатории LabQuest можно провести полное обследование организма, если вы заподозрили у себя признаки анемии. По результатам выполняется бесплатная интерпретация выполненных анализов врачом-экспертом лабораторной диагностики.
Железодефицитная анемия у детей
Почему при ЖДА необходимы препараты железа? В чем преимущества препаратов последнего поколения? Почему прием препаратов железа должен быть длительным? Картина крови при хронической железодефицитной анемии. Выраженные гипохромия эритроци
Почему при ЖДА необходимы препараты железа?
В чем преимущества препаратов последнего поколения?
Почему прием препаратов железа должен быть длительным?
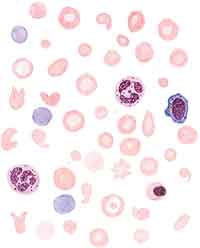 |
| Картина крови при хронической железодефицитной анемии. Выраженные гипохромия эритроцитов, анизоцитоз, пойкилозитоз, шизоцилы, присутствие полихроматофилов |
Анемия — это патологическое состояние, характеризующееся снижением массы эритроцитов, часто в сочетании с уменьшением количества эритроцитов в единице объема крови. Причин возникновения анемий очень много; для детского же возраста наиболее типична железодефицитная анемия (ЖДА). ЖДА характеризуется наличием небольших гипохромных эритроцитов и истощением запасов железа в организме.
Распространенность дефицита железа у детей в раннем возрасте, по данным ВОЗ, составляет от 17,5 до 30%.
Можно выделить следующие причины развития дефицита железа у детей.
Важно отметить, что у детей раннего возраста причинами дефицита железа, как правило, являются недостаточное депо железа и нерациональное питание, а у детей старшего возраста — кровопотеря и резкое вытяжение.
Патофизиологические аспекты
Поскольку всасывание железа ограничено, у большинства людей его поступление с пищей едва покрывает текущую потребность организма, в результате заболеваний или неправильного питания довольно легко развивается дефицит железа. Этот процесс состоит из нескольких стадий.
Стадия 1. Потеря железа превышает его поступление. На фоне отрицательного баланса железа его запасы в костном мозге постепенно истощаются. Хотя уровень железа в сыворотке и количество гемоглобина остаются нормальными, содержание ферритина в сыворотке уменьшается (ниже 20 нг/мл). По мере истощения запасов железа происходит компенсаторное повышение концентрации трансферрина (о чем свидетельствует увеличение железосвязывающей способности).
Стадия 2. Истощенные запасы железа уже не обеспечивают эритропоэтическую функцию костного мозга. В то время как уровень трансферрина в плазме растет, содержание железа в сыворотке снижается, что приводит к его всевозрастающей нехватке при образовании эритроцитов. Эритропоэз нарушается, когда уровень железа ниже 50 мкг%, а насыщение трансферрина — ниже 16%. Возрастает концентрация рецепторов ферритина в сыворотке (более 8,5 мг/л).
Стадия 3. Анемия при внешне нормальных эритроцитах и эритроцитарных индексах.
Стадия 4. Развитие микроцитоза и затем гипохромии.
Стадия 5. Дефицит железа сопровождается симптомами тканевых нарушений.
Клинические проявления
Представление о клиническом статусе больного с анемией зависит от основного заболевания и формы анемии (острой или хронической). ЖДА — состояние хроническое. Проявление анемии per se объясняют с помощью патофизиологических механизмов. Большинство симптомов ЖДА являются отражением сердечно-сосудистых и газообменных изменений, компенсирующих уменьшение массы эритроцитов. Степень выраженности симптомов зависит от скорости развития анемии (при медленном развитии анемии, характерном для железодефицитных состояний, времени для полного развития компенсаторных механизмов достаточно) и ее длительности. Даже анемия средней тяжести нередко протекает бессимптомно. Ребенок может жаловаться на усталость, одышку и сердцебиение, особенно после физической нагрузки. При тяжелой анемии симптоматика сохраняется и в состоянии покоя, больной не может переносить физические нагрузки. Если уровень гемоглобина менее 75 г/л, то минутный сердечный выброс в покое заметно повышается по мере увеличения как частоты сердечных сокращений, так и ударного объема. Симптомы сердечной недостаточности развиваются, когда резерв миокарда исчерпан. Следовательно, тяжесть состояния больного определяется прежде всего степенью выраженности сердечно-сосудистых нарушений.
Симптоматика при анемии средней и тяжелой степени распространяется и на другие системы органов. Больной часто жалуется на головокружение и головные боли, шум в ушах, возможен даже обморок. Человек становится раздражительным, нарушается сон, снижается концентрация внимания. Поскольку кровоток в коже снижен, может развиваться гиперчувствительность к холоду. Возникает симптоматика и со стороны желудочно-кишечного тракта — резкое снижение аппетита, диспепсические расстройства (тошнота, изменение характера и частоты стула), прежде всего это происходит за счет шунтирования крови, минующей сосудистое русло внутренних органов. У девочек-подростков нарушается менструальный цикл, что проявляется в виде аменореи или обильного кровотечения.
Основной признак анемии — бледность кожных покровов. Однако его информативность ограничена другими факторами, определяющими цвет кожи.
Поэтому наиболее информативным признаком анемии является бледность видимых слизистых — слизистой оболочки полости рта, ногтевого ложа и конъюнктивы век. Информативным также считается цвет кожи на сгибах ладонной поверхности — если по цвету они не отличаются от окружающей кожи, то уровень гемоглобина у больного, как правило, менее 80 г/л.
Развитие бледности кожных покровов при анемии объясняется двумя факторами: первый — это, несомненно, уменьшение уровня гемоглобина в крови, второй — шунтирование крови в обход сосудов кожи и других периферических тканей, способствующее усиленному кровоснабжению жизненно важных органов. Перераспределение кровотока представляет собой один из важных механизмов компенсации анемии.
Из других клинических симптомов анемии следует отметить уже упоминавшиеся выше тахикардию, значительные колебания пульсового давления, систолический шум изгнания над предсердиями, снижение умственной и физической активности, дети становятся раздражительными, быстро утомляются, их сон беспокойный, аппетит снижен.
При ЖДА к обычным симптомам анемии присоединяются признаки, специфичные для недостаточности железа. При длительном дефиците железа появляются извращенные аппетит (поедание мела, грязи, красок) и обоняние (нравятся резкие запахи бензина, красок, лаков, поедание льда (пагофагия), развиваются глосситы, хейлит, койлонихия (истонченные, исчерченные, ломкие ногти). При дефиците железа падает активность иммунной системы за счет снижения синтеза ИЛ-2, Т-киллеров; дети чаще болеют ОРВИ, что, в свою очередь, усугубляет имеющийся дефицит железа.
Диагноз подтверждается лабораторными данными. Критерием диагностики ЖДА является анемия микроцитарная, гипохромная, норморегенераторная. Для ЖДА характерны анизоцитоз, тромбоцитоз, снижение уровня сывороточного железа (менее 13 ммоль/л), общая железосвязывающая способность сыворотки не изменена или повышена, уровень сывороточного ферритина менее 15 нг/мл, насыщение трансферрина меньше 16%, уровень протопорфирина эритроцитов повышен, уровень Hb A2 снижен, в костном мозге отмечается раздражение красного ростка (эритроциты : гранулоциты = 1:1 — 1:2), типично отсутствие в костном мозге запасов железа и кольцевидных сидеробластов.
В дифференциально-диагностический поиск включаются талассемия, отравление свинцом, анемия при хронических заболеваниях, врожденные нарушения обмена железа (дефицит трансферрина, нарушение утилизации железа, нарушение реутилизации железа), гемосидероз, в том числе синдром Гудпасчера, дефицит меди.
Принципы лечения ЖДА у детей
Диетотерапия при ЖДА у детей
В настоящее время общепризнано, что устранить дефицит железа в организме только с помощью диетотерапии невозможно. Это связано с тем, что всасывание железа из пищевых продуктов ограничено — 1,8-2 мг (не более 2,5 мг) железа в сутки — даже при рациональном питании, соответствующем возрасту, и при потреблении достаточного количества продуктов с высоким содержанием железа. (Для сравнения: здоровый ребенок в зависимости от возраста теряет за сутки от 0,15 до 0,6 мг железа, девочка во время месячных — 15-50 мг) При приеме современных препаратов железа оно усваивается в 20 раз лучше. Диетотерапия должна быть одной из составляющих терапии ЖДА у детей.
С другой стороны, очень важно ориентироваться не на содержание железа в продуктах питания, а на его форму. Именно форма железа определяет процент его всасывания и усвоения и, следовательно, эффективность терапии. Из различных форм железа легче всего усваивается гемовое железо — сложное органическое соединение, в котором железо находится в составе гемоглобина; неорганические соединения — соли железа — усваиваются организмом значительно хуже. Железо в составе гема активно захватывается клетками слизистой кишечника и всасывается в неизмененном виде. Процессы всасывания гема в кишечнике не зависят от кислотности среды и активности пищевых ферментов. Железо из злаков, овощей, фруктов всасывается значительно хуже из-за присутствия в них ингибиторов ферроабсорбции, таких, как оксалаты, фосфаты, танин и другие. Сравните: коэффициент усвояемости железа из говядины (гемовое железо) составляет 17-22%, из фруктов — не более 3%. Степень усвояемости железа из продуктов животного происхождения также зависит от формы железосодержащих соединений. Так, из печени, где соединения железа представлены в виде ферритина и трансферрина, железо усваивается в значительно меньшем количестве, чем из мясных продуктов, хотя общее содержание железа в печени в 3 раза больше, чем в мясе. Поэтому включение печени в рацион питания для устранения дефицита железа или с профилактической целью не имеет никакого смысла. Таким образом, рацион питания должен быть максимально богат продуктами, в которых железо содержится в виде гема (язык говяжий, мясо кролика, говядина).
Необходимо отметить также, что мясо, печень и рыба улучшают всасывание железа из фруктов и овощей при одновременном их употреблении.
Всасываемость железа из злаковых, бобовых, клубневых, овощей, фруктов значительно ниже, поскольку железо в них содержится в негемовой форме, и во многом зависит от содержания в рационе веществ, ингибирующих или потенцирующих всасывание железа. Усиливают всасывание негемового железа аскорбиновая кислота, продукты из мяса, птицы, рыбы, а также вещества, понижающие кислотность пищи (например, молочная кислота). Снижают усвоение негемового железа соевый протеин, полифенолы, входящие в состав чая, кофе, орехов и бобовых. Несмотря на высокое содержание железа в некоторых продуктах растительного происхождения, они не могут обеспечить высокую потребность в железе, характерную для растущего организма, поскольку железо из них всасывается значительно хуже, чем из продуктов животного происхождения. Рекомендации употреблять в больших количествах фруктовые соки, яблоки, гранаты, гречневую крупу и другие продукты в целях восполнения депо железа при ЖДА также нельзя считать обоснованными. Сбалансированная по основным ингредиентам диета позволяет «покрыть» только физиологическую потребность организма ребенка в железе, но никак не устраняет дефицита железа и должна использоваться в комплексе с препаратами железа при лечении ЖДА. Однако полноценная и сбалансированная диета занимает важное место в профилактике развития дефицита железа в организме ребенка во все периоды детства.
Медикаментозная терапия при ЖДА
Основной задачей терапии ЖДА является устранение дефицита железа в организме ребенка. Это достигается благодаря приему железосодержащих лекарственных препаратов. Основные требования, предъявляемые к препаратам железа, — это достаточное содержание в них элементарного железа и отсутствие побочных эффектов и осложнений. В настоящее время на фармацевтическом рынке России достаточный выбор препаратов железа, что расширяет возможности врача и позволяет учитывать индивидуальные особенности пациентов при назначении лечения (табл. 1). В частности, появились удобные формы для детей младшего возраста — капли и сироп (феррум лек, мальтофер, актиферрин, гемофер).
Все препараты зарегистрированы и разрешены к применению в Российской Федерации.
Современные препараты железа разделяют на две группы:
Усвояемость железа из лекарственного препарата зависит от содержания в нем элементарного (активного) железа. Наибольшее количество элементарного железа содержится в препаратах, в которых железо представлено в виде фумарата (ферретаб, ферронат) или сульфата двухвалентного железа (актиферрин, ферро-фольгамма, гемофер пролангатум, ферро-градумет). В настоящее время появились препараты железа нового поколения, к которым относятся лекарственные средства, представленные гидроксид-полимальтозным комплексом трехвалентного железа (мальтофер, феррум лек). Особенностью этих препаратов является то, что поступление железа из кишечника в кровь происходит путем активного всасывания в отличие от солевых соединений железа, всасывание которых происходит по градиенту концентрации. Это важно, поскольку исключается возможность передозировки препаратов железа, содержащих гидроксид-полимальтозный комплекс трехвалентного железа.
Солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи и с другими лекарствами, что затрудняет абсорбцию железа. Поэтому эта группа препаратов железа назначается за час до еды. Однако на фоне выраженного свободнорадикального стресса, возникающего при взаимодействии железа со слизистой кишечника во время его диффузии, усиливается повреждающее действие на слизистую кишечника соединений железа, что проявляется диспепсическими расстройствами, вплоть до некроза слизистой. При плохой переносимости солевых препаратов железа их можно принимать и во время еды, что уменьшит побочные проявления, но и всасывание железа в свою очередь будет ухудшаться. Солевые препараты железа нельзя запивать чаем, молоком и сочетать их с приемом некоторых медикаментов (тетрациклинов, левомицетина, препаратов кальция, антацидов, пеницилламина), поскольку при этом снижается усвояемость железа.
Препараты неионного железа, как показывают проведенные исследования, не взаимодействуют с компонентами пищи и лекарствами, что позволяет использовать эти препараты, не нарушая режима питания детей (препараты можно добавлять в пищу, соки) и схемы терапии сопутствующей патологии (если есть необходимость в проведении такого лечения).
Суточная терапевтическая доза препаратов железа должна быть достаточной для нормализации уровня гемоглобина и восполнения запасов железа в костном мозге, что составляет для солевых препаратов железа 3-6 мг/кг/сут элементарного железа в два-три приема. Гидроксид-полимальтозный комплекс железа (феррум лек) назначается в дозе 3-6 мг/кг/сут в один или несколько (по желанию пациента) приемов.
Побочные реакции при приеме препаратов железа
Наиболее часто при лечении ферропрепаратами наблюдаются следующие побочные явления (табл. 2): металлический привкус во рту, потемнение эмали зубов, аллергические высыпания на коже, диспепсические нарушения в результате раздражающего действия на слизистую пищеварительного тракта, прежде всего кишечника (жидкий стул, тошнота, рвота). Поэтому начальные дозы препаратов должны составлять 1/2-1/3 терапевтической с последующим увеличением их до полной дозы в течение нескольких дней во избежание возникновения выраженных побочных действий. При непереносимости солевого препарата его можно заменить гидроксид-полимальтозным комплексом железа, в результате применения которого не возникает вышеописанных эффектов. Гидроксид-полимальтозный комплекс железа можно сразу применять в полной дозе. Неионные препараты железа не вызывают перечисленных выше побочных эффектов, чувство переполнения желудка также отмечается редко.
Парентеральное введение препаратов железа
Парентеральное введение препаратов железа проводится только по строгим показаниям из-за развития выраженных местных и системных побочных эффектов. Показания таковы: патология пищеварительного тракта (синдром нарушенного кишечного всасывания, неспецифический язвенный колит, хронический энтероколит, желудочно-кишечное кровотечение) и непереносимость железосодержащих препаратов при пероральном приеме.
Противопоказаниями к назначению препаратов железа являются анемии, не обусловленные дефицитом железа (гемолитические, апластические), гемосидероз, гемохроматоз.
Продолжительность курса лечения
Клинический и терапевтический эффекты при пероральной ферротерапии развиваются постепенно. Через некоторое время появляется клиническое улучшение: уменьшается слабость, исчезает головокружение, ребенок становится более активным, повышается аппетит, постепенно розовеют кожные покровы и видимые слизистые. На 8-10-й день терапии отмечается ретикулоцитарный криз — до 5%, что подтверждает эффективность лечения. Позже наблюдается повышение уровня гемоглобина, чаще всего нормализация гемоглобина происходит на 3-6-й неделе от начала терапии и зависит от степени тяжести анемии. В среднем уровень Hb повышается на 10 г/л за 10 дней. Однако нормализация уровня гемоглобина не является признаком устранения дефицита железа. Для полного восполнения депо железа в организме курс ферротерапии должен составлять не менее 3 месяцев.
Причины неэффективности ферротерапии
Неэффективность терапии на фоне приема препаратов железа при их хорошей переносимости может быть обусловлена следующими факторами:
ЖДА — это заболевание, при правильной терапии которого наступает полное выздоровление!
Ферритин
Сначала, давайте разберемся в самом понятии «ферритин».
Ферритин – сложный белковый комплекс, выполняющий роль основного внутриклеточного депо железа. Можно назвать его своеобразным сейфом, где собирается и копится железо, которое будет предоставлено организму, в экстренном случае. Именно ферритин показывает есть ли у вас предрасположенность к анемии, а не гемоглобин, как многие думают.
Обычно, референсное значение ферритина колеблется от 5 мкг/л до 148 мкг/л. Но как понять, какое значение анализа ферритина является вашей нормой?
Запомните, идеальной цифры ферритина не существует. Это ИНДИВИДУАЛЬНАЯ цифра.
Нижняя граница значения – показатель вашего веса.
Верхняя граница ферритина, когда мы говорим, что это не патология – это 300 мкг/л.
Индивидуальный уровень ферритина рассчитывается по формуле: ваш вес(кг) + 70 мкг/л.
Например, у девушки весом 60 кг., индивидуальный показатель ферритина равен 130 мкг/л.
Мы не ставим диагноз железодефицитной анемии по гемоглобину, необходимо увидеть значение ферритина, потому что это первый и самый ранний показатель признака дефицита железа. А желательно, знать показатели эритроцитов, трансферрина, коэффициент насыщения трансферрина, ОЖСС, сывороточного железа, цветового показателя, MCV, MCH.
Основывать выводы по поводу железодефицитной анемии, рассматривая только показатель гемоглобина, неправильно. Ферритин запасает железо, чтобы в любом экстренном случае анемия не наступила. Если гемоглобин со 120 упадет, а ферритин будет на отметке – 6, анемия не заставит себя ждать.
Задумаетесь о запасах железа на «чёрный» день уже сейчас, тогда падение гемоглобина не будет сопровождаться усталостью, низким КПД, и прочими неприятными эффектами анемии. Ведь на помощь придет ферритин.
Сдавайте анализы, учитывайте все факторы и будьте здоровы!
Дефицит железа и когнитивные расстройства у детей
Риск развития железодефицитной анемии (ЖДА) наиболее высок у детей раннего возраста, подростков, а также у беременных женщин. Около 70–80% всех диагностируемых анемий связаны с дефицитом железа. У детей раннего
Риск развития железодефицитной анемии (ЖДА) наиболее высок у детей раннего возраста, подростков, а также у беременных женщин. Около 70–80% всех диагностируемых анемий связаны с дефицитом железа. У детей раннего возраста частота сидеропении достигает 73%, при этом вероятность перехода латентного дефицита железа в анемию очень высока [1]. Железо, в силу важности выполняемых им функций, признано эссенциальным, т. е. жизненно необходимым: оно является обязательным и незаменимым компонентом ферментных систем организма, обеспечивающих должный уровень системного и клеточного аэробного метаболизма. С участием этого микроэлемента в организме осуществляются такие биохимические процессы, как транспорт электронов (цитохромы, железосеропротеиды), транспорт и депонирование кислорода (миоглобин, гемоглобин), синтез ДНК, тканевое дыхание. Железо участвует в работе окислительно-восстановительных ферментов (оксидаза, гидроксилаза, супероксиддисмутаза). Депонируется железо при избытке поступления в организм в виде железосодержащих веществ (ферритин и гемосидерин). В то же время свободное железо обладает способностью образовывать свободные радикалы, которые могут повреждать такие важнейшие биологические структуры, как липиды, протеины и ДНК, т. е. являться прооксидантом и оказывать токсическое влияние на организм человека.
Самый важный регулирующий центр гомеостаза железа в организме человека находится на апикальной и базолатеральной мембранах эпителия двенадцатиперстной кишки. Апикальная мембрана энтероцита обращена в просвет кишечника и специализируется на транспорте в клетки гемового и двухвалентного железа. Наиболее интенсивно железо транспортируется через двухвалентный транспортер металла белок DMT1. Базолатеральная мембрана участвует в переносе железа, транспортированного в клетки кишечного эпителия, в плазму крови. Железо, не транспортированное в плазму, выводится из организма путем отшелушивания эпителия кишечника. Запасы железа хранятся в организме в виде ферритина и гемосидерина. При этом ферритин обнаруживается практически во всех клетках, представляя собой легкодоступный резерв железа в растворимой, нетоксичной форме. Наиболее богаты ферритином клетки-предшественники эритроцитов в костном мозге, макрофаги, ретикуло-эндотелиальные клетки печени. При дефиците железа в организме истощаются именно эти запасы. Показателями дефицита железа в организме служат снижение уровня сывороточного ферритина, уменьшение содержания железа в сыворотке крови, повышение ее железосвязывающей способности. Дефицит железа приводит к нарушению иммунитета, снижению работоспособности и ухудшает функционирование головного мозга.
Согласно современным исследованиям, наибольшее содержание железа после гемоглобина эритроцитов наблюдается в клетках головного мозга. Youdim и соавторы (1989) показали, что обмен железа в тканях головного мозга находится на более низком уровне, чем в печени, так как клетки головного мозга имеют низкую способность депонирования данного микроэлемента. Однако, в отличие от печени, головной мозг дольше удерживает железо, что препятствует истощению его запасов. В то же время на фоне ферротерапии железо быстрее накапливается в печени, нежели в головном мозге [3]. Железо в тканях головного мозга участвует в генерации импульсов в нервных синапсах, в процессах миелинизации нервных волокон, оказывает влияние на функции гипоталамуса [4]. В случае недостатка железа снижаются количество и чувствительность допаминовых рецепторов Д2, что ведет к нарушению метаболизма допамина в нервных синапсах, в результате чего уменьшается стимулирующий эффект на следующую клетку и сокращается количество проходящих импульсов [4, 5]. Эксперименты, проведенные John L. Beard (2001) на крысах, у которых наблюдался дефицит железа, показали, что недостаток железа сопровождается уменьшением концентрации экстрацеллюлярного допамина в полосатом ядре мозга, в связи с чем уменьшается активность транспортного белка допамина — ДАТ (допаминовый транспортер), активизирующего Д2-рецепторы на пресинаптической мембране [4]. Авторы пришли к выводу, что в условиях дефицита железа происходит перестройка допаминовых рецепторов и увеличение синтеза опиатных пептидов, блокирующих активность ДАТ, что со временем приводит к нарушениям поведения, моторики. Таким образом, дефицит железа может оказывать специфическое воздействие как на центральную нервную систему (нервные клетки, миелин), так и на процесс передачи нервных импульсов [6]. Результаты экспериментальных исследований показали, что дефицит железа, сопровождающийся снижением дофаминергической активности, может привести к изменению поведенческих реакций [7], познавательных функций, негативно повлиять на способность к обучению и память.
Дефицит железа определяется более чем у четверти всего населения земного шара [8]. В течение последних 20 лет проводились многочисленные исследования, посвященные влиянию дефицита железа на различные функции организма. Наиболее убедительными оказались результаты исследований B. Lozoff с коллегами [9, 10, 13], подтвердившие наличие отдаленных неблагоприятных эффектов сидеропении. С целью контроля использовался полный набор тестов, отражающих когнитивное, психоэмоциональное и двигательное развитие, а также проводилась оценка успеваемости в школе. Авторы показали, что подростки, которые в младенческом возрасте имели хронический, тяжелый дефицит железа, получали более низкие баллы при оценке их умственной и двигательной активности. После учета фоновых факторов различия оставались статистически достоверными при выполнении арифметических и письменных заданий, оценке моторной активности, а также некоторых особых когнитивных процессов (пространственная, избирательная память и др.). Многие из детей, в прошлом имевшие дефицит железа, оставались на второй год обучения или обращались за дополнительной помощью в учебе. Родители и учителя оценивали их поведение как проблемное, отмечали у детей беспокойство или депрессию, трудности в общении и проблемы, связанные с отсутствием внимания. Таким образом, тяжелый длительный дефицит железа в раннем возрасте может проявляться впоследствии задержкой развития и изменением поведенческих реакций. Таким детям требуется дополнительная помощь во время учебы в школе, что является важным аргументом в пользу профилактики дефицита железа в раннем возрасте. Учитывая, что развитие головного мозга, процессы его дифференцировки относятся преимущественно к перинатальному периоду и к первым годам жизни, необходима коррекция дефицита железа именно в раннем возрасте [14, 15].
Выбору препарата для коррекции сидеропении придается особое значение, поскольку длительность лечения может составлять от нескольких недель до нескольких месяцев. При этом важны не только эффективность, но и отсутствие побочных эффектов и осложнений, приверженность к проводимой терапии, особенно в педиатрической практике. Главными требованиями, предъявляемыми к препаратам железа для приема внутрь, используемым в детской практике, являются: достаточная биодоступность, высокая безопасность, хорошие органолептические характеристики, лекарственные формы, удобные для пациентов всех возрастов. Этим критериям в наибольшей степени отвечают препараты железа на основе гидроксид-полимальтозного комплекса (феррум лек, мальтофер). Нами были проведены обследования 101 ребенка с железодефицитным состоянием с ЖДА — 48, с латентным дефицитом железа (ЛДЖ)— 33), а также группы детей (20 человек) без сидеропении. В исследование были включены дети в возрасте от 4 мес до 5 лет, из них 60% мальчиков и 39,6% девочек. Подавляющее большинство детей (81%) были в возрасте 1–3 лет, средний возраст — 1 год 8 мес. Наблюдение осуществлялось в домах ребенка № 8 и № 24 Москвы. По этическим соображениям контрольную группу плацебо не набирали. При этом нарушения физического и психического развития (задержка развития) выявлялись с высокой частотой в обеих группах и мало отличались у детей с ЖДА (отставание в физическом развитии в 1-й группе выявлено у 48% детей, во второй — у 54%; отставание в психическом развитии отмечалось у 70% детей 1-й группы и у 66% малышей во 2-й группе) и ЛДЖ (отставание в физическом развитии в 1-й группе выявлено у 35% детей, у 47% — во 2-й; отставание в психическом развитии отмечалось у 48% детей 1-й группы и у 53 % — 2-й группы). Все дети с железодефицитным состоянием получали препараты железа. Период наблюдения составил от 3 до 12 мес. На фоне приема препаратов у испытуемых отмечалось уменьшение симптомов мышечной гипотонии, улучшилось состояние кожи и ее придатков, значительно изменились к лучшему показатели психического и физического развития. При этом не было выявлено побочных эффектов.
Н. А. Коровина, доктор медицинских наук, профессор
И. Н. Захарова, доктор медицинских наук, профессор
В. И. Свинцицкая
РМАПО, Москва

